Resumo
A 9,10-Antraquinona (AQ) é um contaminante com um risco carcinogênico potencial e ocorre no chá em todo o mundo. O limite máximo de resíduos (MRL) do AQ no chá definido pela União Europeia (UE) é de 0,02 mg/kg. As possíveis fontes de AQ no processamento do chá e os principais estágios de sua ocorrência foram investigados com base em uma análise de espectrometria de massa de massa de cromatografia em tandem de AQ modificada e cromatografia gasosa (GC-MS/MS). Comparado à eletricidade como fonte de calor no processamento do chá verde, a AQ aumentou 4,3 a 23,9 vezes no processamento do chá com carvão como fonte de calor, excedendo em muito 0,02 mg/kg, enquanto o nível de AQ no ambiente triplicou. A mesma tendência foi observada no processamento de chá de Oolong sob calor de carvão. As etapas com contato direto entre folhas de chá e fumaça, como fixação e secagem, são consideradas as principais etapas da produção de AQ no processamento do chá. Os níveis de AQ aumentaram com o aumento do tempo de contato, sugerindo que altos níveis de poluente da AQ no chá podem ser derivados dos fumos causados pelo carvão e pela combustão. Quatro e amostras de diferentes workshops com eletricidade ou carvão como fontes de calor foram analisadas, variou de 50,0% -85,0% e 5,0% -35,0% para detecção e exceder as taxas de aq. Além disso, o conteúdo máximo de AQ de 0,064 mg/kg foi observado no produto do chá com carvão como fonte de calor, indicando que os altos níveis de contaminação da AQ em produtos de chá provavelmente serão contribuídos pelo carvão.
Palavras-chave: 9,10-Antraquinona, processamento de chá, carvão, fonte de contaminação
INTRODUÇÃO
O chá fabricado a partir de folhas do arbusto sempre -verde Camellia sinensis (L.) O. Kuntze, é uma das bebidas mais populares devido ao seu sabor refrescante e benefícios à saúde. Em 2020, a produção de chá aumentou para 5.972 milhões de toneladas, o que foi uma duplicação nos últimos 20 anos [1]. Com base em diferentes maneiras de processamento, existem seis tipos principais de chá, incluindo chá verde, chá preto, chá escuro, chá oolong, chá branco e chá amarelo [2,3]. Para garantir a qualidade e a segurança dos produtos, é muito importante monitorar os níveis de poluentes e definir a origem.
Identificar as fontes de contaminantes, como resíduos de pesticidas, metais pesados e outros poluentes, como hidrocarbonetos aromáticos policíclicos (PAHs), é a etapa principal para controlar a poluição. A pulverização direta de produtos químicos sintéticos nas plantações de chá, bem como a deriva do ar causada por operações perto de jardins de chá, são a principal fonte de resíduos de pesticidas no chá [4]. Os metais pesados podem se acumular no chá e levar à toxicidade, que são derivados principalmente do solo, fertilizante e atmosfera [5-7]. Quanto a outras poluições que aparecem inesperadamente no chá, foi bastante difícil identificar devido aos complexos procedimentos da cadeia de chá de produção, incluindo plantação, processamento, pacote, armazenamento e transporte. Os PAHs em chá vieram da deposição de escapamentos de veículos e da combustão de combustíveis usados durante o processamento de folhas de chá, como lenha e carvão [8-10].
Durante a combustão de carvão e lenha, poluentes como óxidos de carbono são formados [11]. Como resultado, é suscetível que os resíduos desses poluentes acima mencionados ocorram nos produtos processados, como grãos, estoque defumado e peixes de gato, a alta temperatura, representando uma ameaça à saúde humana [12,13]. Os PAHs causados pela combustão são derivados da volatilização dos PAHs contidos nos próprios combustíveis, a decomposição de alta temperatura dos compostos aromáticos e a reação composta entre os radicais livres [14]. A temperatura de combustão, o tempo e o teor de oxigênio são fatores importantes que afetam a conversão de HAPs. Com o aumento da temperatura, o conteúdo de PAHS aumentou e depois diminuiu, e o valor de pico ocorreu a 800 ° C; O teor de PAHS diminuiu acentuadamente para rastrear com o aumento do tempo de combustão quando estava abaixo de um limite chamado 'tempo de contorno', com o aumento do teor de oxigênio no ar de combustão, as emissões de PAHs reduziram significativamente, mas a oxidação incompleta produziria OPAHs e outros derivados [15 a 17].
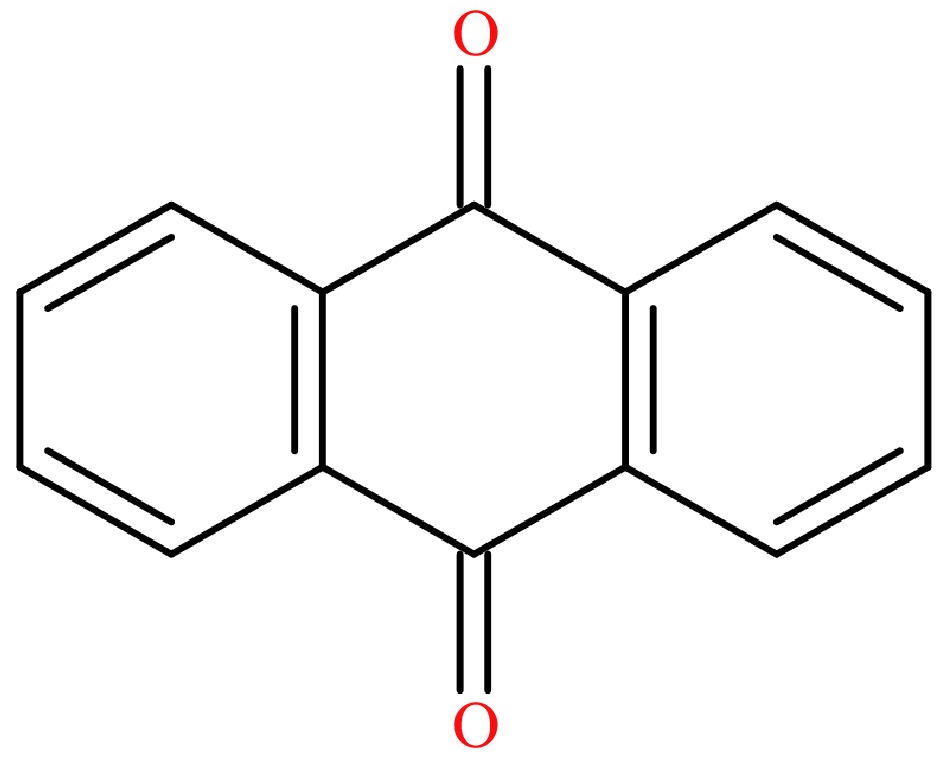
9,10-Antraquinona (AQ, CAS: 84-65-1, Fig. 1), um derivado contendo oxigênio dos PAHs [18], consiste em três ciclos condensados. Foi listado como um possível carcinogênio (Grupo 2B) pela Agência Internacional de Pesquisa sobre Câncer em 2014 [19]. O AQ pode envenenar o complexo de clivagem da Topoisomerase II e inibir a hidrólise do trifosfato de adenosina (ATP) pela Topoisomerase II do DNA, causando quebras de fita dupla do DNA, o que significa que a exposição a longo prazo no ambiente e o risco direto de câncer e o aumento do câncer [o aumento do câncer de altura de AQ pode levar a um aumento de danos e o aumento de DNA, o aumento do risco de AQ e o aumento do câncer e o aumento de DNA. Como efeitos negativos na saúde humana, o limite máximo de resíduos da AQ (MRL) de 0,02 mg/kg foi ambientado no chá pela União Europeia. De acordo com nossos estudos anteriores, os depósitos da AQ foram sugeridos como a principal fonte durante a plantação de chá [21]. Além disso, com base nas consequências experimentais no processamento de chá verde e preto da Indonésia, é óbvio que o nível de AQ mudou significativamente e a fumaça do equipamento de processamento foi sugerida como uma das principais razões [22]. No entanto, a origem precisa da AQ no processamento do chá permaneceu ilusória, embora algumas hipóteses da via química da AQ tenham sido sugeridas [23,24], indicando que é extremamente importante determinar os fatores cruciais que afetam o nível de AQ no processamento do chá.
Figura 1. A fórmula química de Aq.
Dada a pesquisa sobre a formação da AQ durante a combustão de carvão e a ameaça potencial de combustíveis no processamento do chá, foi realizado um experimento comparativo para explicar o efeito do processamento de fontes de calor na AQ no chá e no ar, análise contábil no conteúdo de AQ em diferentes etapas de processamento, que é útil para confirmar a origem da precisão, o padrão de ocorrência e o grau de AQ de AQ em poluição de AQ, que é útil para confirmar a precisão, a ocorrência de ocorrência e o grau de AQ poluição de AQ em poluição por AQ, que são úteis para confirmar a precisão, a ocorrência de ocorrência e o grau de AQ de AQ.
Resultados
Validação do método
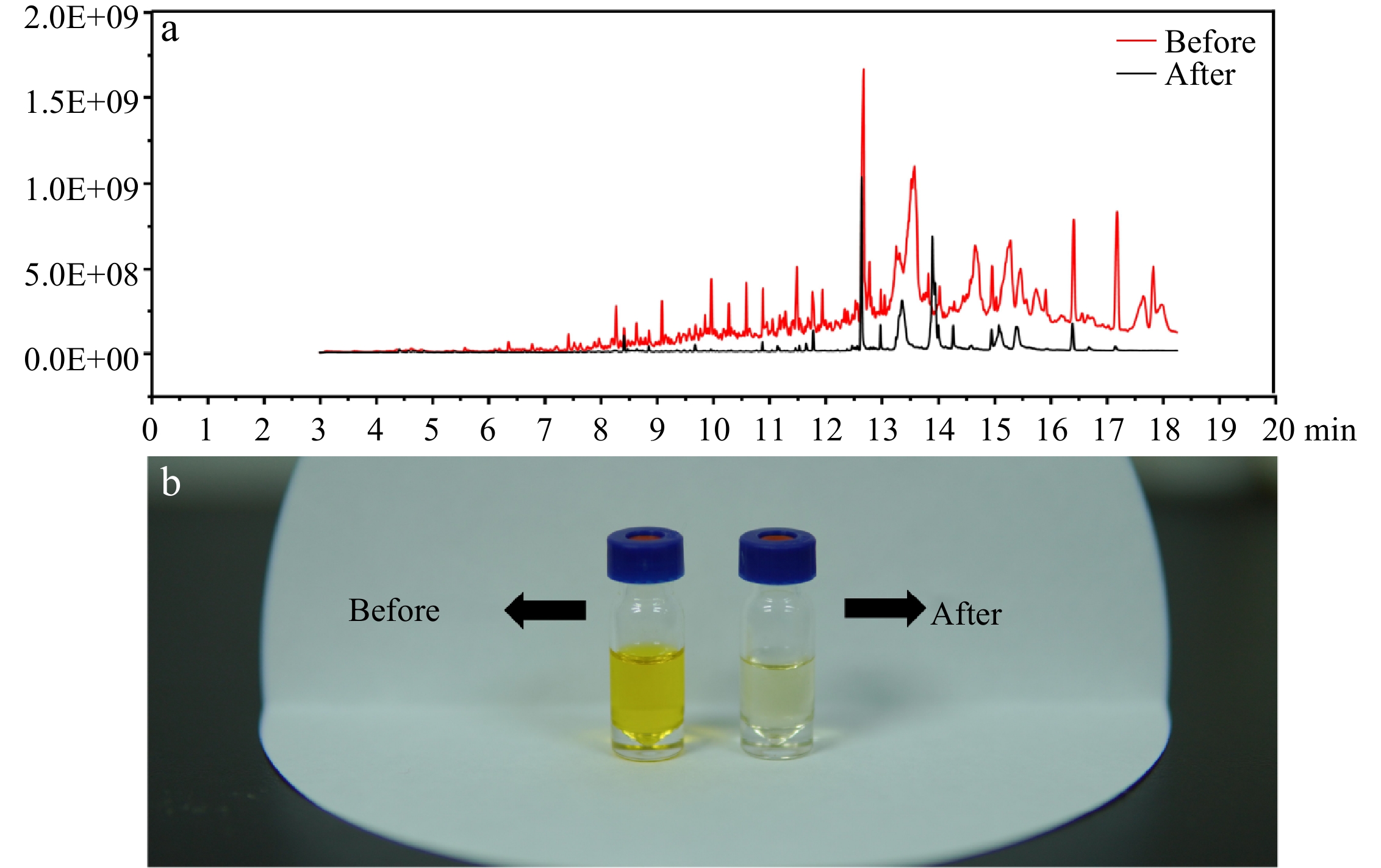
Comparado com nosso estudo anterior [21], um procedimento de extração líquido-líquido foi combinado antes da injeção ao GC-MS/MS, a fim de melhorar a sensibilidade e manter as declarações instrumentais. Na Fig 2b, o método aprimorado mostrou uma melhora significativa na purificação da amostra, o solvente ficou de cor mais clara. Na Fig 2a, um espectro completo de varredura (50-350 m/z) ilustrou que, após a purificação, a linha de base do espectro MS reduziu obviamente e os picos cromatográficos estavam disponíveis, indicando que um grande número de compostos interferentes foi removido após a extrração líquida-líquido.
Figura 2. (A) Espectro completo de varredura da amostra antes e depois da purificação. (b) O efeito de purificação do método aprimorado.
A validação do método, incluindo linearidade, recuperação, limite de quantificação (LOQ) e efeito da matriz (ME), são mostrados na Tabela 1. É satisfatório obter a linearidade com o coeficiente de determinação (R2) superior a 0,998, que variou de 0,005 a 0,2 mg/kg de aeronaves em um matricial de chá e acetilente e acetilente, o reto de um retenção de 0,998, que varia de 0,005 a 0,2 mg em um alcance de um matricial de TEA e ACETILVILENT, a MAg.
A recuperação de AQ foi avaliada em três concentrações de cravos entre concentrações medidas e reais no chá seco (0,005, 0,02, 0,05 mg/kg), brotos de chá frescos (0,005, 0,01, 0,02 mg/kg) e amostra de ar (0,5, 1,5, 3 μg/m3). A recuperação da AQ no chá variou de 77,78% a 113,02% no chá seco e de 96,52% a 125,69% em brotos de chá, com RSD% abaixo de 15%. A recuperação da AQ em amostras de ar variou de 78,47% a 117,06%, com RSD% abaixo de 20%. A concentração mais baixa de Spiked foi identificada como LOQ, que foi de 0,005 mg/kg, 0,005 mg/kg e 0,5 μg/m³ em brotos de chá, chá seco e amostras de ar, respectivamente. Conforme listado na Tabela 1, a matriz de chá seca e brotos de chá aumentou ligeiramente a resposta da AQ, levando ao ME de 109,0% e 110,9%. Quanto à matriz de amostras de ar, o ME foi de 196,1%.
Os níveis de AQ durante o processamento do chá verde
Com o objetivo de descobrir os efeitos de diferentes fontes de calor no ambiente de chá e processamento, um lote de folhas frescas foi dividido em dois grupos específicos e processado separadamente em dois workshops de processamento na mesma empresa. Um grupo foi fornecido com eletricidade e o outro com carvão.
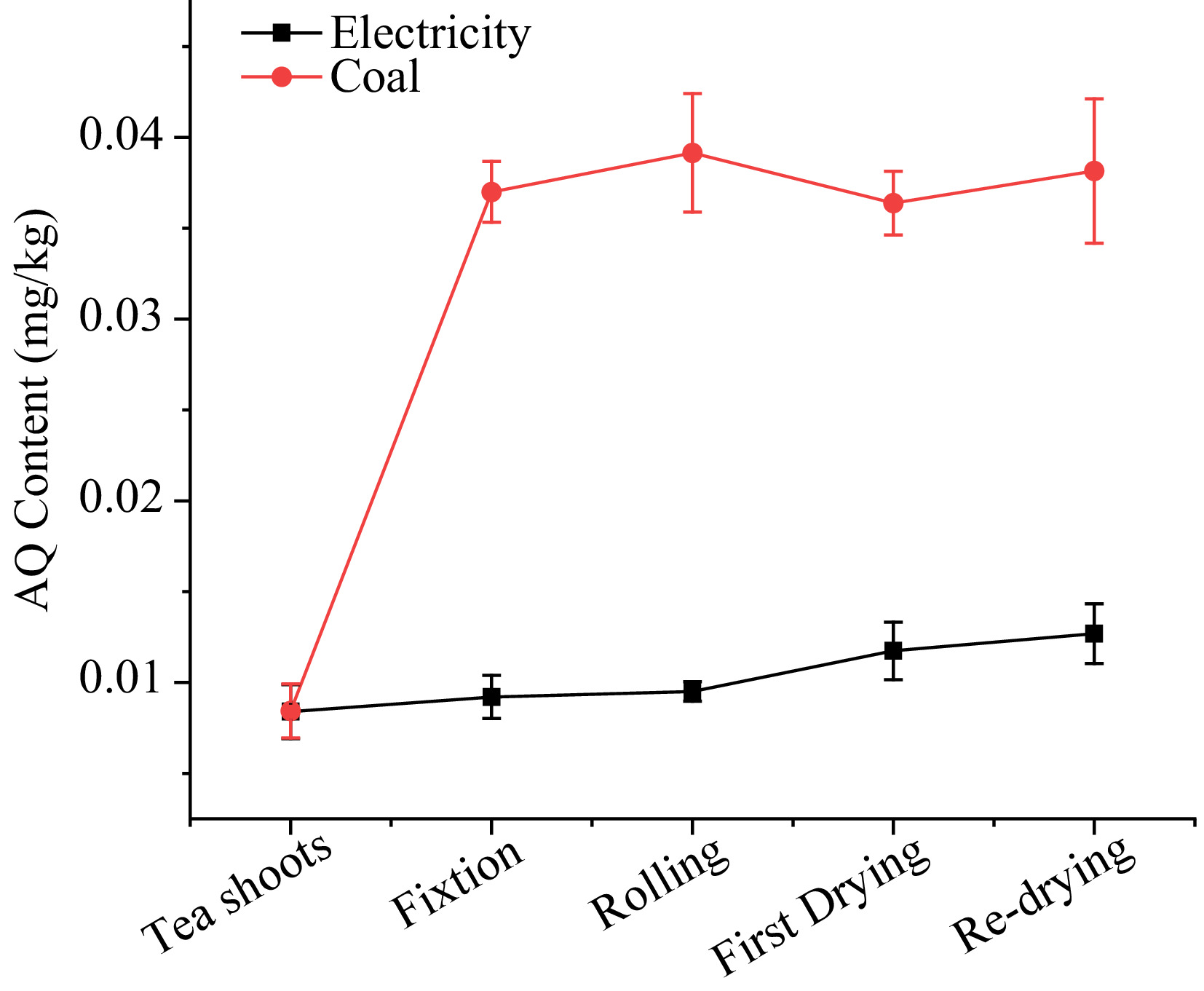
Como mostrado na Fig. 3, o nível de AQ com eletricidade como fonte de calor variou de 0,008 a 0,013 mg/kg. Durante o processo de fixação, o alcance das folhas de chá causado pelo processamento em uma panela com alta temperatura resultou em um aumento de 9,5% na aq. Então, o nível de AQ permaneceu durante o processo de rolamento, apesar da perda de suco, sugerindo que os processos físicos podem não afetar o nível de AQ no processamento do chá. Após as primeiras etapas de secagem, o nível de AQ aumentou ligeiramente de 0,010 para 0,012 mg/kg e continuou subindo para 0,013 mg/kg até o final do re-secagem. Os PFs, que mostraram significativamente a variação em cada etapa, foram 1,10, 1,03, 1,24, 1,08 em fixação, rolagem, secagem e re-secagem, respectivamente. Os resultados do PFS sugeriram que o processamento sob energia elétrica teve um pequeno efeito nos níveis de AQ no chá.
Figura 3. O nível de AQ durante o processamento do chá verde com eletricidade e carvão como fontes de calor.
No caso do carvão como fonte de calor, o conteúdo de AQ aumentou acentuadamente durante o processamento do chá, aumentando de 0,008 para 0,038 mg/kg. 338,9% AQ foram aumentados no procedimento de fixação, atingindo 0,037 mg/kg, que excederam em muito o MRL de 0,02 mg/kg definido pela União Europeia. Durante o estágio de rolamento, o nível de AQ ainda aumentou 5,8%, apesar de estar longe da máquina de fixação. Na primeira secagem e re-secagem, o conteúdo de AQ aumentou pouco ou diminuiu um pouco. Os PFs usando carvão como fonte de calor na fixação, rolando a primeira secagem e re-secagem foram 4,39, 1,05, 0,93 e 1,05, respectivamente.
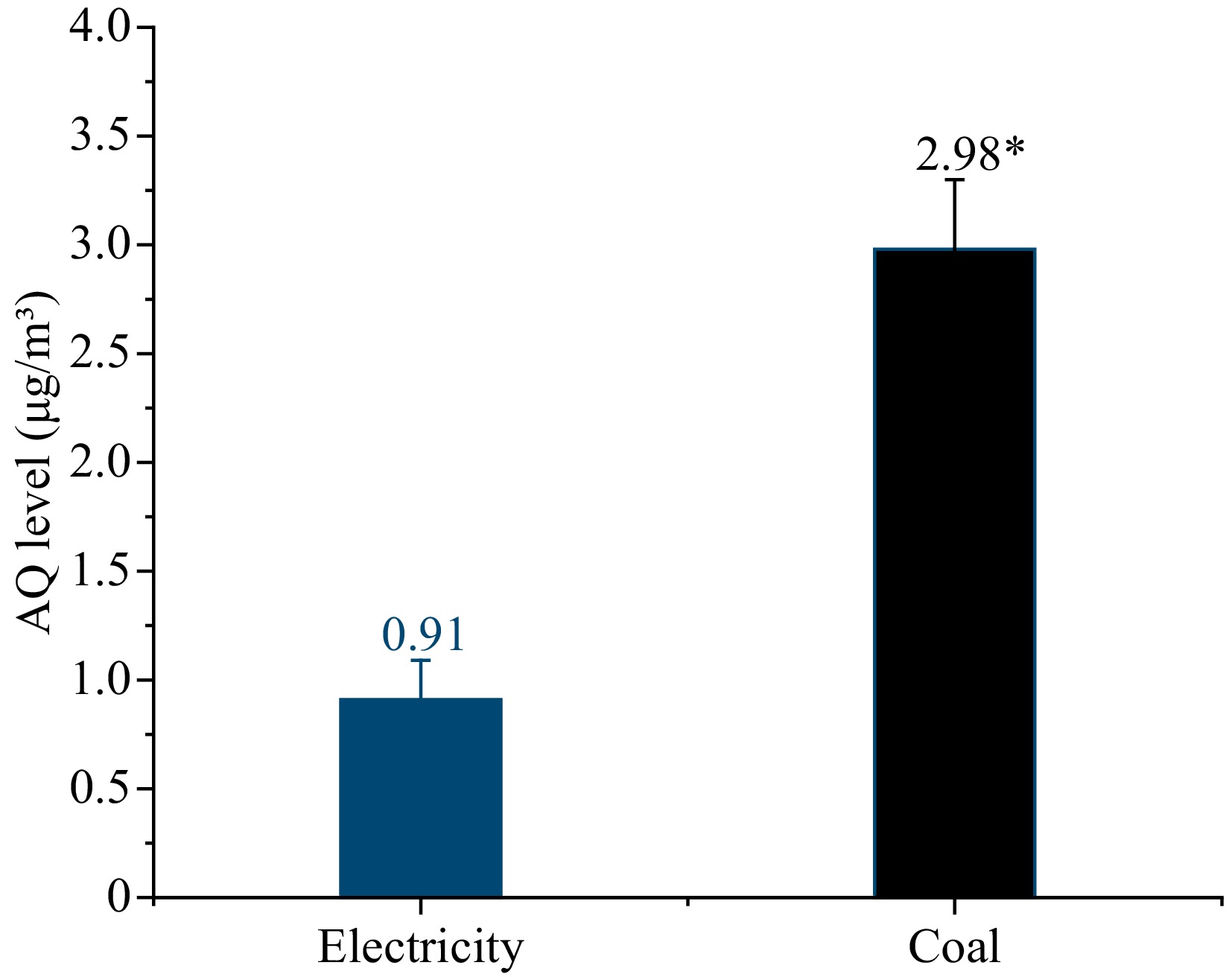
Para determinar ainda mais a relação entre a combustão de carvão e a poluição da AQ, as matérias particuladas suspensas (PMS) no ar nas oficinas sob ambas as fontes de calor foram coletadas para avaliação do ar, como mostrado na Fig. 4. O nível de AQ de PMS com carvão como a fonte de calor foi de 2,98 μg/m3, que foi mais alto que com a eletricidade 0,91 μg.
Figura 4. Os níveis de AQ no ambiente com eletricidade e carvão como fonte de calor. * Indica diferenças significativas nos níveis de AQ nas amostras (p <0,05).
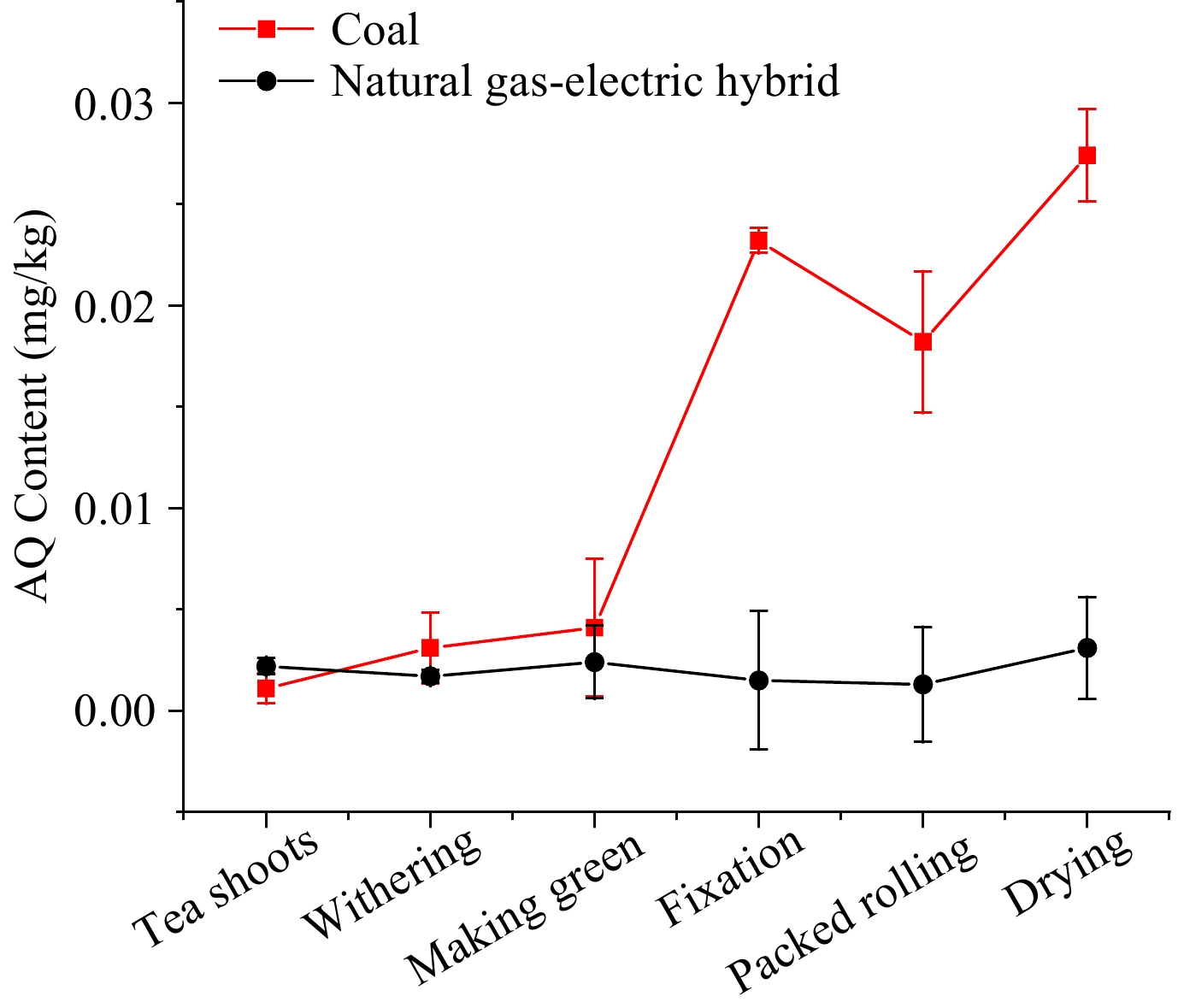
Os níveis de AQ durante o chá Oolong Processing Oolong Tea, produzidos principalmente em Fujian e Taiwan, são uma espécie de chá parcialmente fermentado. Para determinar ainda mais as principais etapas do aumento do nível de AQ e dos efeitos de diferentes combustíveis, o mesmo lote de folhas frescas foi transformado em chá de oolong com carvão e híbrido de gás-elétrico natural que as fontes de calor, simultaneamente. Os níveis de AQ no processamento de chá de Oolong usando diferentes fontes de calor são mostrados na Fig. 5. Para o processamento de chá oolong com híbrido de gás-elétrico natural, a tendência do nível de AQ estava estagnada abaixo de 0,005 mg/kg, que era semelhante à do chá verde com eletricidade.
Figura 5. O nível de AQ durante o processamento de chá de Oolong com mistura e carvão de gás-eletrônico natural como fonte de calor.
Com o carvão como fonte de calor, os níveis de AQ nos dois primeiros passos, murchando e fazendo verde, eram essencialmente os mesmos da mistura de gás-elétrico natural. No entanto, os procedimentos subsequentes até a fixação mostraram que a lacuna aumentou gradualmente, momento em que o nível de AQ aumentou de 0,004 para 0,023 mg/kg. O nível na etapa de rolamento embalado diminuiu para 0,018 mg/kg, o que pode ser devido à perda de suco de chá que leva alguns contaminantes da AQ. Após o estágio de rolamento, o nível no estágio de secagem aumentou para 0,027 mg/kg. Ao murchar, fazer verde, fixação, rolagem e secagem embaladas, os PFs foram 2,81, 1,32, 5,66, 0,78 e 1,50, respectivamente.
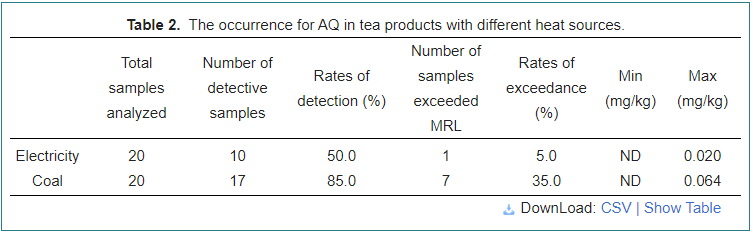
A ocorrência de aq em produtos de chá com diferentes fontes de calor
To determine the effects on AQ content of tea with different heat sources, 40 tea samples from the tea workshops using electricity or coal as heat sources were analyzed, as shown in Table 2. Compared with using electricity as a heat source, coal had the most detective rates (85.0%) with the maximum AQ level of 0.064 mg/kg, indicating that it was easy to cause AQ contaminant by fumes produced by coal combustion, and a rate of 35,0% foram observados em amostras de carvão. Mais conspícuo, a eletricidade teve as taxas mais baixas de detetive e excedância de 56,4% e 7,7%, respectivamente, com o conteúdo máximo de 0,020 mg/kg.
DISCUSSÃO
Com base no PFS durante o processamento com os dois tipos de fontes de calor, ficou claro que a fixação foi a principal etapa que levou ao aumento dos níveis de AQ na produção de chá com carvão e processamento sob energia elétrica, teve um pequeno efeito no conteúdo da AQ no chá. Durante o processamento do chá verde, a combustão de carvão produziu muitos fumos no processo de fixação em comparação com o processo de aquecimento elétrico, indicando que talvez a fumaça fosse a principal fonte de poluentes da AQ do contato com as brotes de chá instantaneamente no processamento de chá, semelhante ao processo de exposição nas amostras de churrasco fumadas [25]. O aumento ligeiramente do conteúdo de AQ durante o estágio de rolamento sugeriu que os fumos causados pela combustão de carvão não apenas afetaram o nível de AQ durante a etapa de fixação, mas também no ambiente de processamento devido à deposição atmosférica. Os carvões também foram usados como fonte de calor na primeira secagem e re-secagem, mas nessas duas etapas o conteúdo de AQ aumentou ligeiramente ou diminuiu ligeiramente. Isso pode ser explicado pelo fato de que o secador de vento quente fechado mantinha o chá longe dos fumos causados pela combustão de carvão [26]. Para determinar a fonte de poluentes, os níveis de AQ na atmosfera foram analisados, resultando em uma lacuna significativa entre as duas oficinas. A principal razão para isso é que o carvão usado na fixação, os estágios de secagem e re-secagem gerariam aq durante a combustão incompleta. Esses AQ foram então adsorvidos nas pequenas partículas de sólidos após a combustão de carvão e dispersas no ar, elevando os níveis de poluição da AQ no ambiente da oficina [15]. Com o tempo, devido à grande área de superfície específica e à capacidade de adsorção do chá, essas partículas se estabeleceram na superfície das folhas de chá, resultando no aumento da AQ na produção. Portanto, acredita -se que a combustão de carvão fosse a principal rota que levava à contaminação excessiva da AQ no processamento do chá, com a fumaça sendo a fonte de poluição.
Quanto ao processamento do chá de Oolong, a AQ foi aumentada em processamento com as duas fontes de calor, mas a diferença entre as duas fontes de calor foi significativa. Os resultados também sugeriram que o carvão como fonte de calor desempenhou um papel importante no aumento do nível de AQ, e a fixação foi considerada a principal etapa para aumentar a contaminação da AQ no processamento de chá de Oolong com base no PFS. Durante o processamento de chá de Oolong com híbrido de gás-elétrico natural como fonte de calor, a tendência do nível de AQ estava estagnada abaixo de 0,005 mg/kg, que era semelhante à do chá verde com eletricidade, sugerindo que a energia limpa, como eletricidade e gás natural, pode diminuir o risco de produzir contaminantes AQ do processamento.
Quanto aos testes de amostragem, os resultados mostraram que a situação da contaminância de AQ era pior ao usar o carvão como fonte de calor e não a eletricidade, o que pode ser devido à fumaça da combustão de carvão que entra em contato com as folhas de chá e a persistência pelo local de trabalho. No entanto, embora fosse óbvio que a eletricidade era a fonte de calor mais limpa durante o processamento do chá, ainda havia contaminante de AQ em produtos de chá usando eletricidade como fonte de calor. A situação parece um pouco semelhante ao trabalho publicado anteriormente, no qual a reação de 2 alcenos com hidroquinonas e benzoquinonas foi sugerida como uma via química potencial [23], as razões para isso serão investigadas em pesquisas futuras.
Conclusões
Neste trabalho, as possíveis fontes de poluição de AQ no chá verde e oolong foram confirmadas por experimentos comparativos com base em métodos analíticos de GC-MS/MS aprimorados. Nossas descobertas apoiaram diretamente que a principal fonte de poluente de altos níveis de AQ foi a fumaça causada pela combustão, o que não apenas afetou os estágios de processamento, mas também afetou os ambientes de oficina. Ao contrário dos estágios rolantes e murchas, onde as mudanças no nível da AQ eram discretas, os estágios com envolvimento direto de carvão e lenha, como fixação, são o principal processo em que a contaminação da AQ aumentou devido à quantidade de contato entre chá e fumos durante esses estágios. Portanto, combustíveis limpos, como gás natural e eletricidade, foram recomendados como fonte de calor no processamento do chá. Além disso, os resultados experimentais também mostraram que, na ausência de fumos gerados pela combustão, ainda havia outros fatores que contribuíram para rastrear AQ durante o processamento do chá, enquanto pequenas quantidades de AQ também foram observadas no workshop com combustíveis limpos, que devem ser investigados mais em pesquisas futuras.
MATERIAIS E MÉTODOS
Reagentes, produtos químicos e materiais
O padrão de antraquinona (99,0%) foi adquirido da Dr. EhrenStorfer GmbH Company (Augsburg, Alemanha). O padrão interno da D8-Antraquinona (98,6%) foi adquirido de isótopos C/D/N (Quebec, Canadá). Sulfato de sódio anidro (Na2SO4) e sulfato de magnésio (mgso4) (Xangai, China). Florisil foi fornecido pela Wenzhou Organic Chemical Company (Wenzhou, China). O papel de fibra de mircro-vidro (90 mm) foi adquirido da Ahlstrom-Munksjö Company (Helsinque, Finlândia).
Preparação de amostras
As amostras de chá verde foram processadas com fixação, rolagem, secagem e re-secagem (usando equipamentos fechados), enquanto as amostras de chá oolong foram processadas com murcha, fazendo verde (balançar e ficar em pé alternadamente), fixação, rolagem embalada e secagem. As amostras de cada etapa foram coletadas três vezes a 100g após mistura completa. Todas as amostras foram armazenadas a -20 ° C para análise posterior.
As amostras de ar foram coletadas por papel de fibra de vidro (90 mm) usando amostradores de volume médio (PTS-100, Qingdao Laoshan Electronic Instrument Company, Qingdao, China) [27], executando a 100 l/min por 4 h.
As amostras fortificadas foram picadas com AQ a 0,005 mg/kg, 0,010 mg/kg, 0,020 mg/kg para brotos de chá frescos, a 0,005 mg/kg, 0,020 mg/kg, 0,050 mg/kg para team seco e 0,012 mg/kg (0,5 µg/m2 SMAPLE DE AR), 0,072 mg/kg (3,0 µg/m3 para amostra de ar) para papel de filtro de vidro, respectivamente. Depois de tremer completamente, todas as amostras foram deixadas por 12 h, seguidas de etapas de extração e limpeza.
O teor de umidade foi obtido tomando 20 g da amostra após misturar cada etapa, aquecer a 105 ° C por 1 h, depois pesando e repetindo três vezes e tomando o valor médio e dividindo -o pelo peso antes do aquecimento.
Extração de amostra e limpeza
Amostra de chá: A extração e purificação da AQ a partir de amostras de chá foram realizadas com base no método publicado de Wang et al. com várias adaptações [21]. Resumidamente, 1,5 g de amostras de chá foram primeiro misturadas com 30 μL de D8-AQ (2 mg/kg) e deixadas para resistir por 30 min, depois bem misturadas com 1,5 ml de água desionizada e deixadas para ficar por 30 min. 15 mL de acetona 20% em n-hexano foram adicionados às amostras de chá e sonicados por 15 min. Em seguida, as amostras foram agitadas com 1,0 g de mgso4 por 30 s e centrifugadas por 5 min, a 11.000 rpm. Depois de serem movidos para frascos de 100 ml em forma de pêra, 10 ml da fase orgânica superior foram evaporados para quase a secura sob vácuo a 37 ° C. 5 ml 2,5% de acetona em n-hexano dissolveu o extrato em frascos em forma de pêra para purificação. A coluna de vidro (10 cm × 0,8 cm) consistia de baixo para cima da lã de vidro e 2G Florisil, que estava entre duas camadas de 2 cm de Na2SO4. Em seguida, 5 ml de acetona de 2,5% no n-hexano pré-lavou a coluna. Após carregar a solução redissolvida, o AQ foi eluído três vezes com 5 mL, 10 mL, 10 ml de acetona de 2,5% em n-hexano. Os eluatos combinados foram transferidos para frascos em forma de pêra e evaporados para quase a secura sob vácuo a 37 ° C. O resíduo seco foi então reconstituído com 1 mL de acetona a 2,5% em hexano, seguido de filtração através de um filtro de tamanho de poro de 0,22 µm. Em seguida, a solução reconstituída foi misturada com acetonitrila a uma proporção de volume de 1: 1. Após a etapa de agitação, o subnata foi usado para análise GC-MS/MS.
Amostra de ar: metade do papel de fibra, pingada com 18 μL de D8-AQ (2 mg/kg), foi imersa em 15 ml de acetona de 20% em n-hexano, depois sonicada por 15 min. A fase orgânica foi separada por centrifugação a 11.000 rpm por 5 min e toda a camada superior foi removida em um frasco em forma de pêra. Todas as fases orgânicas foram evaporadas para quase a secura sob vácuo a 37 ° C. 5 mL de 2,5% de acetona em hexano redissolveram os extratos para purificação da mesma maneira que nas amostras de chá.
Análise GC-MS/MS
O cromatógrafo a gás Varian 450 equipado com o Varian 300 Tandem Mass Detector (Varian, Walnut Creek, CA, EUA) foi usado para realizar a análise AQ com o software MS Workstation versão 6.9.3. Varian Factor Quatro coluna capilar VF-5ms (30 m × 0,25 mm × 0,25 μm) foi utilizada para separação cromatográfica. O gás transportador, hélio (> 99,999%), foi fixado em uma taxa de fluxo constante de 1,0 ml/min com gás de colisão de argônio (> 99,999%). A temperatura do forno começou a partir de 80 ° C e mantida por 1 min; aumentou a 15 ° C/min a 240 ° C, depois atingiu 260 ° C a 20 ° C/min e mantido por 5 minutos. A temperatura da fonte de íons foi de 210 ° C, bem como a temperatura da linha de transferência de 280 ° C. O volume de injeção foi de 1,0 μl. As condições MRM são mostradas na Tabela 3.
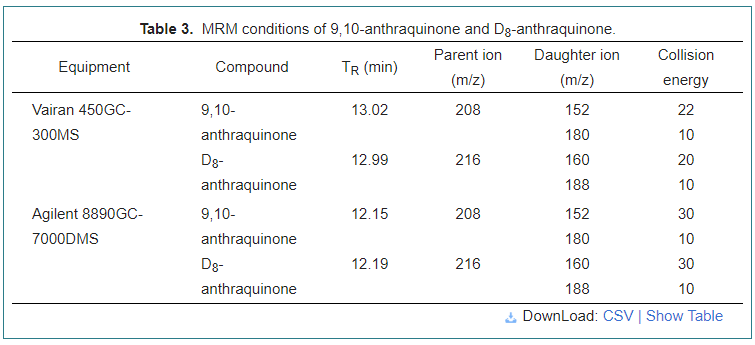
O cromatógrafo a gás Agilent 8890 equipado com o espectrômetro de massa de quadrupolo triplo Agilent 7000D (Agilent, Stevens Creek, CA, EUA) foi usado para analisar o efeito de purificação com o software MassHunter versão 10.1. A coluna Agilent J&W HP-5MS GC (30 m × 0,25 mm × 0,25 μm) foi usada para separação cromatográfica. O gás transportador, hélio (> 99,999%), foi fixado em uma taxa de fluxo constante de 2,25 ml/min com gás de colisão de nitrogênio (> 99,999%). A temperatura da fonte de íons EI foi ajustada a 280 ° C, a mesma que a temperatura da linha de transferência. A temperatura do forno começou a partir de 80 ° C e foi mantida por 5 min; levantado em 15 ° C/min a 240 ° C, depois atingiu 280 ° C a 25 ° C/min e mantido por 5 min. As condições MRM são mostradas na Tabela 3.
Análise Estatística
O conteúdo de AQ em folhas frescas foi corrigido para o conteúdo de matéria seca, dividindo -se pelo conteúdo de umidade, a fim de comparar e analisar os níveis de AQ durante o processamento.
As alterações da AQ em amostras de chá foram avaliadas com o software Microsoft Excel e o IBM SPSS Statistics 20.
O fator de processamento foi usado para descrever as alterações na AQ durante o processamento do chá. PF = RL/RF, onde RF é o nível AQ antes da etapa de processamento e RL é o nível AQ após a etapa de processamento. O PF indica uma diminuição (PF <1) ou um aumento (PF> 1) no resíduo AQ durante uma etapa específica de processamento.
ME indica uma diminuição (Me <1) ou um aumento (ME> 1) em resposta aos instrumentos analíticos, que se baseia na proporção de inclinações de calibração na matriz e solvente da seguinte forma:
Me = (slopeMatrix/slopesolvent - 1) × 100%
Onde a SlopeMatrix é a inclinação da curva de calibração no solvente pareado com matriz, a inclinação é a inclinação da curva de calibração no solvente.
Agradecimentos
Este trabalho foi apoiado pelo projeto principal de ciências e tecnologia na província de Zhejiang (2015c12001) e pela National Science Foundation of China (42007354).
Conflito de interesses
Os autores declaram que não têm conflito de interesses.
Direitos e permissões
Direitos autorais: © 2022 pelo (s) autor (s). Pressão Acadêmica Máxima do Licenciador Exclusivo, Fayetteville, GA. Este artigo é um artigo de acesso aberto distribuído sob a Licença de Atribuição do Creative Commons (CC por 4.0), visite https://creativecommons.org/license/by/4.0/.
Referências
[1] ITC. 2021. Boletim anual de estatísticas 2021. https://inttea.com/publication/
[2] Hicks A. 2001. Revisão da produção global de chá e o impacto na indústria da situação econômica asiática. AU Journal of Technology 5
Google Scholar
[3] Katsuno T, Kasuga H, Kusano Y, Yaguchi Y, Tomomura M, et al. 2014. Caracterização de compostos odorantes e sua formação bioquímica no chá verde com um processo de armazenamento de baixa temperatura. Food Chemistry 148: 388-95 doi: 10.1016/j.foodchem.2013.10.069
CrossRef Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Cadeia de poluição por tri-dimesion no ecossistema de chá e seu controle. Cientia Agricultura Sinica 40: 948-58
Google Scholar
[5] Ele H, Shi L, Yang G, You M, Vasseur L. 2020. Avaliação de risco ecológico de metais pesados do solo e resíduos de pesticidas nas plantações de chá. Agricultura 10:47 doi: 10.3390/Agriculture10020047
CrossRef Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J, et al. 2005. Contaminação de chumbo em folhas de chá e fatores não-ephic que a afetam. Quimosfera 61: 726-32 doi: 10.1016/j.chemosfera.2005.03.053
CrossRef Google Scholar
[7] Owuor Po, Obaga SO, Othieno Co. 1990. Os efeitos da altitude na composição química do chá preto. Journal of the Science of Food and Agriculture 50: 9-17 doi: 10.1002/jsfa.2740500103
CrossRef Google Scholar
[8] Garcia Londoño VA, Reynoso M, Resnik S. 2014. Hidrocarbonetos aromáticos policíclicos (PAHs) em Yerba Mate (Ilex Paraguariensis) do mercado argentino. Aditivos e contaminantes alimentares: Parte B 7: 247-53 doi: 10.1080/19393210.2014.919963
CrossRef Google Scholar
[9] Ishizaki A, Saito K, Hanioka N, Narimatsu S, Kataoka H. 2010. Determinação de hidrocarbonetos aromáticos policíclicos em amostras de alimentos por meio de cromatografia de fase sólida em tubos. Jornal de Cromatografia A 1217: 5555-63 doi: 10.1016/j.chroma.2010.06.068
CrossRef Google Scholar
[10] Phan Thi La, Ngoc NT, Quynh NT, Thanh NV, Kim TT, et al. 2020. Hidrocarbonetos aromáticos policíclicos (HAP) em folhas de chá seco e infusões de chá no Vietnã: níveis de contaminação e avaliação de risco alimentar. Geoquímica Ambiental e Saúde 42: 2853-63 doi: 10.1007/S10653-020-00524-3
CrossRef Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. A ocorrência de 16 EPA Pahs em Food - uma revisão. Compostos aromáticos policíclicos 35: 248-84 doi: 10.1080/10406638.2014.918550
CrossRef Google Scholar
[12] Omodara NB, Olabemiwo OM, Adedosu TA. 2019. Comparação de PAHs formados em lenha e estoque defumado de carvão e peixes de gato. American Journal of Food Science and Technology 7: 86-93 doi: 10.12691/AJFST-7-3-3
CrossRef Google Scholar
[13] Zou Ly, Zhang W, Atkiston S. 2003. A caracterização de emissões de hidrocarbonetos aromáticos policíclicos da queima de diferentes espécies de lenha na Austrália. Poluição ambiental 124: 283-89 doi: 10.1016/s0269-7491 (02) 00460-8
CrossRef Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL, et al. 2000. Atividade do benzo [A] pireno e seus metabólitos hidroxilados em um ensaio genético do receptor de estrogênio-α. Toxicological Sciences 55: 320−26 doi: 10.1093/toxsci/55.2.320
CrossRef Google Scholar
[15] Han Y, Chen Y, Ahmad S, Feng Y, Zhang F, et al. 2018. Medições de alto tempo e tamanho resolvido de PM e composição química da combustão de carvão: implicações para o processo de formação da CE. Ciência e Tecnologia Ambiental 52: 6676-85 doi: 10.1021/acs.est.7b05786
CrossRef Google Scholar
[16] Khiadani (Hajian) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M, et al. 2013. Determinação da concentração de hidrocarbonetos aromáticos policíclicos em oito marcas de chá preto que são mais usadas no Irã. Jornal Internacional de Engenharia de Saúde Ambiental 2:40 doi: 10.4103/2277-9183.122427
CrossRef Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J, Andrews G, Jones JM, et al. 2007. Emissão de espécies oxigenadas da combustão da madeira de pinheiro e sua relação com a formação de fuligem. Segurança do processo e proteção ambiental 85: 430-40 doi: 10.1205/pSep07020
CrossRef Google Scholar
[18] Shen G, Tao S, Wang W, Yang Y, Ding J, et al. 2011. Emissão de hidrocarbonetos aromáticos policíclicos oxigenados da combustão de combustível sólido interno. Ciência e Tecnologia Ambiental 45: 3459-65 doi: 10.1021/ES104364T
CrossRef Google Scholar
[19] Agência Internacional de Pesquisa sobre Câncer (IARC), Organização Mundial da Saúde. 2014. Espaços de motor a diesel e gasolina e alguns nitroarenos. Agência Internacional de Pesquisa sobre Monografias de Câncer sobre a avaliação de riscos carcinogênicos para os seres humanos. Relatório. 105: 9
[20] de Oliveira Galvão MF, de Oliveira Alves N, Ferreira PA, Caumo S, de Castro Vasconcellos P, et al. 2018. Partículas de queima de biomassa na região da Amazônia brasileira: efeitos mutagênicos de nitro e oxi-pahs e avaliação de riscos à saúde. Poluição Ambiental 233: 960−70 doi: 10.1016/j.envpol.2017.09.068
CrossRef Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H, et al. 2018. O depósito de 9,10-Antraquinona na plantação de chá pode ser um dos motivos da contaminação no chá. Food Chemistry 244: 254-59 doi: 10.1016/j.foodchem.2017.09.123
CrossRef Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Identificação da contaminação de 9,10-Antraquinona durante o processamento de chá preto e verde na Indonésia. Food Chemistry 327: 127092 doi: 10.1016/j.foodchem.2020.127092
CrossRef Google Scholar
[23] Zamora R, Hidalgo FJ. 2021. Formação de naftoquinonas e antraquinonas por reações de carbonil-hidroquinona/benzoquinona: uma rota potencial para a origem de 9,10-antraquinona no chá. Food Chemistry 354: 129530 doi: 10.1016/j.foodchem.2021.129530
CrossRef Google Scholar
[24] Yang M, Luo F, Zhang X, Wang X, Sun H, et al. 2022. Captação, translocação e metabolismo do antraceno em plantas de chá. Ciência do Ambiente Total 821: 152905 doi: 10.1016/j.scitotenv.2021.152905
CrossRef Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019. Influência do tabagismo e churrasqueira no conteúdo da antraquinona (ATQ) e hidrocarbonetos aromáticos policíclicos (HAP) em salsagens do tipo Frankfurter. Journal of Agricultural and Food Chemistry 67: 13998-4004 doi: 10.1021/acs.jafc.9b03316
CrossRef Google Scholar
[26] Fouillaud M, Caro Y, Venkatachalam M, Grondin I, Dufossé L. 2018. Anthraquinonas. Em compostos fenólicos em alimentos: caracterização e análise, eds. Leo Ml.Vol. 9. Boca Raton: CRC Press. pp. 130−70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muniategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, et al. 2003. Um novo método para a determinação simultânea de HAP e metais em amostras de material particulado atmosférico. Ambiente Atmosférico 37: 4171-75 doi: 10.1016/s1352-2310 (03) 00523-5
CrossRef Google Scholar
Sobre este artigo
Cite este artigo
Yu J, Zhou L, Wang X, Yang M, Sun H, et al. 2022. 9,10-Antraquinona Contaminação no processamento do chá usando carvão como fonte de calor. Planta de bebidas Pesquisa 2: 8 doi: 10.48130/bpr-2022-0008
Hora de postagem: maio-09-2022