Abstrakcyjny
9,10-anthraquinon (AQ) jest zanieczyszczeniem o potencjalnym ryzyku rakotwórczym i występuje w herbacie na całym świecie. Maksymalny limit pozostałości (MRL) AQ w herbatę ustaloną przez Unię Europejską (UE) wynosi 0,02 mg/kg. Możliwe źródła AQ w przetwarzaniu herbaty i główne stadia jej występowania zbadano na podstawie zmodyfikowanej metody analitycznej AQ i analizy chromatografii gazowej-chromatografii tandemowej (GC-MS/MS). W porównaniu z energią elektryczną jako źródłem ciepła w przetwarzaniu zielonej herbaty AQ wzrosło o 4,3 do 23,9 razy w przetwarzaniu herbaty z węglem jako źródłem ciepła, znacznie przekraczającym 0,02 mg/kg, podczas gdy poziom AQ w środowisku potroił. Ten sam trend zaobserwowano w przetwarzaniu herbaty Oolong w cieple węgla. Kroki z bezpośrednim kontaktem między liśćmi herbaty i oparami, takimi jak utrwalanie i suszenie, są uważane za główne kroki produkcji AQ w przetwarzaniu herbaty. Poziomy AQ wzrosły wraz z rosnącym czasem kontaktu, co sugeruje, że wysoki poziom zanieczyszczenia AQ w herbatę może pochodzić z oparów spowodowanych węglem i spalaniem. Analizowano cztery próbki z różnych warsztatów z energią elektryczną lub węglem, ponieważ źródła ciepła wynosiły od 50,0% - 85,0% i 5,0% - 35,0% dla wykrywania i przekraczania stawek AQ. Ponadto maksymalna zawartość AQ 0,064 mg/kg zaobserwowano w produkcie herbaty z węglem jako źródło ciepła, co wskazuje, że wysokie poziomy zanieczyszczenia AQ w produktach herbaty będą prawdopodobnie wkładane przez węgiel.
Słowa kluczowe: 9,10-antraquinon, przetwarzanie herbaty, źródło węgla, źródło zanieczyszczenia
WSTĘP
Herbata wyprodukowana z liści wiecznie zielonego krzewu Camellia sinensis (L.) O. Kuntze, jest jednym z najbardziej popularnych napojów ze względu na jego odświeżający smak i korzyści zdrowotne. W 2020 r. Produkcja herbaty wzrosła do 5 972 milionów ton metrycznych, co było podwojeniem w ciągu ostatnich 20 lat [1]. Na podstawie różnych sposobów przetwarzania istnieje sześć głównych rodzajów herbaty, w tym zielona herbata, czarna herbata, ciemna herbata, herbata oolong, biała herbata i żółta herbata [2,3]. Aby zapewnić jakość i bezpieczeństwo produktów, bardzo ważne jest monitorowanie poziomów zanieczyszczeń i zdefiniowanie pochodzenia.
Identyfikacja źródeł zanieczyszczeń, takich jak reszty pestycydów, metale ciężkie i inne zanieczyszczenia, takie jak wielopierścieniowe węglowodory aromatyczne (WWA), jest głównym krokiem do kontrolowania zanieczyszczenia. Bezpośrednie opryskiwanie syntetycznych chemikaliów na plantacjach herbaty, a także dryf powietrza spowodowany operacjami w pobliżu ogrodów herbacianych, są głównym źródłem pozostałości pestycydów w herbatę [4]. Metale ciężkie mogą gromadzić się w herbacie i prowadzić do toksyczności, które pochodzą głównie z gleby, nawozu i atmosfery [5–7]. Jeśli chodzi o inne zanieczyszczenia, które pojawiają się nieoczekiwanie w herbacie, trudno było zidentyfikować złożone procedury produkcyjnego łańcucha herbacianego, w tym plantacja, przetwarzanie, pakiet, przechowywanie i transport. WWA w herbatie pochodziły z osadzania wydechów pojazdów i spalania paliw stosowanych podczas przetwarzania liści herbaty, takich jak drewno opałowe i węgiel [8–10].
Podczas spalania węgla i drewna opałowego powstają zanieczyszczenia, takie jak tlenki węglowe [11]. W rezultacie jest to podatne na to, że pozostałości tych wyżej wymienionych zanieczyszczeń występują w przetworzonych produktach, takich jak ziarno, wędzone stado i ryby kotów, w wysokiej temperaturze, stanowiąc zagrożenie dla zdrowia ludzkiego [12,13]. PAH spowodowane spalaniem pochodzą z ulatniania się WWA zawartych w samych paliwach, w wysokiej temperaturze rozkład związków aromatycznych i reakcji złożonej między wolnymi rodnikami [14]. Temperatura spalania, czas i zawartość tlenu są ważnymi czynnikami wpływającymi na konwersję WWA. Wraz ze wzrostem temperatury zawartość WWA najpierw wzrosła, a następnie zmniejszyła się, a wartość szczytowa wystąpiła w 800 ° C; Zawartość WWA gwałtownie spadła wraz ze wzrostem czasu spalania, gdy był poniżej limitu zwanego „czasem granicznym”, wraz ze wzrostem zawartości tlenu w powietrzu spalinowym, emisje PAH znacznie zmniejszyły się, ale niepełne utlenianie spowodowałoby opah i inne pochodne [15–17].
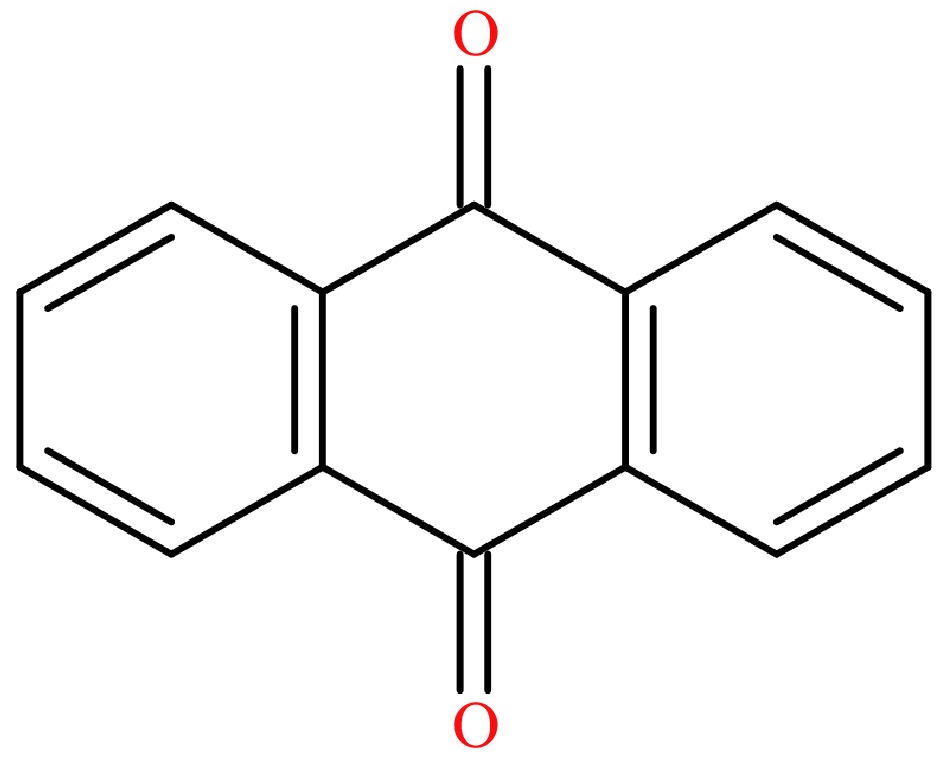
9,10-anthraquinon (AQ, CAS: 84-65-1, ryc. 1), pochodna WWA zawierająca tlen [18], składa się z trzech skondensowanych cykli. Został wymieniony jako możliwy czynnik rakotwórczy (grupa 2B) przez Międzynarodową Agencję Badań nad Rakiem w 2014 r. [19]. AQ może zatruć do kompleksu rozszczepiania topoizomerazy II i hamować hydrolizę trifosforanu adenozynowego (ATP) przez topoizomerazę DNA II, powodując uszkodzenie DNA podwójnej nici, co oznacza, że długoterminowa ekspozycja w środowisku zawierającym AQ i bezpośredni kontakt z wysokim poziomem AQ może prowadzić do uszkodzenia DNA, mutację i zwiększenie ryzyka raka [20]. Jako negatywny wpływ na zdrowie ludzkie, maksymalna limit pozostałości AQ (MRL) 0,02 mg/kg została ustalona w herbaty przez Unię Europejską. Zgodnie z naszymi wcześniejszymi badaniami złoża AQ sugerowano jako główne źródło podczas plantacji herbaty [21]. Ponadto, w oparciu o eksperymentalne konsekwencje w indonezyjskim przetwarzaniu zielonej i czarnej herbaty, oczywiste jest, że poziom AQ zmienił się znacząco, a dym z urządzeń przetwarzania został zasugerowany jako jeden z głównych powodów [22]. Jednak dokładne pochodzenie AQ w przetwarzaniu herbaty pozostało nieuchwytne, chociaż sugerowano niektóre hipotezy szlaku chemicznego AQ [23,24], co wskazuje, że niezwykle ważne jest określenie kluczowych czynników wpływających na poziom AQ w przetwarzaniu herbaty.
Ryc. 1. Wzór chemiczny AQ.
Biorąc pod uwagę badania nad tworzeniem AQ podczas spalania węgla i potencjalnego zagrożenia paliw w przetwarzaniu herbaty, przeprowadzono eksperyment porównawczy, aby wyjaśnić wpływ przetwarzania źródeł ciepła na AQ w herbatę i powietrze, analiza ilościowa na zmianach zawartości AQ na różnych etapach przetwarzania, co jest pomocne w potwierdzeniu dokładnego pochodzenia, wzorca i stopnia zanieczyszczenia AQ w przetwarzaniu herbaty.
WYNIKI
Walidacja metody
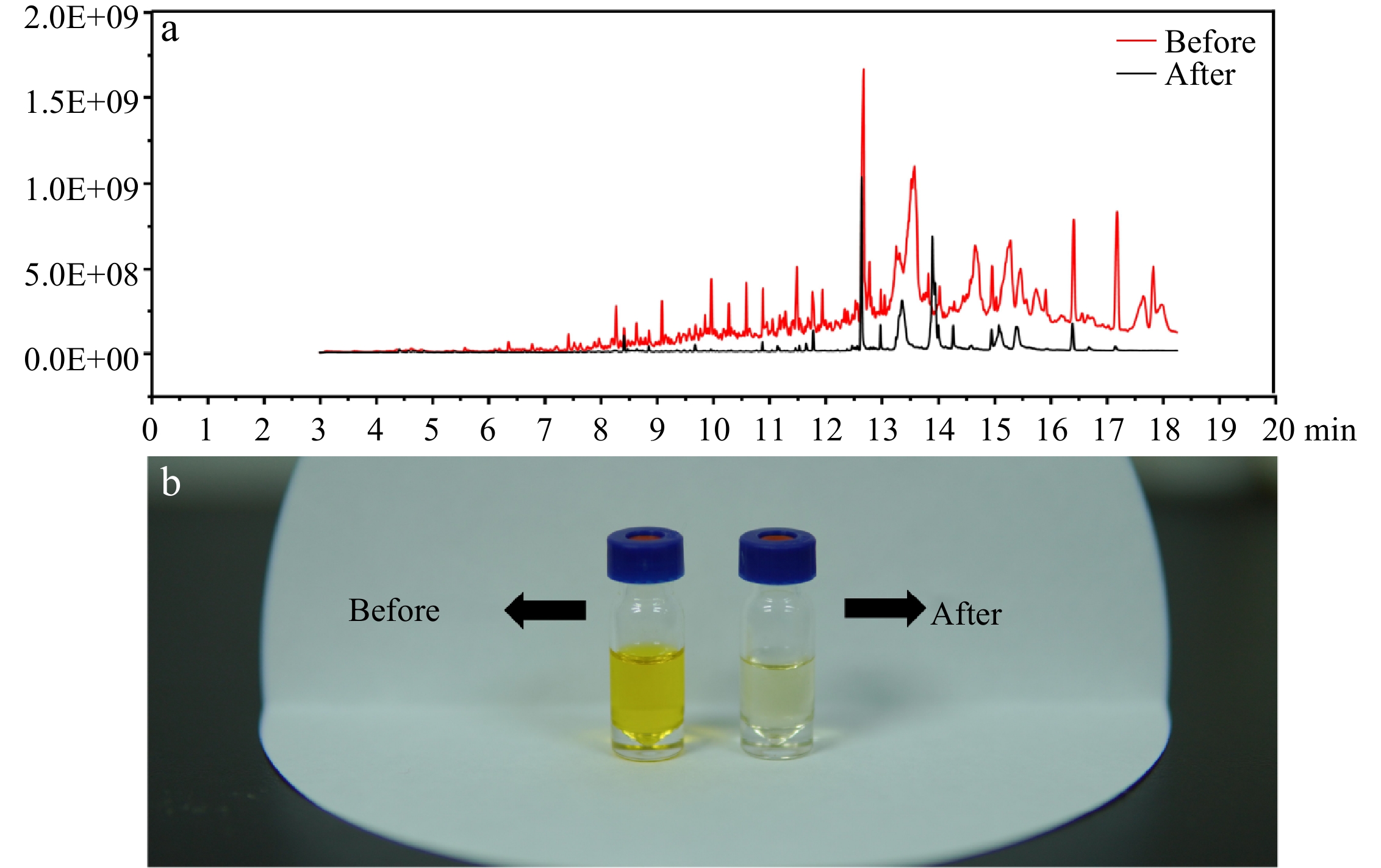
W porównaniu z naszym poprzednim badaniem [21] procedurę ekstrakcji cieczy ciecz-ciecz połączono przed wstrzyknięciem do GC-MS/MS w celu poprawy wrażliwości i utrzymania instrumentalnych stwierdzeń. Na ryc. 2B ulepszona metoda wykazała znaczną poprawę w oczyszczaniu próbki, rozpuszczalnik stał się lżejszy. Na ryc. 2A pełne spektrum skanowania (50–350 m/z) zilustrowało, że po oczyszczeniu linia podstawowa widma MS oczywiście zmniejszyła się i dostępna była mniej pików chromatograficznych, co wskazuje, że duża liczba związków zakłócających usunięto po ekstrakcji cieczy ciecz-ciecz.
Ryc. 2. (A) Pełne spektrum skanowania próbki przed i po oczyszczeniu. (b) Efekt oczyszczania ulepszonej metody.
Walidacja metody, w tym liniowość, odzyskiwanie, granica ilościowa (LOQ) i efekt matrycy (ME), pokazano w tabeli 1. Uzyskanie liniowości jest satysfakcjonujące przy współczynniku określenia (R2) wyższym niż 0,998, który wahał się od 0,005 do 0,2 mg/kg w matrycy herbacianej i octonitrylowej oraz w próbce powietrznej z zakresu 0,5 do 8 μg/m3.
Odzyskiwanie AQ oceniono przy trzech stężeniach wzbogaconych między mierzonymi a faktycznymi stężeniami w suchej herbaty (0,005, 0,02, 0,05 mg/kg), świeżych pędach herbaty (0,005, 0,01, 0,02 mg/kg) i próbce powietrza (0,5, 1,5, 3 μg/m3). Odzyskiwanie AQ w herbatę wahało się od 77,78% do 113,02% w suchej herbaty i z 96,52% do 125,69% w sesjach herbaty, z RSD% niższym niż 15%. Odzyskiwanie AQ w próbkach powietrza wahało się od 78,47% do 117,06% z RSD% poniżej 20%. Najniższe stężenie kolczastego zidentyfikowano jako LOQ, które wynosiły odpowiednio 0,005 mg/kg, 0,005 mg/kg i 0,5 μg/m3, suchą herbatę i próbki powietrza. Jak wymieniono w tabeli 1, matryca suchej herbaty i pędów herbaty nieznacznie zwiększyła odpowiedź AQ, co prowadzi do ME 109,0% i 110,9%. Jeśli chodzi o matrycę próbek powietrza, ME wynosił 196,1%.
Poziomy AQ podczas przetwarzania zielonej herbaty
W celu znalezienia wpływu różnych źródeł ciepła na herbatę i środowisko przetwarzania, partia świeżych liści podzielono na dwie konkretne grupy i przetworzono osobno w dwóch warsztatach przetwarzania w tym samym przedsiębiorstwie. Jedna grupa była dostarczana z elektrycznością, a druga z węglem.
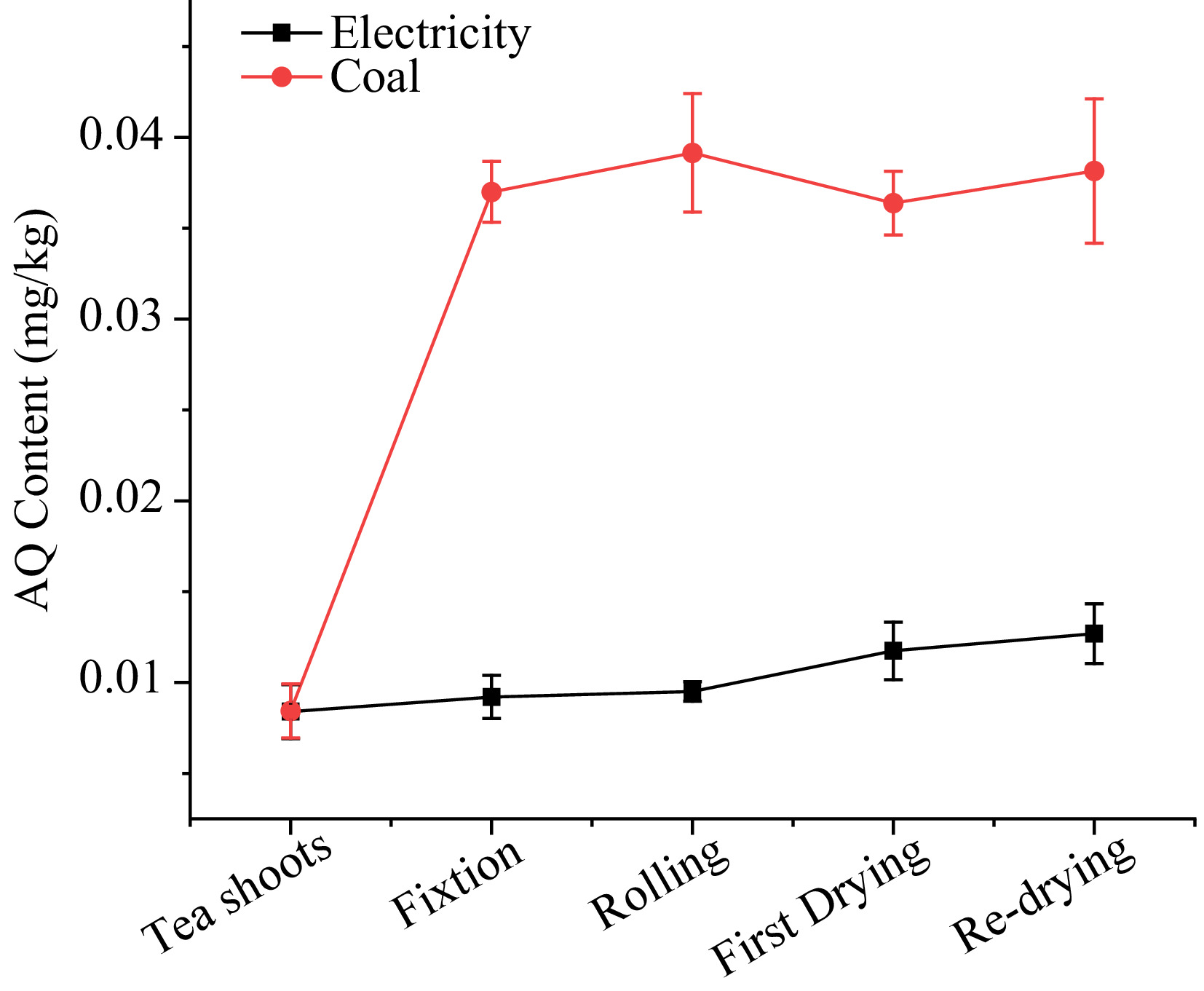
Jak pokazano na ryc. 3, poziom AQ z elektrycznością jako źródło ciepła wahał się od 0,008 do 0,013 mg/kg. Podczas procesu utrwalania spada liście herbaty spowodowane przetwarzaniem w doniczce o wysokiej temperaturze spowodowało wzrost AQ o 9,5%. Następnie poziom AQ pozostał podczas procesu toczenia pomimo utraty soku, co sugeruje, że procesy fizyczne mogą nie wpływać na poziom AQ w przetwarzaniu herbaty. Po pierwszych etapach suszenia poziom AQ nieznacznie wzrósł z 0,010 do 0,012 mg/kg, a następnie wzrastał do 0,013 mg/kg do końca ponownego wyschnięcia. PFS, który znacząco wykazywał zmienność na każdym etapie, wynosiły odpowiednio 1,10, 1,03, 1,24, 1,08 w fiksacji, toalet, pierwszym suszeniu i ponownym wysuszaniu. Wyniki PFS sugerowały, że przetwarzanie pod energią elektryczną miało niewielki wpływ na poziomy AQ w herbatę.
Rysunek 3. Poziom AQ podczas przetwarzania zielonej herbaty z elektrycznością i węglem jako źródła ciepła.
W przypadku węgla jako źródła ciepła zawartość AQ gwałtownie wzrosła podczas przetwarzania herbaty, spadając z 0,008 do 0,038 mg/kg. 338,9% AQ zostało zwiększonych w procedurze utrwalania, osiągając 0,037 mg/kg, co znacznie przekroczyło MRL 0,02 mg/kg ustalone przez Unię Europejską. Podczas etapu toczenia poziom AQ nadal wzrósł o 5,8%, mimo że jest daleko od maszyny do fiksacji. Podczas pierwszego suszenia i ponownego wyschnięcia zawartość AQ niewiele wzrosła lub nieznacznie spadła. PFS wykorzystujący węgiel jako źródło ciepła w fiksacji, toczące się pierwsze suszenie i ponowne suszenie wynosiły odpowiednio 4,39, 1,05, 0,93 i 1,05.
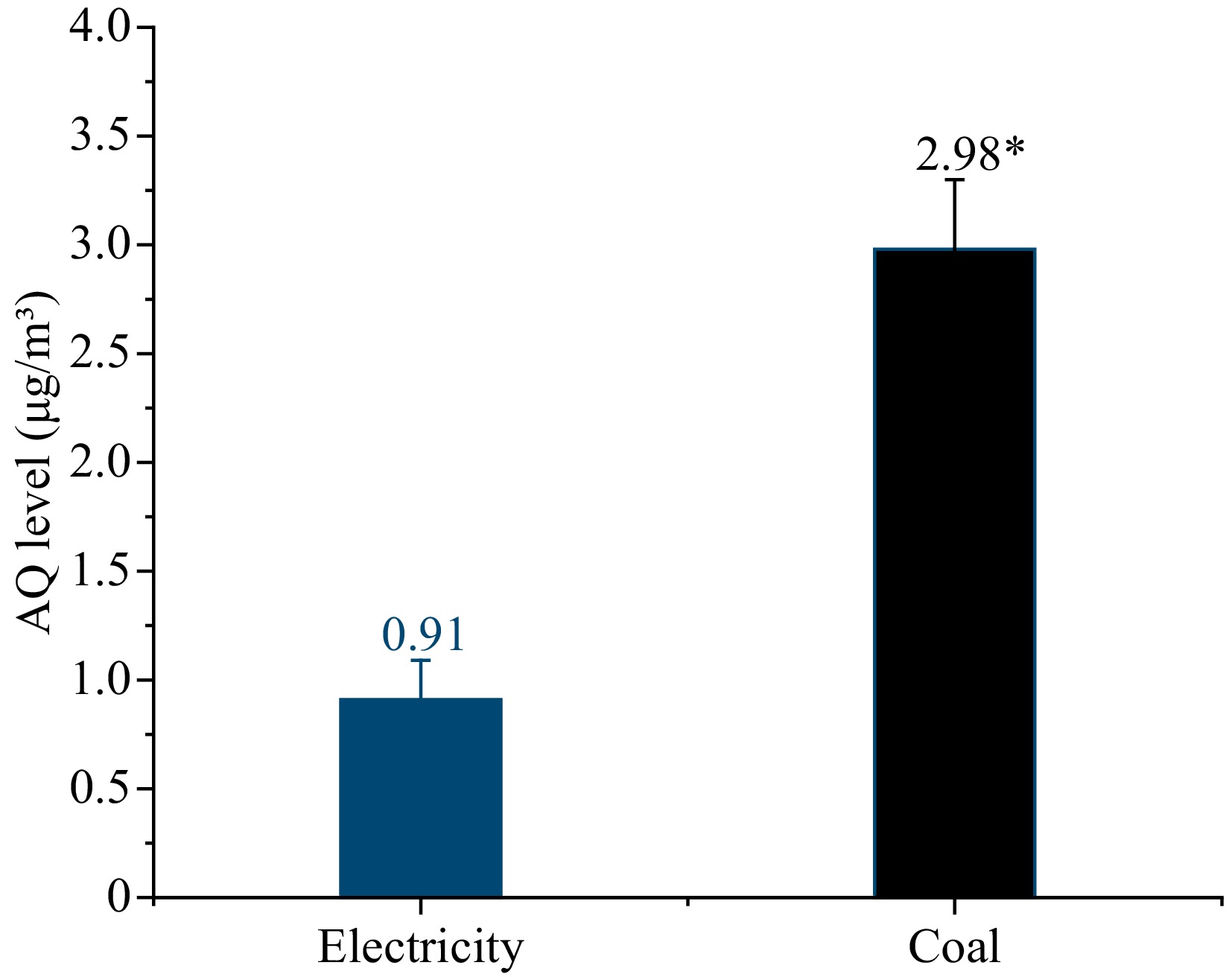
Aby dalej określić związek między spalaniem węgla a zanieczyszczeniem AQ, zawieszone materiały cząstek stałych (PMS) w powietrzu w warsztatach pod obiema źródłami ciepła zebrano do oceny powietrza, jak pokazano na ryc. 4. Poziom AQ PMS z węglem, ponieważ źródło ciepła wynosiło 2,98 μg/m3, które było ponad trzykrotnie wyższe niż w przypadku elektryczności 0,91 μg/m3.
Rycina 4. Poziomy AQ w środowisku z energią elektryczną i węglem jako źródłem ciepła. * Wskazuje znaczące różnice w poziomach AQ w próbkach (p <0,05).
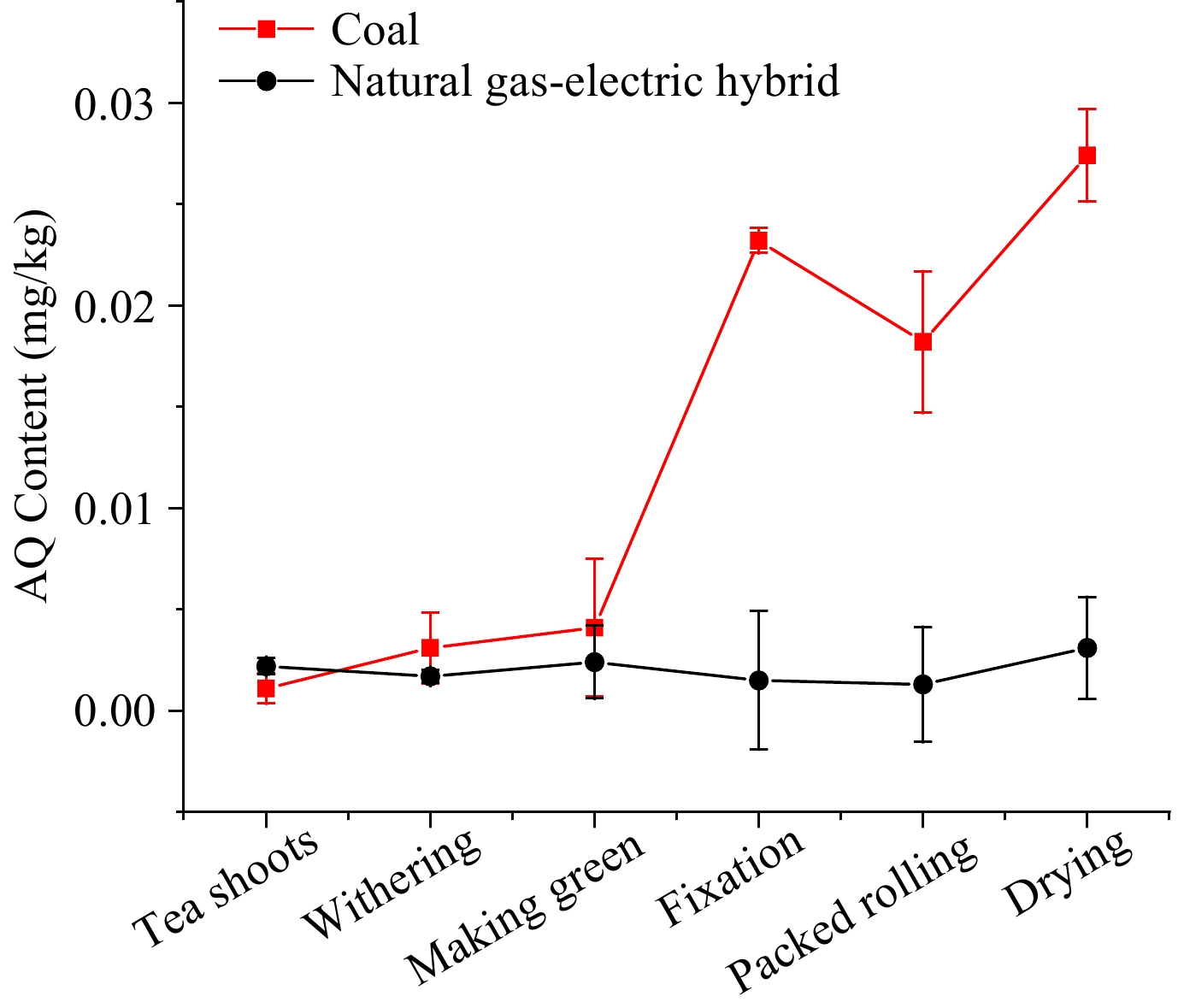
Poziomy AQ podczas herbaty Oolong Herbata Oolong, produkowana głównie w Fujian i Tajwan, jest rodzajem częściowo fermentowanej herbaty. Aby dalej określić główne etapy zwiększania poziomu AQ i wpływu różnych paliw, ta sama partia świeżych liści wykonano na herbatę Oolong z hybrydą węgla i gazu-gazowo-elektrycznego jak źródła ciepła. Poziomy AQ w przetwarzaniu herbaty Oolong przy użyciu różnych źródeł ciepła pokazano na ryc. 5. W przypadku przetwarzania herbaty Oolong z hybrydą gazu ziemnego elektrycznego, trend poziomu AQ stagnował poniżej 0,005 mg/kg, co było podobne do tej zielonej herbaty z energią elektryczną.
Rycina 5. Poziom AQ podczas przetwarzania herbaty Oolong z mieszanką gazu-elektrycznego gazu i węgla jako źródło ciepła.
Z węglem jako źródłem ciepła poziomy AQ w pierwszych dwóch krokach, miażdżenie i wytwarzanie zielonego, były zasadniczo takie same jak w przypadku mieszanki gazu ziemnego elektrycznego. Jednak kolejne procedury do momentu utrwalenia szczeliny rozszerzono stopniowo, w którym to momencie poziom AQ wzrósł z 0,004 do 0,023 mg/kg. Poziom w zapakowanym etapie toczenia zmniejszył się do 0,018 mg/kg, co może być spowodowane utratą soku herbacianego przewożącego niektóre zanieczyszczenia AQ. Po etapie toczenia poziom w etapie suszenia wzrósł do 0,027 mg/kg. W miażdżącym, tworzeniu zielonego, fiksacji, pakowanego toczenia i suszenia PFS wynosiły odpowiednio 2,81, 1,32, 5,66, 0,78 i 1,50.
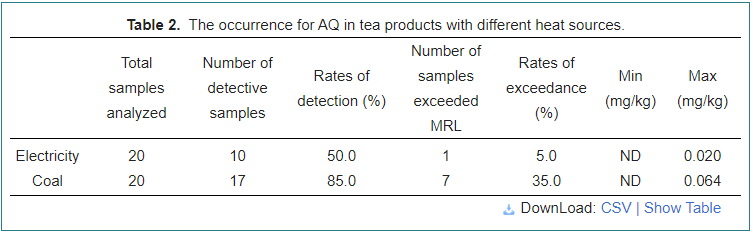
Występowanie AQ w produktach herbacianych z różnymi źródłami ciepła
Aby określić wpływ na zawartość AQ w herbatę z różnymi źródłami ciepła, przeanalizowano 40 próbek herbaty z warsztatów herbaty za pomocą energii elektrycznej lub węgla jako źródeł ciepła, jak pokazano w tabeli 2. W porównaniu z użyciem energii elektrycznej jako źródła ciepła, węgiel miał najbardziej detektywne stawki (85,0%) z maksymalnym poziomem AQ wynoszącym 0,064 mg/kg, wskazując, że było to łatwe do wywołania Contaminatu AQ przez FUMES przez kombinację węglową, a i i i i i wyprodukowania węgla i i i wyprodukowania węgla. Szybkość 35,0% zaobserwowano w próbkach węgla. Najwyraźniej energia elektryczna miała najniższy wskaźnik detektywa i współczynnik wynoszący odpowiednio 56,4% i 7,7%, przy maksymalnej zawartości 0,020 mg/kg.
DYSKUSJA
W oparciu o PFS podczas przetwarzania z dwoma rodzajami źródeł ciepła było jasne, że utrwalanie było głównym krokiem, które doprowadziło do wzrostu poziomów AQ w produkcji herbaty z węglem i przetwarzaniem pod energią elektryczną, miała niewielki wpływ na zawartość AQ w herbatę. Podczas przetwarzania zielonej herbaty spalanie węgla wytwarzało wiele oparów w procesie fiksacji w porównaniu z elektrycznym procesem ogrzewania, co wskazuje, że być może opary były głównym źródłem zanieczyszczeń AQ z kontaktu z pędami herbaty w przetwarzaniu herbaty, podobnie jak w procesie ekspozycji w wędzonych próbkach grilla [25]. Nieco wzrost zawartości AQ na etapie toczenia sugeruje, że opary spowodowane spalaniem węgla wpłynęły nie tylko na poziom AQ na etapie utrwalania, ale także w środowisku przetwarzania z powodu osadzania atmosferycznego. Węglki były również używane jako źródło ciepła w pierwszym suszeniu i ponownym wysuszeniu, ale w tych dwóch etapach zawartość AQ nieznacznie wzrosła lub nieznacznie spadła. Można to wytłumaczyć faktem, że zamknięta suszarka na gorąco trzymała herbatę z dala od oparów spowodowanych spalaniem węgla [26]. Aby określić źródło zanieczyszczeń, przeanalizowano poziomy AQ w atmosferze, co spowodowało znaczną lukę między dwoma warsztatami. Głównym powodem tego jest to, że węgiel użyty w fiksacji, pierwszego suszenia i ponownego wyschnięcia stadiów generowałby AQ podczas niepełnego spalania. Te AQ zostały następnie zaadsorbowane w małych cząstkach stałych po spalaniu węgla i rozproszono w powietrzu, podnosząc poziomy zanieczyszczenia AQ w środowisku warsztatowym [15]. Z czasem, ze względu na dużą powierzchnię właściwą i zdolność adsorpcji herbaty, cząstki te osiadły na powierzchni liści herbaty, co spowodowało wzrost AQ w produkcji. Dlatego uważano, że spalanie węgla jest główną drogą prowadzącą do nadmiernego zanieczyszczenia AQ w przetwarzaniu herbaty, przy czym opary są źródłem zanieczyszczenia.
Jeśli chodzi o przetwarzanie herbaty Oolong, AQ zwiększono w przetwarzaniu obu źródeł ciepła, ale różnica między dwoma źródłami ciepła była znacząca. Wyniki sugerują również, że węgiel jako źródło ciepła odegrał ważną rolę w zwiększaniu poziomu AQ, a fiksacja uznano za główny krok do zwiększenia zanieczyszczenia AQ w przetwarzaniu herbaty Oolong w oparciu o PFS. Podczas przetwarzania herbaty Oolong z hybrydą gazu ziemnego jako źródła ciepła trend poziomu AQ stagnował poniżej 0,005 mg/kg, co było podobne do zielonej herbaty z energią elektryczną, co sugeruje, że czysta energia, taka jak energia elektryczna i gaz ziemny, może zmniejszyć ryzyko wytwarzania puszek AQ z przetwarzania.
Jeśli chodzi o testy pobierania próbek, wyniki wykazały, że sytuacja zanieczyszczenia AQ była gorsza podczas używania węgla jako źródła ciepła, a nie energii elektrycznej, co może wynikać z oparów z spalania węgla, które kontaktują się z liśćmi herbaty i utrzymywanie się wokół miejsca pracy. Jednak, choć było oczywiste, że energia elektryczna była najczystszym źródłem ciepła podczas przetwarzania herbaty, nadal było zanieczyszczenie AQ w produktach herbacianych przy użyciu energii elektrycznej jako źródła ciepła. Sytuacja wydaje się nieco podobna do wcześniej opublikowanych prac, w których reakcja 2-alkenałów z hydrochinonami i benzochinonami została zasugerowana jako potencjalny szlak chemiczny [23], przyczyny tego zostaną zbadane w przyszłych badaniach.
Wnioski
W tej pracy możliwe źródła zanieczyszczenia AQ w zielonej i Oolong Tea zostały potwierdzone przez eksperymenty porównawcze oparte na ulepszonych metod analitycznych GC-MS/MS. Nasze ustalenia bezpośrednio potwierdziły, że główne źródło zanieczyszczeń wysokich poziomów AQ było oparte na spalaniu, które nie tylko wpłynęło na etapy przetwarzania, ale także wpłynęło na środowiska warsztatowe. W przeciwieństwie do stadiów toczących się i miażdżenia, w których zmiany poziomu AQ były niepozorne, etapy z bezpośrednim zaangażowaniem węgla i drewna opałowego, takiego jak utrwalanie, są głównym procesem, w którym wzrosło zanieczyszczenie AQ ze względu na ilość kontaktu między herbatą a oparami w tych etapach. Dlatego zalecane były czyste paliwa, takie jak gaz ziemny i energia elektryczna jako źródło ciepła w przetwarzaniu herbaty. Ponadto wyniki eksperymentalne wykazały również, że przy braku opasek generowanych przez spalanie wciąż były inne czynniki przyczyniające się do śledzenia AQ podczas przetwarzania herbaty, podczas gdy niewielkie ilości AQ zaobserwowano również w warsztatach z czystymi paliwami, które należy dalej zbadać w przyszłych badaniach.
Materiały i metody
Odczynniki, chemikalia i materiały
Standard antrachinonu (99,0%) został zakupiony od Dr. Ehrenstorfer GmbH Company (Augsburg, Niemcy). D8-anthraquinon wewnętrzny standard (98,6%) zakupiono od C/D/N izotopów (Quebec, Kanada). Bezwodny siarczan sodu (NA2SO4) i siarczan magnezu (MGSO4) (Szanghaj, Chiny). Florisil został dostarczony przez Wenzhou Organic Chemical Company (Wenzhou, Chiny). Papier światłowodowy Mircro-szklany (90 mm) został zakupiony od Ahlstrom-Munksjö Company (Helsinki, Finlandia).
Przygotowanie próbki
Próbki zielonej herbaty przetwarzano z fiksacją, toczeniem, pierwszym suszeniem i ponownym wyschnięciem (przy użyciu zamkniętego sprzętu), podczas gdy próbki herbaty Oolong były przetwarzane z miażdżeniem, wytwarzając zielone (bujane i stojące na przemian ze świeżych liści), fiksacja, pakowanie i suszenie. Próbki z każdego kroku zebrano trzy razy w 100 g po dokładnym mieszaniu. Wszystkie próbki przechowywano w -20 ° C w celu dalszej analizy.
Próbki powietrza pobrano za pomocą papieru szklanego (90 mm) przy użyciu próbników o średniej objętości (PTS-100, Qingdao Laoshan Electronic Instrument Company, Qingdao, Chiny) [27], działającym po 100 l/min przez 4 godziny.
Fortified samples were spiked with AQ at 0.005 mg/kg, 0.010 mg/kg, 0.020 mg/kg for fresh tea shoots, at 0.005 mg/kg, 0.020 mg/kg, 0.050 mg/kg for dry tea and at 0.012 mg/kg (0.5 µg/m3 for air sample), 0.036 mg/kg (1.5 µg/m3 for Smaple powietrza), odpowiednio 0,072 mg/kg (3,0 µg/m3 dla próbki powietrza) dla bibuły filtracyjnej szklanej. Po dokładnym wstrząsie wszystkie próbki pozostawiono na 12 godzin, a następnie etapy ekstrakcji i czyszczenia.
Zawartość wilgoci uzyskano przez pobranie 20 g próbki po zmieszaniu każdego kroku, ogrzewając się w temperaturze 105 ° C przez 1 godzinę, a następnie ważenie i powtarzanie trzykrotnie oraz przyjmując średnią wartość i podzielenie jej przez wagę przed podgrzaniem.
Ekstrakcja i czyszczenie próbki
Próbka herbaty: Ekstrakcja i oczyszczanie AQ z próbek herbaty przeprowadzono na podstawie opublikowanej metody Wang i in. z kilkoma adaptacjami [21]. W skrócie, 1,5 g próbek herbaty najpierw zmieszano z 30 μl D8-AQ (2 mg/kg) i pozostawiono do stania przez 30 minut, a następnie dobrze zmieszano z 1,5 ml wody dejonizowanej i pozostawiono do 30 minut. 15 ml 20% aceton w n-heksanu dodano do próbek herbaty i sonikowano przez 15 minut. Następnie próbki wirowano 1,0 g mgso4 przez 30 s i wirowano przez 5 minut, przy 11 000 obr / min. Po przeniesieniu do 100 ml kolb w kształcie gruszki 10 ml górnej fazy organicznej odparowano do prawie suchości pod próżnią w 37 ° C. 5 ml 2,5% acetonu w N-heksanie ponownie wyciągnęło ekstrakt w kolbach w kształcie gruszki w celu oczyszczenia. Szklana kolumna (10 cm × 0,8 cm) składała się z dołu do górnej szklanej wełny i 2G Florisil, która była między dwiema warstwami 2 cm Na2SO4. Następnie 5 ml 2,5% acetonu w N-heksanie wstępnie przedłużyło kolumnę. Po załadowaniu roztworu redisolowanego AQ eluowano trzykrotnie 5 ml, 10 ml, 10 ml 2,5% acetonu w N-heksanu. Połączone eluaty przeniesiono do kolb w kształcie gruszki i odparowano do prawie suchości pod próżnią w 37 ° C. Suszoną resztę odtworzono następnie 1 ml 2,5% acetonu w heksanie, a następnie filtracja przez filtr wielkości porów 0,22 µm. Następnie odtworzony roztwór zmieszano z acetonitrylem przy stosunku objętości 1: 1. Po kroku wstrząsania podnatant zastosowano do analizy GC-MS/MS.
Próbka powietrza: połowa papieru światłowodowego, kapitana 18 μl D8-AQ (2 mg/kg), zanurzono w 15 ml 20% acetonu w n-heksanie, a następnie sonikowano przez 15 minut. Fazę organiczną oddzielono przez wirowanie przy 11 000 rpm przez 5 minut, a całą górną warstwę usunięto w kolbie w kształcie gruszki. Wszystkie fazy organiczne odparowano do prawie suchości pod próżnią w 37 ° C. 5 ml 2,5% acetonu w heksanie zbudowało ekstrakty do oczyszczania w taki sam sposób, jak w próbkach herbaty.
Analiza GC-MS/MS
Chromatograf gazowy Varian 450 wyposażony w detektor masy tandemowej Varian 300 (Varian, Walnut Creek, Kalifornia, USA) zastosowano do przeprowadzenia analizy AQ za pomocą oprogramowania MS Workstation w wersji 6.9.3. Współczynnik Varian Four Capilary VF-5M (30 m × 0,25 mm × 0,25 μm) zastosowano do separacji chromatograficznej. Gaz nośnika, hel (> 99,999%), ustawiono przy stałym natężeniu przepływu 1,0 ml/min z gazem zderzeniowym argonu (> 99,999%). Temperatura piekarnika rozpoczęła się od 80 ° C i utrzymywała się przez 1 min; Zwiększony przy 15 ° C/min do 240 ° C, a następnie osiągnął 260 ° C w 20 ° C/min i utrzymywał 5 minut. Temperatura źródła jonów wynosiła 210 ° C, a także temperatura linii transferowej 280 ° C. Objętość wstrzyknięcia wynosiła 1,0 μl. Warunki MRM pokazano w tabeli 3.
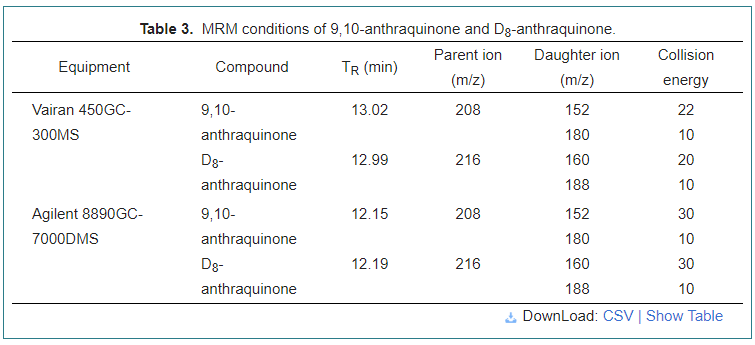
Agilent 8890 Chromatograf gazowy wyposażony w potrójny spektrometr masowy Agilent 7000D (Agilent, Stevens Creek, Kalifornia, USA) zastosowano do analizy efektu oczyszczania za pomocą oprogramowania MasShunter wersja 10.1. Do separacji chromatograficznej zastosowano kolumnę Agilent J&W HP-5MS GC (30 m × 0,25 mm × 0,25 μm). Gaz nośnika, hel (> 99,999%), ustawiono przy stałym natężeniu przepływu 2,25 ml/min z gazem kolizyjnym azotu (> 99,999%). Temperaturę źródła jonowego EI regulowano w 280 ° C, tak samo jak temperatura linii transferowej. Temperatura piekarnika rozpoczęła się od 80 ° C i utrzymywano przez 5 minut; podniesiony o 15 ° C/min do 240 ° C, a następnie osiągnął 280 ° C w 25 ° C/min i utrzymywał przez 5 minut. Warunki MRM pokazano w tabeli 3.
Analiza statystyczna
Zawartość AQ w świeżych liściach została skorygowana w celu suchej zawartości materii poprzez dzielenie przez zawartość wilgoci w celu porównania i analizy poziomów AQ podczas przetwarzania.
Zmiany AQ w próbkach herbaty oceniono za pomocą Microsoft Excel Software i IBM SPSS Statistics 20.
Współczynnik przetwarzania zastosowano do opisania zmian w AQ podczas przetwarzania herbaty. PF = RL/RF, gdzie RF jest poziomem AQ przed etapem przetwarzania i RL to poziom AQ po etapie przetwarzania. PF wskazuje spadek (PF <1) lub wzrost (PF> 1) w resztku AQ podczas określonego etapu przetwarzania.
Me wskazuje spadek (Me <1) lub wzrost (Me> 1) w odpowiedzi na instrumenty analityczne, które opiera się na stosunku zboczy kalibracji w macierzy i rozpuszczalnika w następujący sposób:
ME = (Slopematrix/Slopsolvent - 1) × 100%
Tam, gdzie Slopematrix jest nachyleniem krzywej kalibracyjnej w dopasowanym do matrycy rozpuszczalniku, zbocz jest nachyleniem krzywej kalibracji w rozpuszczalniku.
PODZIĘKOWANIE
Prace te były wspierane przez główny projekt nauki i technologii w prowincji Zhejiang (2015C12001) i National Science Foundation of China (42007354).
Konflikt interesów
Autorzy oświadczają, że nie mają konfliktu interesów.
Prawa i uprawnienia
Prawa autorskie: © 2022 autorstwa autora. Ekskluzywny licencjobiorca Maksymalna prasa akademicka, Fayetteville, GA. Ten artykuł to artykuł otwartego dostępu rozproszony na podstawie licencji Creative Commons Actiftion (CC do 4.0), odwiedź https://creativecommons.org/licenses/by/4.0/.
Odniesienia
[1] ITC. 2021. Coroczny biuletyn statystyki 2021. https://inttea.com/publication/
[2] Hicks A. 2001. Przegląd globalnej produkcji herbaty i wpływ na przemysł w azjatyckiej sytuacji gospodarczej. AU Journal of Technology 5
Google Scholar
[3] Katsuno T, Kasuga H, Kusano Y, Yaguchi Y, Tomomura M, i in. 2014. Charakterystyka związków zapachowych i ich tworzenie biochemiczne w zielonej herbaty z procesem przechowywania niskiej temperatury. Chemia żywności 148: 388–95 doi: 10.1016/j.foodchem.2013.10.069
Crossref Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Tri-Dimesion Zanieczyszczenie w ekosystemie herbaty i jego kontroli. Scientia Agricultura sinica 40: 948–58
Google Scholar
[5] He H, Shi L, Yang G, You M, Vasseur L. 2020. Ocena ryzyka ekologicznego metali ciężkich gleby i pozostałości pestycydów na plantacjach herbaty. Rolnictwo 10:47 DOI: 10.3390/Agriculture10020047
Crossref Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J, i in. 2005. Zanieczyszczenie ołowiu w liściach herbaty i czynnikach nieedafowych wpływających na to. Chemosfera 61: 726–32 doi: 10.1016/j.chemosphere.2005.03.053
Crossref Google Scholar
[7] Owuor PO, Obaga SO, Othieno CO. 1990. Wpływ wysokości na skład chemiczny czarnej herbaty. Journal of the Science of Food and Agriculture 50: 9–17 doi: 10.1002/jsfa.2740500103
Crossref Google Scholar
[8] Garcia Londoño VA, Reynoso M, Resnik S. 2014. Policykliczne aromatyczne węglowodory (PAH) w Yerba Mate (Ilex paraguariensis) z rynku argentyńskiego. Dodatki i zanieczyszczenia żywności: Część B 7: 247–53 doi: 10.1080/19393210.2014.919963
Crossref Google Scholar
[9] Ishizaki A, Saito K, Hanioka N, Narimatsu S, Kataoka H. 2010. Oznaczanie wielopierścieniowych węglowodorów aromatycznych w próbkach żywności przez zautomatyzowane mikroekstrakcja w fazie stałej w sieci w sposób stały. Journal of Chromatography A 1217: 5555-63 doi: 10.1016/j.chroma.2010.06.068
Crossref Google Scholar
[10] Phan Thi La, Ngoc NT, Quynh NT, Thanh NV, Kim TT, i in. 2020. Policykliczne węglowodory aromatyczne (WWA) w liściach suchych herbaty i infuzji herbaty w Wietnamie: poziomy zanieczyszczenia i ocena ryzyka dietetycznego. Geochemia środowiskowa i zdrowie 42: 2853–63 doi: 10.1007/s10653-020-00524-3
Crossref Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. Występowanie 16 WWA EPA w żywności - recenzja. Policykliczne związki aromatyczne 35: 248–84 doi: 10.1080/10406638.2014.918550
Crossref Google Scholar
[12] Omodara NB, Olabemiwo OM, Adedosu TA. 2019. Porównanie WWA utworzone w drewnie opałowym i wędzonym węglu drzewnym i rybom kotom. American Journal of Food Science and Technology 7: 86–93 DOI: 10.12691/AJFST-7-3-3
Crossref Google Scholar
[13] Zou Ly, Zhang W, Atkiston S. 2003. Charakterystyka wielopierpliwych emisji węglowodorów aromatycznych po spalaniu różnych gatunków drewna opałowego w Australii. Zanieczyszczenie środowiska 124: 283–89 doi: 10.1016/s0269-7491 (02) 00460-8
Crossref Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL i in. 2000. Aktywność benzo [A] pirenu i jego hydroksylowanych metabolitów w teście genu reportera receptora estrogenowego-α. Nauki toksykologiczne 55: 320–26 DOI: 10.1093/Toxsci/55.2.320
Crossref Google Scholar
[15] Han Y, Chen Y, Ahmad S, Feng Y, Zhang F, i in. 2018. Wysokie pomiary z rozdzielczością czasu i wielkości PM i składu chemicznego z spalania węgla: implikacje dla procesu tworzenia EC. Nauka o środowisku i technologia 52: 6676–85 doi: 10.1021/acs.est.7b05786
Crossref Google Scholar
[16] Khiadani (Hajian) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M, i in. 2013. Określenie wielopierścieniowych stężenia węglowodorów aromatycznych u ośmiu marek czarnej herbaty, które są używane bardziej w Iranie. International Journal of Environmental Health Engineering 2:40 DOI: 10.4103/2277-9183.122427
Crossref Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J, Andrews G, Jones JM i in. 2007. Emisja natlenionych gatunków z spalania drewna sosnowego i jego związek z tworzeniem sadzy. Proces bezpieczeństwa i ochrony środowiska 85: 430–40 DOI: 10.1205/psep07020
Crossref Google Scholar
[18] Shen G, Tao S, Wang W, Yang Y, Ding J, i in. 2011. Emisja natlenionych wielopierścieniowych węglowodorów aromatycznych z spalania paliwa stałe. Nauka o środowisku i technologia 45: 3459–65 doi: 10.1021/es104364t
Crossref Google Scholar
[19] Międzynarodowa Agencja Badań nad Rakiem (IARC), Światowa Organizacja Zdrowia. 2014. Wydech oleju napędowego i benzynowego i niektóre nitroareny. Międzynarodowa Agencja Badań nad monografiami raka na temat oceny ryzyka rakotwórczego dla ludzi. Raport. 105: 9
[20] De Oliveira Galvão MF, de Oliveira Alves N, Ferreira PA, Caumo S, de Castro Vasconcellos P, i in. 2018. Cząstki spalania biomasy w brazylijskim regionie Amazonii: mutagenne działanie nitro i tlen-PAH oraz ocena zagrożeń dla zdrowia. Zanieczyszczenie środowiska 233: 960–70 doi: 10.1016/j.envpol.2017.09.068
Crossref Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H, i in. 2018. Depozyt 9,10-antraquinon w plantacji herbaty może być jednym z powodów zanieczyszczenia herbaty. Chemia żywności 244: 254–59 doi: 10.1016/j.foodchem.2017.09.123
Crossref Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Identyfikacja zanieczyszczenia 9,10-anthraquinon podczas przetwarzania czarnej i zielonej herbaty w Indonezji. Chemia żywności 327: 127092 doi: 10.1016/j.foodchem.2020.127092
Crossref Google Scholar
[23] Zamora R, Hidalgo FJ. 2021. Tworzenie naftochinonów i antrachinonów za pomocą reakcji karbonylo-hydrochinonu/benzochinonu: potencjalna droga pochodzenia 9,10-anthraquinone w herbatę. Chemia żywności 354: 129530 doi: 10.1016/j.foodchem.2021.129530
Crossref Google Scholar
[24] Yang M, Luo F, Zhang X, Wang X, Sun H, i in. 2022. Wychwyt, translokacja i metabolizm antracenu w roślinach herbacianych. Nauka o całkowitym środowisku 821: 152905 doi: 10.1016/j.scitotenv.2021.152905
Crossref Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019. Wpływ palenia i grillowania na zawartość antrachinonu (ATQ) i wielopierścieniowych węglowodorów aromatycznych (PAH) w kiełbasach typu frankfurtera. Journal of Agricultural and Food Chemistry 67: 13998-4004 doi: 10.1021/acs.jafc.9b03316
Crossref Google Scholar
[26] Fouilud M, Caro Y, Venkatachalam M, Grondin I, Dufossé L. 2018. Anthraquinones. W związkach fenolowych w żywności: charakterystyka i analiza, red. Leo Ml.vol. 9. Boca Raton: CRC Press. str. 130–70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, i in. 2003. Nowa metoda jednoczesnego oznaczania WWA i metali w próbkach cząstek stałych atmosferycznych. Środowisko atmosferyczne 37: 4171–75 DOI: 10.1016/S1352-2310 (03) 00523-5
Crossref Google Scholar
O tym artykule
Cytować ten artykuł
Yu J, Zhou L, Wang X, Yang M, Sun H, i in. 2022. 9,10-antraquinon zanieczyszczenie w przetwarzaniu herbaty za pomocą węgla jako źródła ciepła. Badania roślin napojów 2: 8 DOI: 10.48130/BPR-2022-0008
Czas po: 09-2022