Abstrak
9,10-anthraquinone (AQ) adalah bahan pencemar dengan risiko karsinogenik yang berpotensi dan berlaku di teh di seluruh dunia. Had residu maksimum (MRL) AQ dalam teh yang ditetapkan oleh Kesatuan Eropah (EU) ialah 0.02 mg/kg. Sumber-sumber AQ yang mungkin dalam pemprosesan teh dan peringkat utama kejadiannya disiasat berdasarkan kaedah analisis AQ yang diubahsuai dan analisis spektrometri massa kromatografi gas (GC-MS/MS). Berbanding dengan elektrik sebagai sumber haba dalam pemprosesan teh hijau, AQ meningkat sebanyak 4.3 hingga 23.9 kali dalam pemprosesan teh dengan arang batu sebagai sumber haba, jauh melebihi 0.02 mg/kg, manakala tahap AQ di alam sekitar tiga kali ganda. Trend yang sama diperhatikan dalam pemprosesan teh oolong di bawah haba arang batu. Langkah -langkah dengan hubungan langsung antara daun teh dan asap, seperti penetapan dan pengeringan, dianggap sebagai langkah utama pengeluaran AQ dalam pemprosesan teh. Tahap AQ meningkat dengan masa hubungan yang semakin meningkat, menunjukkan bahawa paras pencemar AQ yang tinggi dalam teh boleh diperolehi daripada asap yang disebabkan oleh arang batu dan pembakaran. Empat puluh sampel dari bengkel yang berbeza dengan elektrik atau arang batu sebagai sumber haba dianalisis, adalah dari 50.0% -85.0% dan 5.0% -35.0% untuk pengesanan dan melebihi kadar aq. Di samping itu, kandungan AQ maksimum 0.064 mg/kg diperhatikan dalam produk teh dengan arang batu sebagai sumber haba, menunjukkan bahawa tahap pencemaran AQ yang tinggi dalam produk teh mungkin disumbangkan oleh arang batu.
Kata kunci: 9,10-anthraquinone, pemprosesan teh, arang batu, sumber pencemaran
Pengenalan
Teh yang dihasilkan dari daun semak malar hijau Camellia sinensis (L.) O. Kuntze, adalah salah satu minuman yang paling popular di seluruh dunia kerana rasa yang menyegarkan dan manfaat kesihatannya. Pada tahun 2020 di seluruh dunia, pengeluaran teh telah meningkat kepada 5,972 juta tan metrik, yang merupakan dua kali ganda dalam 20 tahun yang lalu [1]. Berdasarkan cara pemprosesan yang berbeza, terdapat enam jenis teh utama, termasuk teh hijau, teh hitam, teh gelap, teh oolong, teh putih dan teh kuning [2,3]. Untuk memastikan kualiti dan keselamatan produk, sangat penting untuk memantau tahap bahan pencemar dan menentukan asalnya.
Mengenal pasti sumber bahan cemar, seperti residu racun perosak, logam berat dan bahan pencemar lain seperti hidrokarbon aromatik polycyclic (PAHs), adalah langkah utama untuk mengawal pencemaran. Penyemburan langsung bahan kimia sintetik di ladang teh, serta hanyutan udara yang disebabkan oleh operasi berhampiran taman teh, merupakan sumber utama residu racun perosak dalam teh [4]. Logam berat boleh berkumpul dalam teh dan membawa kepada ketoksikan, yang kebanyakannya berasal dari tanah, baja dan atmosfera [5-7]. Bagi pencemaran lain yang kelihatan tidak disangka -sangka dalam teh, agak sukar untuk dikenal pasti kerana prosedur kompleks rantaian teh pengeluaran termasuk ladang, pemprosesan, pakej, penyimpanan dan pengangkutan. PAH dalam teh datang dari pemendapan ekzos kenderaan dan pembakaran bahan api yang digunakan semasa pemprosesan daun teh, seperti kayu bakar dan arang batu [8-10].
Semasa pembakaran arang batu dan kayu api, bahan pencemar seperti oksida karbon terbentuk [11]. Akibatnya, ia terdedah kepada sisa-sisa bahan pencemar yang disebutkan di atas ini berlaku dalam produk yang diproses, seperti bijirin, stok asap dan ikan kucing, pada suhu tinggi, menimbulkan ancaman kepada kesihatan manusia [12,13]. PAH yang disebabkan oleh pembakaran diperolehi daripada volatilisasi PAH yang terkandung dalam bahan api itu sendiri, penguraian suhu tinggi sebatian aromatik dan tindak balas kompaun antara radikal bebas [14]. Suhu pembakaran, masa, dan kandungan oksigen adalah faktor penting yang mempengaruhi penukaran PAH. Dengan peningkatan suhu, kandungan PAHs mula -mula meningkat dan kemudian menurun, dan nilai puncak berlaku pada 800 ° C; Kandungan PAHS menurun dengan ketara untuk mengesan dengan peningkatan masa pembakaran apabila ia berada di bawah had yang disebut 'masa sempadan', dengan peningkatan kandungan oksigen dalam udara pembakaran, pelepasan PAHS dikurangkan dengan ketara, tetapi pengoksidaan yang tidak lengkap akan menghasilkan opAH dan derivatif lain [15-17].
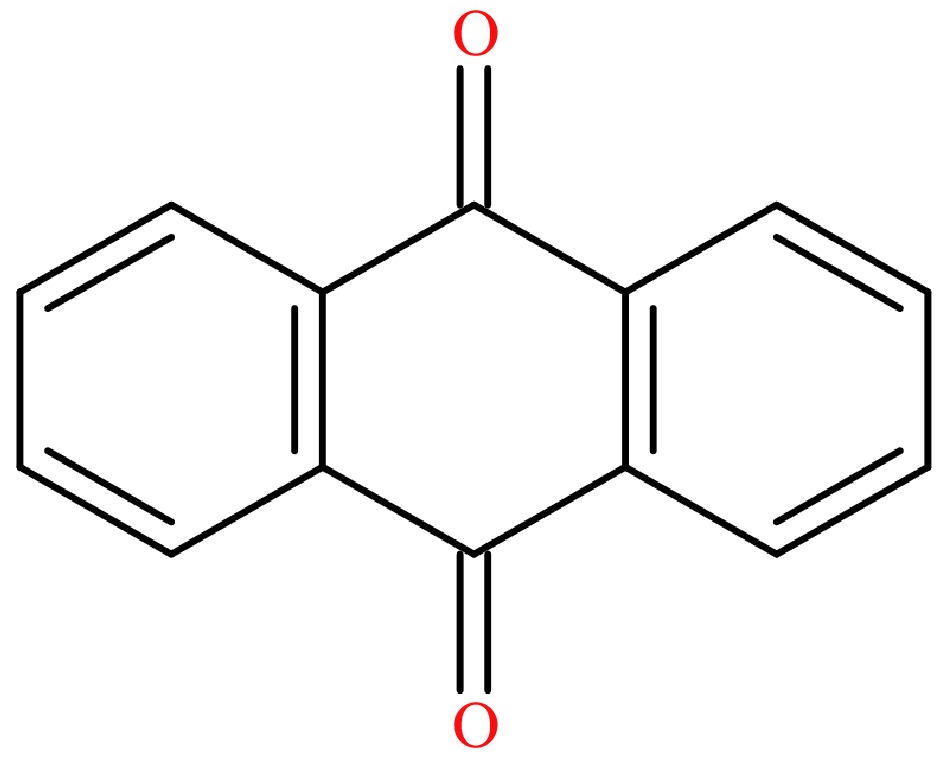
9,10-anthraquinone (AQ, CAS: 84-65-1, Rajah 1), derivatif yang mengandungi oksigen PAHs [18], terdiri daripada tiga kitaran pekat. Ia disenaraikan sebagai karsinogen yang mungkin (Kumpulan 2B) oleh Agensi Antarabangsa untuk Penyelidikan Kanser pada tahun 2014 [19]. AQ boleh racun ke kompleks pembekuan topoisomerase II dan menghalang hidrolisis adenosine triphosphate (ATP) oleh topoisomerase DNA II, menyebabkan pemecahan dua helai DNA. Sebagai kesan negatif terhadap kesihatan manusia, had residu maksimum AQ (MRL) 0.02 mg/kg ditetapkan dalam teh oleh Kesatuan Eropah. Menurut kajian terdahulu kami, deposit AQ dicadangkan sebagai sumber utama semasa ladang teh [21]. Juga, berdasarkan akibat eksperimen dalam pemprosesan teh hijau dan hitam Indonesia, jelas bahawa tahap AQ berubah dengan ketara dan asap dari peralatan pemprosesan dicadangkan sebagai salah satu sebab utama [22]. Walau bagaimanapun, asal -usul AQ yang tepat dalam pemprosesan teh kekal sukar difahami, walaupun beberapa hipotesis laluan kimia AQ dicadangkan [23,24], menunjukkan bahawa sangat penting untuk menentukan faktor -faktor penting yang mempengaruhi tahap AQ dalam pemprosesan teh.
Rajah 1. Formula kimia aq.
Memandangkan penyelidikan mengenai pembentukan AQ semasa pembakaran arang batu dan potensi ancaman bahan api dalam pemprosesan teh, eksperimen perbandingan dilakukan untuk menjelaskan kesan pemprosesan sumber haba pada AQ dalam teh dan udara, analisis kuantitatif pada perubahan kandungan AQ pada langkah -langkah pemprosesan yang berbeza, yang membantu mengesahkan asal -usul tepat, corak kejadian dan tahap pencemaran AQ dalam pemprosesan TEA.
Hasilnya
Pengesahan kaedah
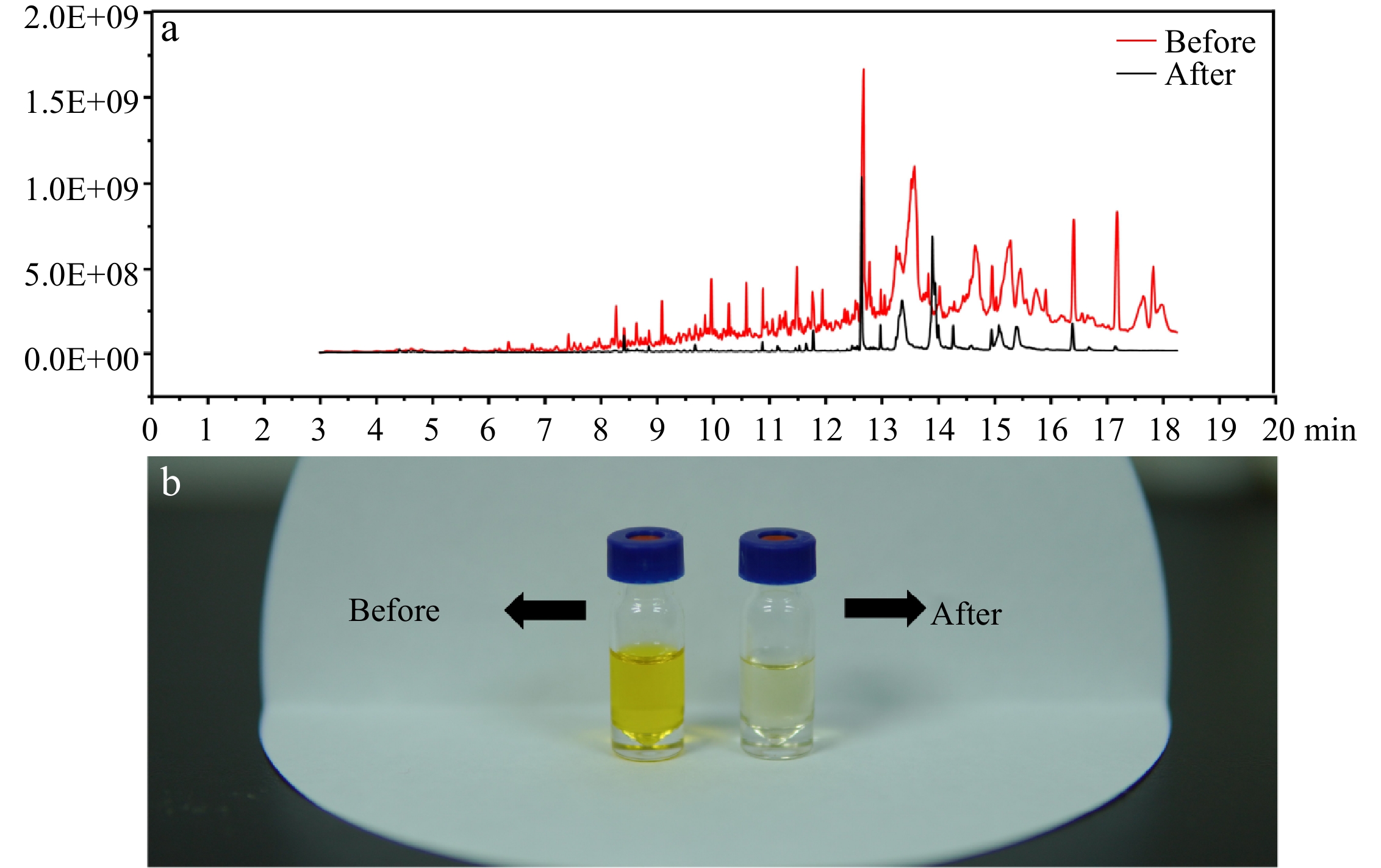
Berbanding dengan kajian terdahulu kami [21], prosedur pengekstrakan cecair cecair digabungkan sebelum suntikan ke GC-MS/MS untuk meningkatkan kepekaan dan mengekalkan penyata instrumental. Dalam Rajah 2b, kaedah yang lebih baik menunjukkan peningkatan yang ketara dalam pemurnian sampel, pelarut menjadi lebih ringan. Dalam Rajah 2a, spektrum imbasan penuh (50-350 m/z) menggambarkan bahawa selepas pembersihan, garis asas spektrum MS dikurangkan dengan jelas dan puncak kromatografi yang lebih sedikit tersedia, menunjukkan bahawa sebilangan besar sebatian mengganggu telah dikeluarkan selepas pengekstrakan cecair cecair.
Rajah 2. (A) Spektrum imbasan penuh sampel sebelum dan selepas pembersihan. (b) Kesan pemurnian kaedah yang lebih baik.
Pengesahan kaedah, termasuk linearity, pemulihan, had kuantiti (LOQ) dan kesan matriks (ME), ditunjukkan dalam Jadual 1. Ia memuaskan untuk mendapatkan linearity dengan pekali penentuan (R2) lebih tinggi daripada 0.998, yang berkisar dari 0.00 hingga 0.
Pemulihan AQ dinilai pada tiga kepekatan yang diukur antara kepekatan yang diukur dan sebenar dalam teh kering (0.005, 0.02, 0.05 mg/kg), pucuk teh segar (0.005, 0.01, 0.02 mg/kg) dan sampel udara (0.5, 1.5, 3 μg/m3). Pemulihan AQ dalam teh adalah dari 77.78% hingga 113.02% dalam teh kering dan dari 96.52% hingga 125.69% dalam pucuk teh, dengan RSD% lebih rendah daripada 15%. Pemulihan AQ dalam sampel udara adalah dari 78.47% hingga 117.06% dengan RSD% di bawah 20%. Kepekatan terendah terendah telah dikenalpasti sebagai LOQ, iaitu 0.005 mg/kg, 0.005 mg/kg dan 0.5 μg/m³ dalam pucuk teh, teh kering dan sampel udara. Seperti yang disenaraikan dalam Jadual 1, matriks teh kering dan pucuk teh sedikit meningkatkan tindak balas AQ, yang membawa kepada ME sebanyak 109.0% dan 110.9%. Bagi matriks sampel udara, ME adalah 196.1%.
Tahap AQ semasa pemprosesan teh hijau
Dengan tujuan mencari kesan sumber haba yang berbeza pada persekitaran teh dan pemprosesan, kumpulan daun segar dibahagikan kepada dua kumpulan tertentu dan diproses secara berasingan dalam dua bengkel pemprosesan dalam perusahaan yang sama. Satu kumpulan dibekalkan dengan elektrik, dan yang lain dengan arang batu.
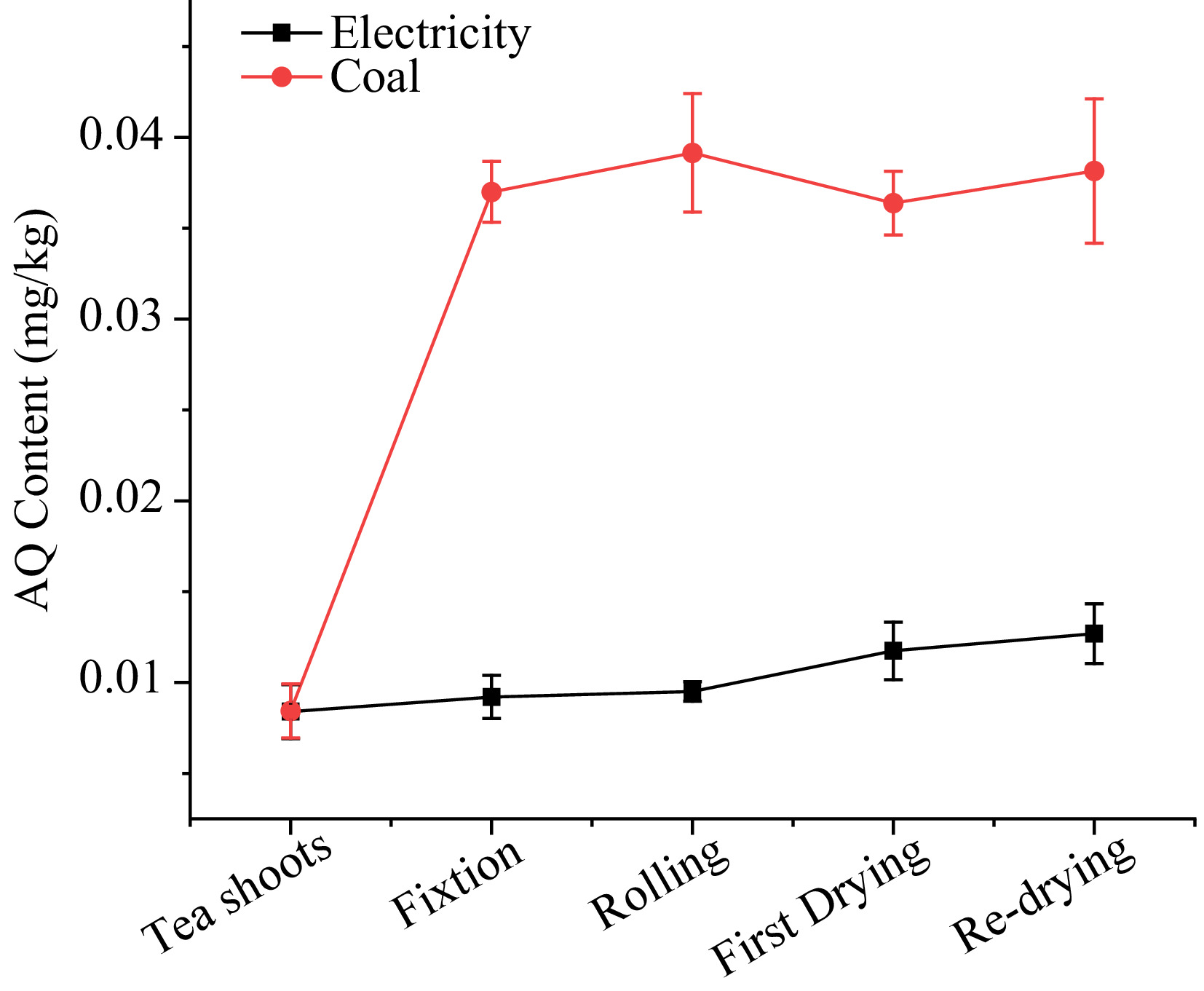
Seperti yang ditunjukkan dalam Rajah 3, tahap AQ dengan elektrik sebagai sumber haba berkisar antara 0.008 hingga 0.013 mg/kg. Semasa proses penetapan, parching daun teh yang disebabkan oleh pemprosesan dalam periuk dengan suhu tinggi mengakibatkan kenaikan 9.5% dalam aq. Kemudian, tahap AQ kekal semasa proses rolling walaupun kehilangan jus, menunjukkan bahawa proses fizikal mungkin tidak menjejaskan tahap AQ dalam pemprosesan teh. Selepas langkah pengeringan pertama, tahap AQ meningkat sedikit dari 0.010 hingga 0.012 mg/kg, kemudian terus meningkat kepada 0.013 mg/kg sehingga akhir pengeringan semula. PFS, yang menunjukkan variasi dalam setiap langkah, adalah 1.10, 1.03, 1.24, 1.08 dalam penetapan, rolling, pengeringan pertama dan pengeringan semula. Hasil PFS mencadangkan bahawa pemprosesan di bawah tenaga elektrik mempunyai sedikit kesan pada tahap AQ dalam teh.
Rajah 3. Tahap AQ semasa pemprosesan teh hijau dengan elektrik dan arang batu sebagai sumber haba.
Dalam kes arang batu sebagai sumber haba, kandungan AQ meningkat dengan ketara semasa pemprosesan teh, melonjak dari 0.008 hingga 0.038 mg/kg. 338.9% aq meningkat dalam prosedur penetapan, mencapai 0.037 mg/kg, yang jauh melebihi MRL 0.02 mg/kg yang ditetapkan oleh Kesatuan Eropah. Semasa peringkat rolling, tahap AQ masih meningkat sebanyak 5.8% walaupun jauh dari mesin penetapan. Dalam pengeringan pertama dan pengeringan semula, kandungan AQ meningkat sedikit atau menurun sedikit. PFS menggunakan arang batu sebagai sumber haba dalam penetapan, pengeringan pertama dan pengeringan semula adalah 4.39, 1.05, 0.93, dan 1.05.
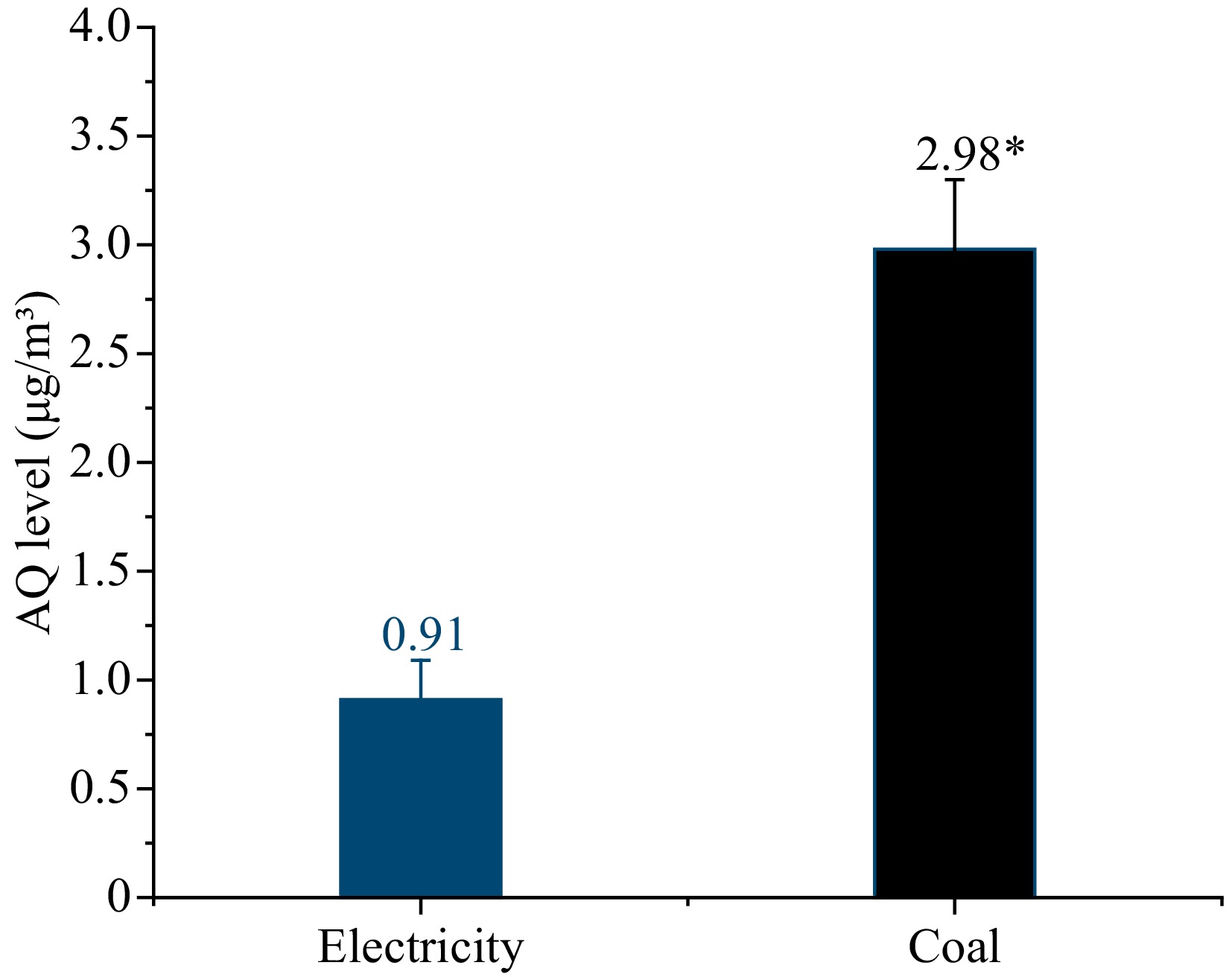
Untuk terus menentukan hubungan antara pembakaran arang batu dan pencemaran AQ, perkara zarah yang digantung (PMS) di udara di bengkel di bawah kedua -dua sumber haba dikumpulkan untuk penilaian udara, seperti yang ditunjukkan dalam Rajah 4.
Rajah 4. Tahap AQ di alam sekitar dengan elektrik dan arang batu sebagai sumber haba. * Menunjukkan perbezaan yang signifikan dalam tahap AQ dalam sampel (p <0.05).
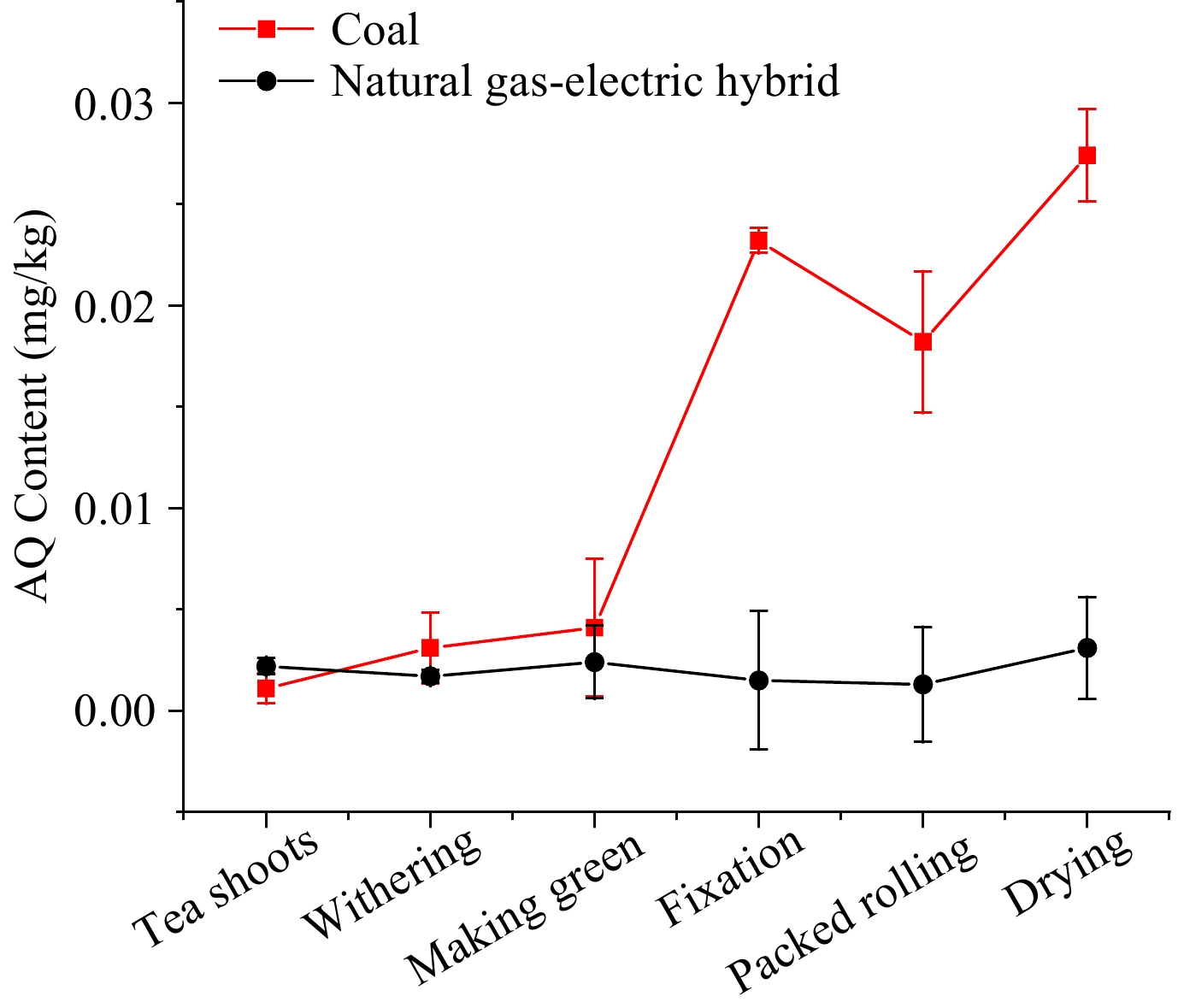
Tahap AQ semasa pemprosesan teh oolong teh oolong, terutamanya yang dihasilkan di Fujian dan Taiwan, adalah sejenis teh yang ditapai. Untuk terus menentukan langkah-langkah utama peningkatan tahap AQ dan kesan bahan api yang berbeza, kumpulan daun segar yang sama dibuat ke dalam teh oolong dengan hibrid arang batu dan gas asli sebagai sumber haba, pada masa yang sama. Tahap AQ dalam pemprosesan teh oolong menggunakan sumber haba yang berbeza ditunjukkan dalam Rajah 5. Bagi pemprosesan teh oolong dengan hibrid elektrik gas asli, trend tahap AQ tidak berubah di bawah 0.005 mg/kg, yang serupa dengan teh hijau dengan elektrik.
Rajah 5. Tahap AQ semasa pemprosesan teh oolong dengan campuran gas asli dan arang batu sebagai sumber haba.
Dengan arang batu sebagai sumber haba, tahap AQ dalam dua langkah pertama, lonjakan dan membuat hijau, pada dasarnya sama dengan campuran gas elektrik asli. Walau bagaimanapun, prosedur berikutnya sehingga penetapan menunjukkan jurang melebar secara beransur -ansur, di mana tahap AQ melonjak dari 0.004 hingga 0.023 mg/kg. Tahap dalam langkah rolling yang dibungkus menurun kepada 0.018 mg/kg, yang mungkin disebabkan oleh kehilangan jus teh yang membawa beberapa bahan pencemar AQ. Selepas peringkat rolling, tahap di peringkat pengeringan meningkat kepada 0.027 mg/kg. Dalam lonjakan, membuat hijau, penetapan, rolling dan pengeringan yang dibungkus, PFS masing -masing adalah 2.81, 1.32, 5.66, 0.78, dan 1.50.
Kejadian AQ dalam produk teh dengan sumber haba yang berbeza
Untuk menentukan kesan pada kandungan AQ teh dengan sumber haba yang berbeza, 40 sampel teh dari bengkel teh menggunakan elektrik atau arang batu sebagai sumber haba dianalisis, seperti yang ditunjukkan dalam Jadual 2. 35.0% diperhatikan dalam sampel arang batu. Yang paling jelas, elektrik mempunyai kadar detektif dan kegembiraan yang paling rendah sebanyak 56.4% dan 7.7%, dengan kandungan maksimum 0.020 mg/kg.
Perbincangan
Berdasarkan PFS semasa pemprosesan dengan dua jenis sumber haba, jelas bahawa penetapan adalah langkah utama yang membawa kepada peningkatan tahap AQ dalam pengeluaran teh dengan arang batu dan pemprosesan di bawah tenaga elektrik mempunyai sedikit kesan pada kandungan AQ dalam teh. Semasa pemprosesan teh hijau, pembakaran arang batu menghasilkan banyak asap dalam proses penetapan berbanding dengan proses pemanasan elektrik, menunjukkan bahawa mungkin asap adalah sumber utama pencemar AQ dari sentuhan dengan pucuk teh dengan serta -merta dalam pemprosesan teh, sama seperti proses pendedahan dalam sampel barbeku asap [25]. Peningkatan sedikit kandungan AQ semasa peringkat rolling mencadangkan bahawa asap yang disebabkan oleh pembakaran arang batu bukan sahaja menjejaskan tahap AQ semasa langkah penetapan, tetapi juga dalam persekitaran pemprosesan akibat pemendapan atmosfera. Coal juga digunakan sebagai sumber haba dalam pengeringan pertama dan mengeringkan semula, tetapi dalam kedua-dua langkah ini kandungan AQ meningkat sedikit atau menurun sedikit. Ini boleh dijelaskan oleh hakikat bahawa pengering angin panas yang disimpan terus teh dari asap yang disebabkan oleh pembakaran arang batu [26]. Untuk menentukan sumber pencemar, tahap AQ di atmosfera dianalisis, menghasilkan jurang yang ketara antara kedua -dua bengkel tersebut. Sebab utama ini ialah arang batu yang digunakan dalam penetapan, pengeringan pertama dan pengeringan semula akan menghasilkan AQ semasa pembakaran tidak lengkap. AQ ini kemudian diserap dalam zarah -zarah kecil pepejal selepas pembakaran arang batu dan tersebar di udara, meningkatkan tahap pencemaran AQ dalam persekitaran bengkel [15]. Dari masa ke masa, disebabkan oleh kawasan permukaan spesifik yang besar dan kapasiti penjerapan teh, partikel -partikel ini kemudian diselesaikan di permukaan daun teh, mengakibatkan peningkatan AQ dalam pengeluaran. Oleh itu, pembakaran arang batu dianggap sebagai laluan utama yang membawa kepada pencemaran AQ yang berlebihan dalam pemprosesan teh, dengan asap menjadi sumber pencemaran.
Bagi pemprosesan teh oolong, AQ meningkat di bawah pemprosesan dengan kedua -dua sumber haba, tetapi perbezaan antara kedua -dua sumber haba adalah penting. Hasilnya juga mencadangkan bahawa arang batu sebagai sumber haba memainkan peranan utama dalam meningkatkan tahap AQ, dan penetapan itu dianggap sebagai langkah utama untuk meningkatkan pencemaran AQ dalam pemprosesan teh oolong berdasarkan PFS. Semasa pemprosesan teh oolong dengan hibrid elektrik gas asli sebagai sumber haba, trend paras AQ tidak berubah di bawah 0.005 mg/kg, yang sama dengan teh hijau dengan elektrik, menunjukkan bahawa tenaga bersih, seperti elektrik dan gas asli, dapat mengurangkan risiko menghasilkan bahan pencemar AQ dari pemprosesan dari pemprosesan.
Bagi ujian persampelan, hasilnya menunjukkan bahawa keadaan pencemar AQ lebih buruk apabila menggunakan arang batu sebagai sumber haba dan bukannya elektrik, yang mungkin disebabkan oleh asap dari pembakaran arang batu yang bersentuhan dengan daun teh dan berlarutan di sekitar tempat kerja. Walau bagaimanapun, walaupun jelas bahawa elektrik adalah sumber haba yang paling bersih semasa pemprosesan teh, masih terdapat pencemaran AQ dalam produk teh menggunakan elektrik sebagai sumber haba. Keadaan ini seolah-olah sedikit serupa dengan kerja yang diterbitkan sebelum ini di mana reaksi 2-alkenal dengan hydroquinones dan benzoquinones dicadangkan sebagai laluan kimia yang berpotensi [23], sebab-sebab ini akan disiasat dalam penyelidikan masa depan.
Kesimpulan
Dalam kerja ini, kemungkinan sumber pencemaran AQ dalam teh hijau dan oolong telah disahkan oleh eksperimen perbandingan berdasarkan kaedah analisis GC-MS/MS yang lebih baik. Penemuan kami secara langsung menyokong bahawa sumber pencemar utama tahap tinggi AQ adalah asap yang disebabkan oleh pembakaran, yang bukan sahaja mempengaruhi peringkat pemprosesan tetapi juga mempengaruhi persekitaran bengkel. Tidak seperti dalam peringkat rolling dan lonat, di mana perubahan dalam tahap AQ tidak mencolok, peringkat dengan penglibatan langsung arang batu dan kayu api, seperti penetapan, adalah proses utama di mana pencemaran AQ meningkat disebabkan oleh jumlah hubungan antara teh dan asap semasa peringkat ini. Oleh itu, bahan api bersih seperti gas asli dan elektrik disyorkan sebagai sumber haba dalam pemprosesan teh. Di samping itu, keputusan eksperimen juga menunjukkan bahawa jika tiada asap yang dihasilkan oleh pembakaran, masih terdapat faktor -faktor lain yang menyumbang untuk mengesan AQ semasa pemprosesan teh, sementara sejumlah kecil AQ juga diperhatikan di bengkel dengan bahan api bersih, yang harus disiasat lagi dalam penyelidikan masa depan.
Bahan dan kaedah
Reagen, bahan kimia dan bahan
Standard Anthraquinone (99.0%) dibeli daripada Dr. Ehrenstorfer GmbH Company (Augsburg, Jerman). Standard dalaman D8-Anthraquinone (98.6%) telah dibeli daripada isotop C/D/N (Quebec, Kanada). Natrium sulfat anhydrous (Na2SO4) dan magnesium sulfat (MgSO4) (Shanghai, China). Florisil dibekalkan oleh Wenzhou Organic Chemical Company (Wenzhou, China). Kertas serat kaca Mircro (90 mm) dibeli dari Ahlstrom-Munksjö Company (Helsinki, Finland).
Penyediaan sampel
Sampel teh hijau diproses dengan penetapan, rolling, pengeringan pertama dan pengeringan semula (menggunakan peralatan tertutup), manakala sampel teh oolong diproses dengan lonjakan, membuat hijau (goyang dan berdiri daun segar secara bergantian), penetapan, bergulir, dan pengeringan. Sampel dari setiap langkah dikumpulkan tiga kali pada 100g selepas pencampuran menyeluruh. Semua sampel disimpan pada -20 ° C untuk analisis selanjutnya.
Sampel udara dikumpulkan oleh kertas serat kaca (90 mm) menggunakan sampler volum sederhana (PTS-100, Qingdao Laoshan Electronic Instrument Company, Qingdao, China) [27], berjalan pada 100 L/min selama 4 jam.
Sampel yang diperkaya telah meningkat dengan AQ pada 0.005 mg/kg, 0.010 mg/kg, 0.020 mg/kg untuk pucuk teh segar, pada 0.005 mg/kg, 0.020 mg/kg, 0.050 mg/kg untuk teh kering dan pada 0.012 mg/kg (0.5 μg/m3 (0.5 μg/cg/m3 (0.5 μg/cg/m3 (0.5 μg/mg/m3 untuk udara kering (0.5 μg/mg/mg/0 0.00 mg/kg, smaple udara), 0.072 mg/kg (3.0 μg/m3 untuk sampel udara) untuk kertas penapis kaca. Selepas berjabat dengan teliti, semua sampel ditinggalkan selama 12 jam, diikuti dengan langkah pengekstrakan dan pembersihan.
Kandungan kelembapan diperoleh dengan mengambil 20 g sampel selepas mencampurkan setiap langkah, pemanasan pada 105 ° C selama 1 jam, kemudian menimbang dan mengulangi tiga kali dan mengambil nilai purata dan membahagikannya dengan berat sebelum pemanasan.
Pengekstrakan sampel dan pembersihan
Contoh Teh: Pengekstrakan dan pemurnian AQ dari sampel teh dilakukan berdasarkan kaedah yang diterbitkan dari Wang et al. dengan beberapa penyesuaian [21]. Secara ringkas, 1.5 g sampel teh pertama kali dicampur dengan 30 μl D8-AQ (2 mg/kg) dan dibiarkan berdiri selama 30 minit, kemudian dicampur dengan 1.5 ml air deionized dan dibiarkan berdiri selama 30 minit. 15 ml 20% aseton dalam n-heksana telah ditambah kepada sampel teh dan diawasi selama 15 minit. Kemudian sampel telah dibuang dengan 1.0 g MgSO4 selama 30 s, dan disentrifugasi selama 5 minit, pada 11,000 rpm. Setelah dipindahkan ke 100 ml berbentuk pir, 10 ml fasa organik atas telah disejat ke hampir kekeringan di bawah vakum pada suhu 37 ° C. 5 ml 2.5% aseton dalam n-hexane membubarkan semula ekstrak dalam kikat berbentuk pir untuk pembersihan. Lajur kaca (10 cm × 0.8 cm) terdiri daripada bahagian bawah ke atas bulu kaca dan 2G Florisil, yang terletak di antara dua lapisan 2 cm Na2SO4. Kemudian 5 ml sebanyak 2.5% aseton dalam n-hexane menyusun semula lajur. Selepas memuatkan larutan redissolved, AQ telah dielakkan tiga kali dengan 5 ml, 10 mL, 10 mL dari 2.5% aseton dalam n-heksana. Eluates gabungan telah dipindahkan ke berkotak berbentuk pir dan disejat ke hampir kekeringan di bawah vakum pada suhu 37 ° C. Sisa kering kemudiannya direkulasi semula dengan 1 ml sebanyak 2.5% aseton dalam heksana diikuti dengan penapisan melalui penapis saiz liang 0.22 μm. Kemudian penyelesaian yang direkabentuk dicampur dengan asetonitril pada nisbah isipadu 1: 1. Berikutan langkah gemetar, subnatan digunakan untuk analisis GC-MS/MS.
Sampel udara: Separuh kertas serat, menetes dengan 18 μL D8-AQ (2 mg/kg), direndam dalam 15 mL 20% aseton dalam n-heksana, kemudian diawasi selama 15 minit. Fasa organik dipisahkan oleh sentrifugasi pada 11,000 rpm selama 5 minit dan keseluruhan lapisan atas dikeluarkan dalam botol berbentuk pir. Semua fasa organik telah disejat ke hampir kekeringan di bawah vakum pada suhu 37 ° C. 5 ml 2.5% aseton dalam heksana redissolved ekstrak untuk pembersihan dengan cara yang sama seperti dalam sampel teh.
Analisis GC-MS/MS
Varian 450 kromatografi gas yang dilengkapi dengan pengesan massa Varian 300 Tandem (Varian, Walnut Creek, CA, Amerika Syarikat) digunakan untuk melakukan analisis AQ dengan perisian Workstation versi 6.9.3. Faktor Varian Empat lajur kapilari VF-5ms (30 m × 0.25 mm × 0.25 μm) digunakan untuk pemisahan kromatografi. Gas pembawa, helium (> 99.999%), ditetapkan pada kadar aliran tetap 1.0 ml/min dengan gas perlanggaran argon (> 99.999%). Suhu ketuhar bermula dari 80 ° C dan dipegang selama 1 minit; meningkat pada suhu 15 ° C/min hingga 240 ° C, kemudian mencapai 260 ° C pada 20 ° C/min dan dipegang selama 5 minit. Suhu sumber ion adalah 210 ° C, serta suhu garis pemindahan 280 ° C. Jumlah suntikan ialah 1.0 μl. Keadaan MRM ditunjukkan dalam Jadual 3.
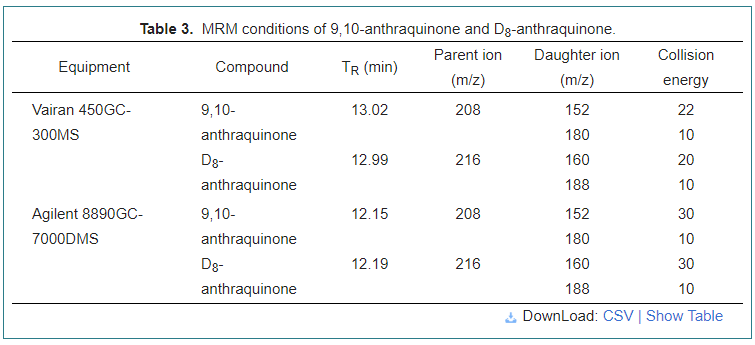
Agilent 8890 kromatografi gas yang dilengkapi dengan spektrometer massa quadrupole 7000D triple Agilent (Agilent, Stevens Creek, CA, Amerika Syarikat) digunakan untuk menganalisis kesan pembersihan dengan perisian versi 10.1 Masshunter. Agilent J & W HP-5MS GC lajur (30 m × 0.25 mm × 0.25 μm) digunakan untuk pemisahan kromatografi. Gas pembawa, helium (> 99.999%), ditetapkan pada kadar aliran malar 2.25 ml/min dengan gas perlanggaran nitrogen (> 99.999%). Suhu sumber ion EI diselaraskan pada 280 ° C, sama dengan suhu garis pemindahan. Suhu ketuhar bermula dari 80 ° C dan diadakan selama 5 minit; Dibesarkan sebanyak 15 ° C/min hingga 240 ° C, kemudian mencapai 280 ° C pada 25 ° C/min dan dikekalkan selama 5 minit. Keadaan MRM ditunjukkan dalam Jadual 3.
Analisis statistik
Kandungan AQ dalam daun segar telah diperbetulkan kepada kandungan bahan kering dengan membahagikan kandungan kelembapan untuk membandingkan dan menganalisis tahap AQ semasa pemprosesan.
Perubahan AQ dalam sampel teh dinilai dengan perisian Microsoft Excel dan statistik IBM SPSS 20.
Faktor pemprosesan digunakan untuk menggambarkan perubahan dalam AQ semasa pemprosesan teh. PF = RL/RF, di mana RF adalah tahap AQ sebelum langkah pemprosesan dan RL adalah tahap AQ selepas langkah pemprosesan. PF menunjukkan penurunan (PF <1) atau peningkatan (pf> 1) dalam sisa AQ semasa langkah pemprosesan tertentu.
Saya menunjukkan penurunan (saya <1) atau peningkatan (saya> 1) sebagai tindak balas kepada instrumen analisis, yang berdasarkan nisbah lereng penentukuran dalam matriks dan pelarut seperti berikut:
ME = (slopematrix/slopesolvent - 1) × 100%
Di mana slopematrix adalah cerun lengkung penentukuran dalam pelarut yang dipadankan dengan matriks, slopesolvent adalah cerun lengkung penentukuran dalam pelarut.
Penghargaan
Kerja ini disokong oleh projek utama sains dan teknologi di wilayah Zhejiang (2015c12001) dan Yayasan Sains Kebangsaan China (42007354).
Konflik kepentingan
Penulis mengisytiharkan bahawa mereka tidak mempunyai konflik kepentingan.
Hak dan kebenaran
Hak cipta: © 2022 oleh pengarang. Pemegang Lesen Eksklusif Akademik Maksimum Akademik, Fayetteville, GA. Artikel ini adalah artikel akses terbuka yang diedarkan di bawah Lesen Atribusi Creative Commons (CC oleh 4.0), lawati https://creativecommons.org/licenses/by/4.0/.
Rujukan
[1] ITC. 2021. Buletin Statistik Tahunan 2021. https://inttea.com/publication/
[2] Hicks A. 2001. Kajian semula pengeluaran teh global dan kesan ke atas industri keadaan ekonomi Asia. AU Journal of Technology 5
Google Scholar
[3] Katsuno T, Kasuga H, Kusano Y, Yaguchi Y, Tomomura M, et al. 2014. Pencirian sebatian bau dan pembentukan biokimia mereka dalam teh hijau dengan proses penyimpanan suhu yang rendah. Kimia Makanan 148: 388-95 doi: 10.1016/j.foodchem.2013.10.069
Crossref Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Rantaian pencemaran tri-dimtes dalam ekosistem teh dan kawalannya. Scientia Agricultura Sinica 40: 948-58
Google Scholar
[5] Dia H, Shi L, Yang G, You M, Vasseur L. 2020. Penilaian risiko ekologi logam berat tanah dan sisa racun perosak di ladang teh. Pertanian 10:47 doi: 10.3390/pertanian10020047
Crossref Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J, et al. 2005. Pencemaran utama dalam daun teh dan faktor bukan edaphic yang mempengaruhi. Chemosphere 61: 726-32 doi: 10.1016/j.chemosphere.2005.03.053
Crossref Google Scholar
[7] Owuor PO, Obaga SO, Othieno CO. 1990. Kesan ketinggian pada komposisi kimia teh hitam. Jurnal Sains Makanan dan Pertanian 50: 9-17 doi: 10.1002/jsfa.2740500103
Crossref Google Scholar
[8] Garcia Londoño VA, Reynoso M, Resnik S. 2014. Hydrocarbons aromatik polycyclic (PAHS) dalam pasangan yerba (Ilex paraguariensis) dari pasaran Argentina. Aditif & Pencemaran Makanan: Bahagian B 7: 247-53 DOI: 10.1080/19393210.2014.919963
Crossref Google Scholar
[9] Ishizaki A, Saito K, Hanioka N, Narimatsu S, Kataoka H. 2010. Penentuan hidrokarbon aromatik polycyclic dalam sampel makanan secara automatik dalam talian microextraction fasa pepejal dalam talian. Jurnal Kromatografi A 1217: 5555-63 doi: 10.1016/j.chroma.2010.06.068
Crossref Google Scholar
[10] Phan Thi LA, Ngoc NT, Quynh NT, Thanh NV, Kim TT, et al. 2020. Hidrokarbon aromatik polycyclic (PAHs) dalam daun teh kering dan infusi teh di Vietnam: tahap pencemaran dan penilaian risiko diet. Geokimia dan Kesihatan Alam Sekitar 42: 2853-63 DOI: 10.1007/s10653-020-00524-3
Crossref Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. Kejadian 16 EPA PAHs dalam Makanan - Kajian. Sebatian aromatik polycyclic 35: 248-84 doi: 10.1080/10406638.2014.918550
Crossref Google Scholar
[12] Omodara NB, Olabemiwo OM, Adedosu TA. 2019. Perbandingan PAH yang dibentuk dalam kayu api dan arang stok salai dan ikan kucing. Jurnal Amerika Sains dan Teknologi Makanan 7: 86-93 DOI: 10.12691/AJFST-7-3-3
Crossref Google Scholar
[13] Zou LY, Zhang W, Atkiston S. 2003. Pencirian pelepasan hidrokarbon aromatik polycyclic daripada membakar spesies kayu api yang berlainan di Australia. Pencemaran Alam Sekitar 124: 283-89 doi: 10.1016/s0269-7491 (02) 00460-8
Crossref Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL, et al. 2000. Aktiviti benzo [a] pyrene dan metabolit hidroksilatnya dalam ujian gen reseptor-α estrogen. Sains Toksikologi 55: 320-26 doi: 10.1093/toxsci/55.2.320
Crossref Google Scholar
[15] Han Y, Chen Y, Ahmad S, Feng Y, Zhang F, et al. 2018. Pengukuran masa yang tinggi dan saiz yang diselesaikan PM dan komposisi kimia dari pembakaran arang batu: implikasi untuk proses pembentukan EC. Sains & Teknologi Alam Sekitar 52: 6676-85 doi: 10.1021/acs.est.7b05786
Crossref Google Scholar
[16] Khiadani (Haji) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M, et al. 2013. Penentuan kepekatan hidrokarbon aromatik polycyclic dalam lapan jenama teh hitam yang digunakan lebih banyak di Iran. Jurnal Antarabangsa Kejuruteraan Kesihatan Alam Sekitar 2:40 doi: 10.4103/2277-9183.122427
Crossref Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J, Andrews G, Jones JM, et al. 2007. Pelepasan spesies oksigen dari pembakaran kayu pain dan hubungannya dengan pembentukan jelaga. Proses Keselamatan dan Perlindungan Alam Sekitar 85: 430-40 DOI: 10.1205/PSEP07020
Crossref Google Scholar
[18] Shen G, Tao S, Wang W, Yang Y, Ding J, et al. 2011. Pelepasan hidrokarbon aromatik polycyclic oksigen dari pembakaran bahan api pepejal dalaman. Sains & Teknologi Alam Sekitar 45: 3459-65 DOI: 10.1021/ES104364T
Crossref Google Scholar
[19] Agensi Antarabangsa Penyelidikan Kanser (IARC), Pertubuhan Kesihatan Sedunia. 2014. Ekzos enjin diesel dan petrol dan beberapa nitroaren. Agensi Antarabangsa untuk Penyelidikan mengenai Monograf Kanser mengenai Penilaian Risiko Karsinogenik kepada Manusia. Laporan. 105: 9
[20] De Oliveira Galvão MF, De Oliveira Alves N, Ferreira PA, Caumo S, de Castro Vasconcellos P, et al. 2018. Biomass pembakaran zarah di rantau Amazon Brazil: kesan mutagenik nitro dan oxy-PAHs dan penilaian risiko kesihatan. Pencemaran Alam Sekitar 233: 960-70 doi: 10.1016/j.envpol.2017.09.068
Crossref Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H, et al. 2018. 9,10-anthraquinone deposit di ladang teh mungkin salah satu sebab pencemaran dalam teh. Kimia Makanan 244: 254-59 doi: 10.1016/j.foodchem.2017.09.123
Crossref Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Pengenalpastian pencemaran 9,10-anthraquinone semasa pemprosesan teh hitam dan hijau di Indonesia. Kimia Makanan 327: 127092 doi: 10.1016/j.foodchem.2020.127092
Crossref Google Scholar
[23] Zamora R, Hidalgo FJ. 2021. Pembentukan naphthoquinones dan anthraquinones oleh reaksi karbonyl-hydroquinone/benzoquinone: laluan yang berpotensi untuk asal 9,10-anthraquinone dalam teh. Kimia Makanan 354: 129530 doi: 10.1016/j.foodchem.2021.129530
Crossref Google Scholar
[24] Yang M, Luo F, Zhang X, Wang X, Sun H, et al. 2022. Pengambilan, translocation, dan metabolisme anthracene dalam tumbuhan teh. Sains Persekitaran Total 821: 152905 doi: 10.1016/j.scitotenv.2021.152905
Crossref Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019 pengaruh merokok dan barbeku pada kandungan anthraquinone (ATQ) dan hidrokarbon aromatik polycyclic (PAHs) dalam sosis jenis Frankfurter. Jurnal Kimia Pertanian dan Makanan 67: 13998-4004 doi: 10.1021/acs.Jafc.9b03316
Crossref Google Scholar
[26] Fouillaud M, Caro Y, Venkatachalam M, Grondin I, Dufossé L. 2018. Anthraquinones. Dalam sebatian fenolik dalam makanan: pencirian dan analisis, eds. Leo ML.Vol. 9. Boca Raton: CRC Press. ms 130-70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muniategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, et al. 2003. Kaedah baru untuk penentuan serentak PAH dan logam dalam sampel bahan partikulat atmosfera. Persekitaran atmosfera 37: 4171-75 doi: 10.1016/s1352-2310 (03) 00523-5
Crossref Google Scholar
Mengenai artikel ini
Cite artikel ini
Yu J, Zhou L, Wang X, Yang M, Sun H, et al. 2022. 9,10-anthraquinone pencemaran dalam pemprosesan teh menggunakan arang batu sebagai sumber haba. Penyelidikan Loji Minuman 2: 8 doi: 10.48130/bpr-2022-0008
Masa Post: Mei-09-2022