抽象的な
9,10-アントラキノン(AQ)は、潜在的な発がんリスクを伴う汚染物質であり、世界中の茶で発生します。欧州連合(EU)が設定した茶中のAQの最大残留限界(MRL)は0.02 mg/kgです。 TEA処理におけるAQの可能性のある原因とその発生の主要な段階は、修正されたAQ分析方法とガスクロマトグラフィータンデム質量分析(GC-MS/MS)分析に基づいて調査されました。緑茶加工の熱源としての電気と比較して、aqは熱源として石炭を使用して茶加工で4.3から23.9倍に増加し、0.02 mg/kgをはるかに超え、環境のAQレベルは3倍になりました。石炭熱の下でのウーロン茶加工でも同じ傾向が観察されました。茶葉と煙との間に直接接触したステップは、固定や乾燥など、茶加工におけるAQ生産の主要なステップと見なされます。 AQのレベルは接触時間の上昇とともに増加し、茶中の高レベルのAQ汚染物質が石炭と燃焼によって引き起こされる煙に由来する可能性があることを示唆しています。熱源として電気または石炭を備えた異なるワークショップの40のサンプルが分析され、検出の場合は50.0%-85.0%および5.0%-35.0%の範囲で、AQの割合を超えました。さらに、0.064 mg/kgの最大AQ含有量は、炭で熱源として石炭の茶製品で観察され、茶製品の高レベルのAQ汚染が石炭によって寄与される可能性が高いことを示しています。
キーワード:9,10-アントラキノン、お茶加工、石炭、汚染源
導入
常緑低木Camellia Sinensis(L.)O。Kuntzeの葉から製造されたお茶は、爽やかな味と健康上の利点のために最も世界的に人気のある飲み物の1つです。 2020年には、茶生産量が5,972百万トンに増加し、過去20年間で2倍になりました[1]。さまざまな加工方法に基づいて、緑茶、紅茶、ダークティー、ウーロンティー、ホワイトティー、イエローティーなど、6つの主要なタイプのお茶があります[2,3]。製品の品質と安全性を確保するには、汚染物質のレベルを監視し、起源を定義することが非常に重要です。
残留農薬、重金属、および多環芳香族炭化水素(PAH)などの他の汚染物質などの汚染物質の供給源を特定することは、汚染を制御する主なステップです。茶園における合成化学物質の直接散布、および茶園の近くの操作によって引き起こされる空気漂流は、茶中の農薬残留源です[4]。重金属は茶に蓄積し、毒性を引き起こす可能性があります。これは、主に土壌、肥料、大気に由来します[5-7]。お茶には予期せずに現れる他の汚染については、プランテーション、加工、パッケージ、保管、輸送など、生産茶チェーンの複雑な手順のために特定することは非常に困難でした。お茶のpahは、fireや炭炭などの茶葉の加工中に使用される燃料の排気と燃料の燃焼から来ました[8-10]。
石炭とfireの燃焼中に、酸化炭素などの汚染物質が形成されます[11]。その結果、これらの上記の汚染物質の残留物は、高温で穀物、スモークストック、猫の魚などの加工製品で発生し、人間の健康に脅威を与えます[12,13]。燃焼によって引き起こされるPAHは、燃料自体に含まれるPAHの揮発、芳香族化合物の高温分解、およびフリーラジカル間の化合物反応に由来します[14]。燃焼温度、時間、酸素含有量は、PAHの変換に影響を与える重要な要因です。温度の上昇とともに、PAHS含有量は最初に増加してから減少し、ピーク値は800°Cで発生しました。 PAHSの含有量は、「境界時間」と呼ばれる制限を下回る燃焼時間の増加とともに急激に減少し、燃焼空気中の酸素含有量の増加により、PAHS排出量は大幅に減少しましたが、不完全な酸化はOPAHおよび他の誘導体を生成します[15-17]。
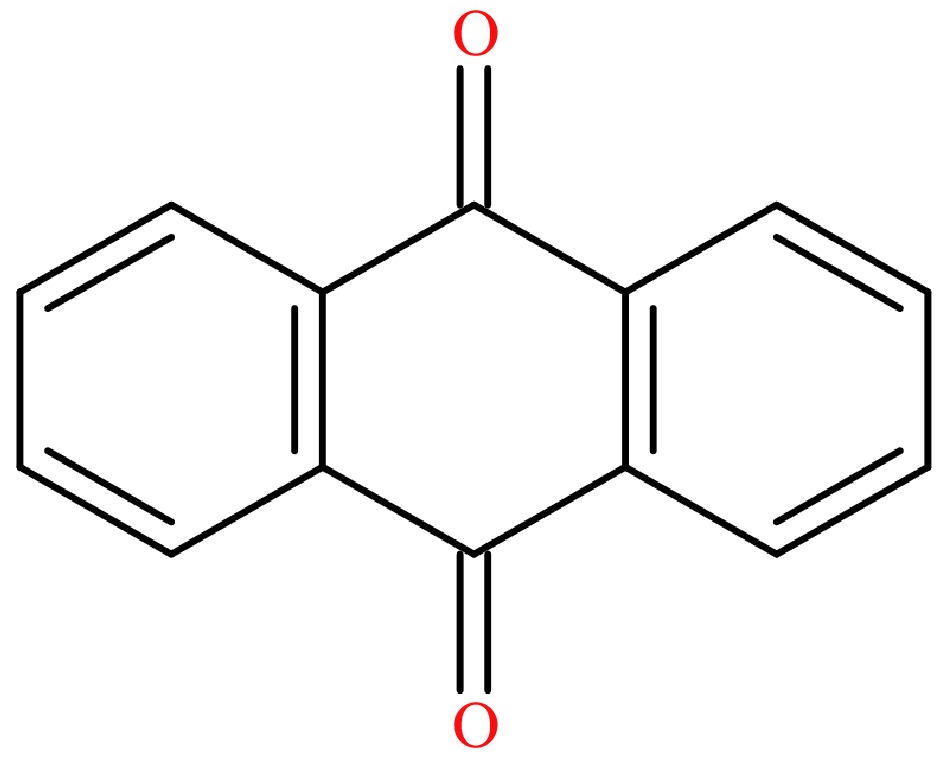
9,10-アントラキノン(AQ、CAS:84-65-1、図1)、PAHの酸素含有誘導体[18]は、3つの凝縮サイクルで構成されています。 2014年に国際癌研究機関によって発がん性の可能性(グループ2B)としてリストされました[19]。 AQはトポイソメラーゼII切断複合体に毒をかけ、DNAトポイソメラーゼIIによるアデノシン三リン酸(ATP)の加水分解を阻害し、DNA二本鎖切断を引き起こします。これは、AQ含有環境下での長期暴露と高レベルのAQとの直接接触がDNA損傷を引き起こし、癌の発生を増加させることを意味します。人間の健康に悪影響を及ぼすため、0.02 mg/kgのAQ最大残基限界(MRL)が欧州連合によってTEAで設定されました。私たちの以前の研究によると、AQの堆積物は茶農園中の主要な源として提案されました[21]。また、インドネシアの緑と紅茶の加工の実験的結果に基づいて、AQレベルが大幅に変化し、処理装置からの煙が主な理由の1つとして示唆されたことは明らかです[22]。しかし、茶加工におけるAQの正確な起源はとらえどころのないままでしたが、AQ化学経路のいくつかの仮説が示唆されており[23,24]、TEA処理のAQレベルに影響を与える重要な要因を決定することが非常に重要であることを示しています。
図1。AQの化学式。
石炭燃焼中のAQの形成と茶加工における燃料の潜在的な脅威に関する研究を考えると、茶と空気中のAQに対する熱源の処理の効果を説明するために比較実験を実施しました。
結果
メソッド検証
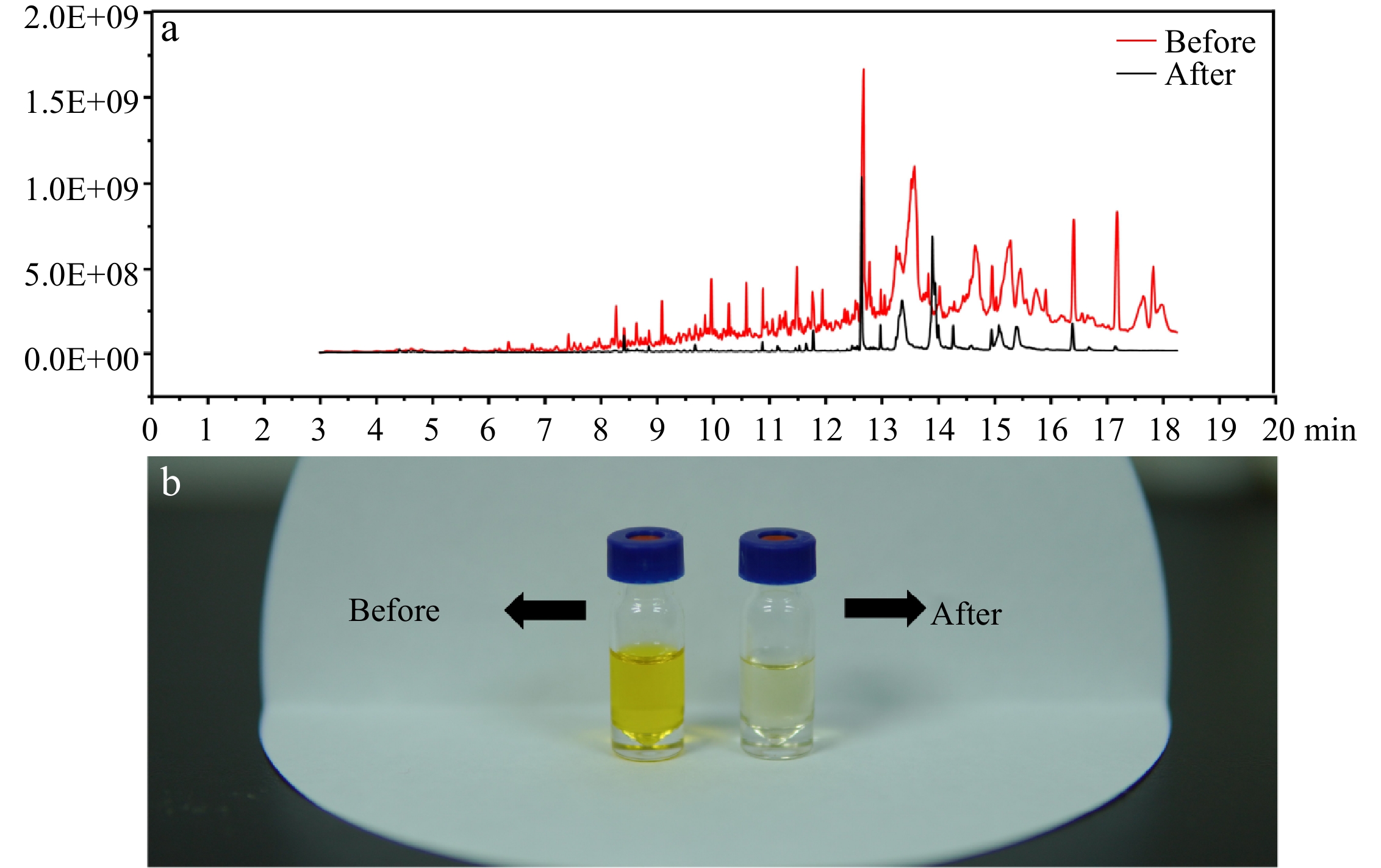
以前の研究[21]と比較して、感度を改善し、機器の声明を維持するために、GC-MS/MSに注入する前に液液抽出手順を組み合わせました。図2Bでは、改善された方法では、サンプルの精製に大幅な改善が示され、溶媒の色が軽くなりました。図2Aでは、精製後、MSスペクトルのベースラインが明らかに減少し、クロマトグラフィーピークが少なくなり、液体液体抽出後に多数の干渉化合物が除去されたことを示していることを示していることが示されました。
図2。(a)精製前後のサンプルの完全なスキャンスペクトル。 (b)改良された方法の精製効果。
線形性、回復、定量の制限(LOQ)およびマトリックス効果(ME)を含むメソッド検証を表1に示します。0.998を超える測定係数(R2)で直線性を得るのは満足です。
AQの回収は、乾燥茶(0.005、0.02、0.05 mg/kg)、新鮮なティーシュート(0.005、0.01、0.02 mg/kg)および空気サンプル(0.5、1.5、3μg/m3)の測定濃度と実際の濃度の間の3つのスパイク濃度で評価されました。茶中のAQの回収率は、乾燥茶で77.78%から113.02%、茶芽で96.52%から125.69%の範囲で、RSD%が15%未満でした。空気サンプル中のAQの回収率は78.47%から117.06%の範囲で、RSD%は20%未満でした。最も低いスパイク濃度は、それぞれ0.005 mg/kg、0.005 mg/kg、0.5μg/m³であるLOQとして同定されました。表1にリストされているように、ドライティーとティーシュートのマトリックスはAQ応答をわずかに増加させ、MEに109.0%と110.9%になりました。空気サンプルのマトリックスに関しては、MEは196.1%でした。
緑茶加工中のAQのレベル
お茶や加工環境に対するさまざまな熱源の影響を見つけることを目的として、新鮮な葉のバッチを2つの特定のグループに分割し、同じ企業の2つの処理ワークショップで個別に処理されました。 1つのグループには電気が供給され、もう1つのグループに石炭が供給されました。
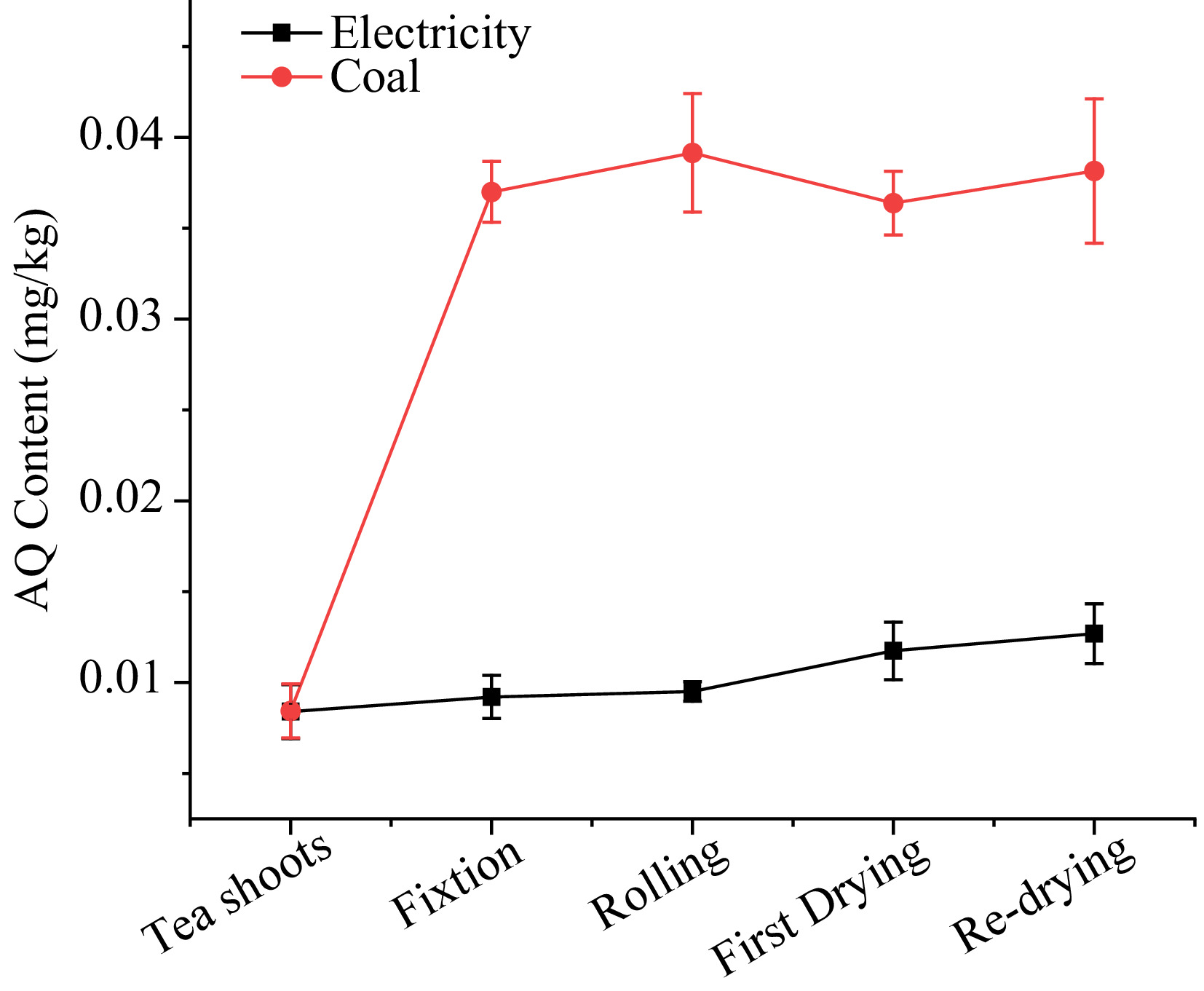
図3に示すように、熱源が0.008から0.013 mg/kgの範囲であるため、電気のAQレベル。固定プロセス中に、高温の鍋での加工によって引き起こされる茶葉の乾いた状態は、AQが9.5%増加しました。その後、ジュースの喪失にもかかわらず、ローリングプロセス中はAQのレベルが残り、物理的なプロセスがTEA処理のAQのレベルに影響を与えない可能性があることを示唆しています。最初の乾燥ステップの後、AQレベルは0.010から0.012 mg/kgにわずかに増加し、再乾燥の終わりまで0.013 mg/kgまで上昇し続けました。各ステップの変動を有意に示したPFSは、固定、ローリング、最初の乾燥、再乾燥がそれぞれ1.10、1.03、1.24、1.08でした。 PFSの結果は、電気エネルギーの下での処理が茶中のAQレベルにわずかな影響を与えることを示唆しました。
図3。熱源としての電気と石炭を使用した緑茶加工中のAQレベル。
熱源としての石炭の場合、茶加工中にAQ含有量が急激に増加し、0.008から0.038 mg/kgに急増しました。固定手順で338.9%AQが増加し、0.037 mg/kgに達し、欧州連合が設定した0.02 mg/kgのMRLをはるかに超えました。ローリング段階では、固定機から遠く離れているにもかかわらず、AQのレベルは5.8%増加しました。最初の乾燥と再乾燥では、AQ含有量はほとんど増加するか、わずかに減少しました。石炭を固定の熱源として使用するPFS、最初の乾燥と再乾燥のローリングは、それぞれ4.39、1.05、0.93、および1.05でした。
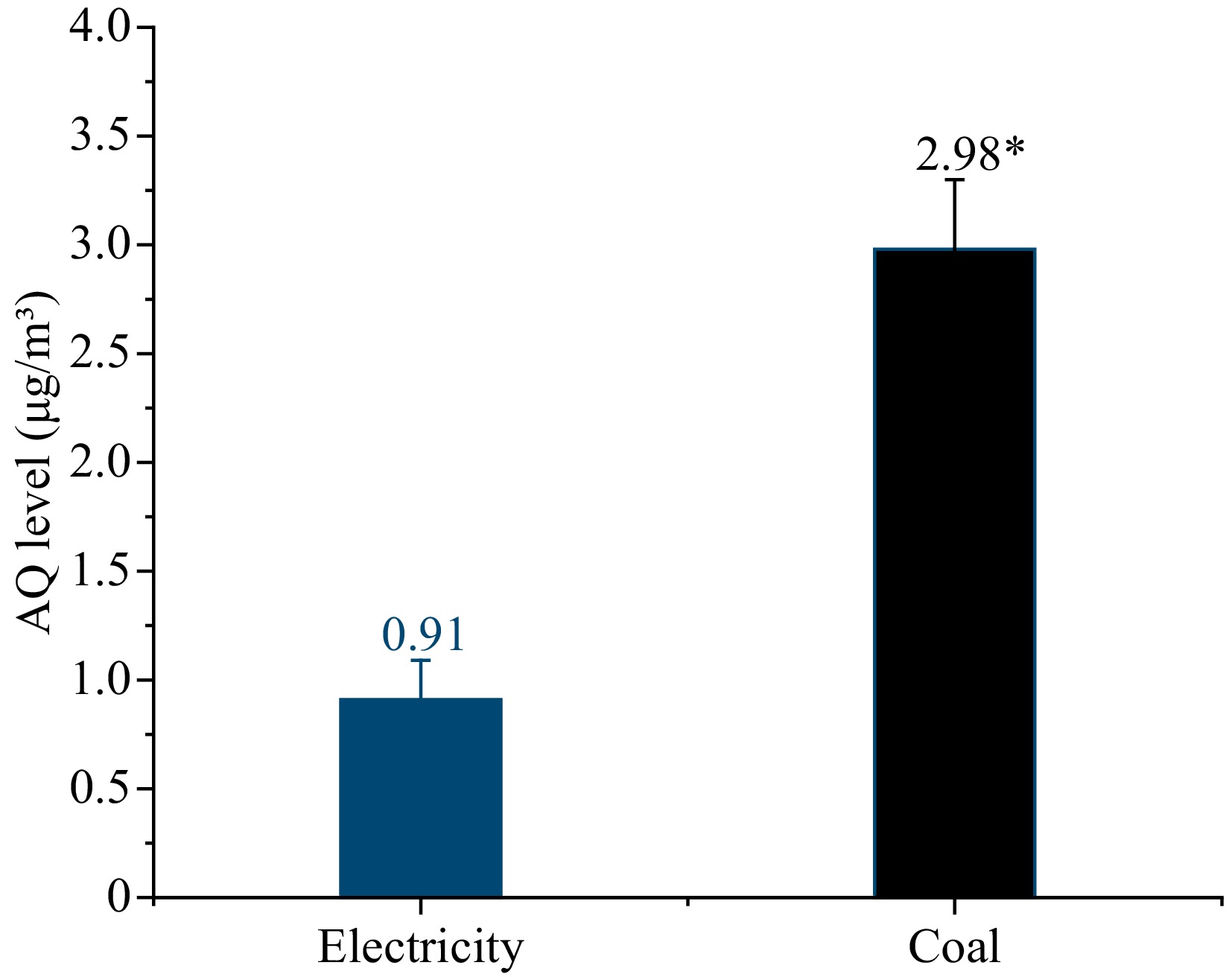
石炭燃焼とAQ汚染との関係をさらに決定するために、図4に示すように、両方の熱源の下でのワークショップの空気中の空気中の空気中の空気中の空気中の空気の問題(PMS)が収集されました。熱源は2.98μg/m3であり、電気0.91μg/m3の3倍以上でした。
図4。熱源としての電気と石炭のある環境のAQのレベル。 *サンプルのAQレベルの有意差を示します(P <0.05)。
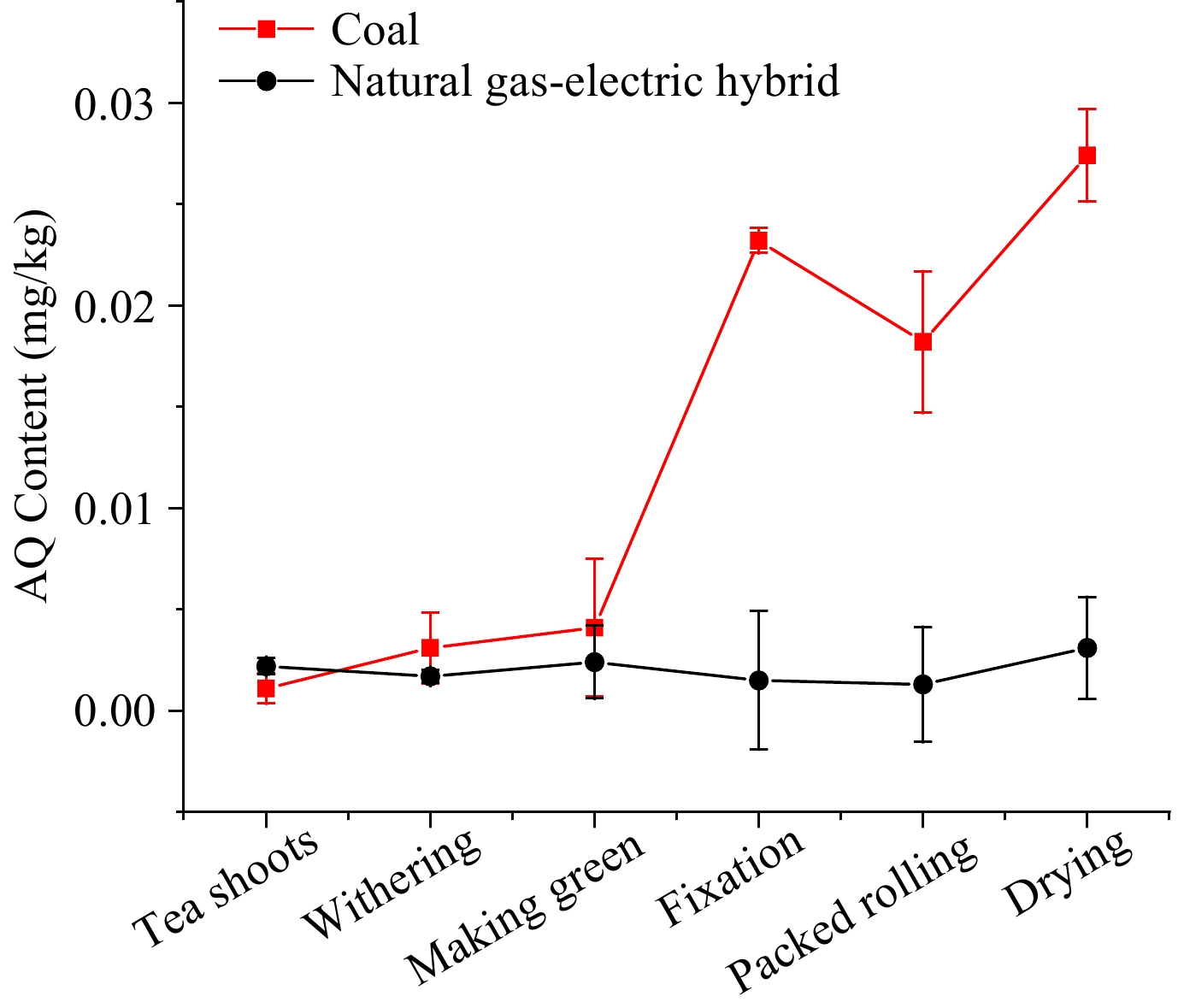
主に福建派と台湾で生産されるウーロン茶加工中のAQのレベルは、一種の部分的に発酵した茶です。 AQレベルの増加と異なる燃料の影響の主なステップをさらに判断するために、同じ新鮮な葉のバッチを同時に、熱源と同時に天然ガス電気ハイブリッドを備えたウーロン茶にしました。異なる熱源を使用したウーロン茶加工のAQレベルを図5に示します。天然ガス電気ハイブリッドを使用したウーロン茶加工については、AQレベルの傾向は0.005 mg/kg未満で停滞していました。
図5。天然ガス電気ブレンドと石炭を熱源としてのウーロン茶加工中のAQレベル。
石炭が熱源として、最初の2つのステップのAQレベルは、枯れて緑色になり、天然ガス電気ブレンドと本質的に同じでした。ただし、固定までの後続の手順では、ギャップが徐々に広がっていることが示され、その時点でAQレベルは0.004から0.023 mg/kgに急増しました。詰め込まれたローリングステップのレベルは0.018 mg/kgに減少しました。これは、AQ汚染物質の一部を運ぶ茶ジュースが失われたためかもしれません。ローリングステージの後、乾燥段階のレベルは0.027 mg/kgに増加しました。枯れ、緑色、固定、詰め込まれたローリングと乾燥において、PFSはそれぞれ2.81、1.32、5.66、0.78、および1.50でした。
異なる熱源を持つお茶製品でのAQの発生
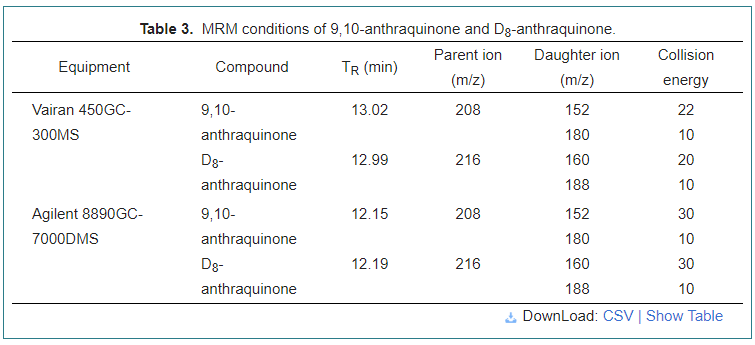
さまざまな熱源を持つお茶のAQ含有量の影響を判断するために、表2に示すように、電気を使用して電気を使用するのと比較して、電気を使用して最大AQレベルの0.064 mg/kgで、石炭を使用したことを示す、AQ Conticad by Contion by by by by by by by by by by by by by by by by by by by by by by by by by col col石炭のサンプルでは、35.0%の割合が観察されました。最も顕著なのは、電気の最低56.4%と7.7%で、最大含有量は0.020 mg/kgでした。
議論
2種類の熱源での処理中のPFSに基づいて、炭化と電気エネルギーの下での処理を伴う茶生産のAQレベルの増加につながった主なステップであることが、茶中のAQの含有量にわずかな影響を与えたことが明らかになりました。緑茶の加工中、石炭燃焼は電気加熱プロセスと比較して固定プロセスで多くの煙を生成し、スモークバーベキューサンプルの暴露プロセスと同様に、茶芽と茶撮影との接触からのAQ汚染物質の主な原因であることを示しています[25]。ローリング段階でのAQ含有量がわずかに増加すると、石炭燃焼によって引き起こされる煙が、固定段階でAQレベルに影響を与えただけでなく、大気沈着による加工環境でも影響を与えたことが示唆されました。石炭は、最初の乾燥と再乾燥の熱源としても使用されましたが、これら2つのステップでは、AQ含有量がわずかに増加するか、わずかに減少しました。これは、囲まれた熱風乾燥機が石炭燃焼によって引き起こされる煙からお茶を遠ざけたという事実によって説明されるかもしれません[26]。汚染源を決定するために、大気中のAQレベルを分析し、2つのワークショップ間に大きなギャップをもたらしました。これの主な理由は、固定、最初の乾燥段階、再乾燥段階で使用される石炭が、不完全な燃焼中にAQを生成することです。次に、これらのAQを石炭燃焼後に固体の小さな粒子に吸着し、空気中に分散し、ワークショップ環境でAQ汚染のレベルを上昇させました[15]。時間が経つにつれて、茶の特異的な表面積と吸着能力が大きいため、これらの微粒子は茶葉の表面に落ち着き、生産のAQの増加をもたらしました。したがって、石炭燃焼は、茶加工において過剰なAQ汚染につながる主要なルートであると考えられており、煙が汚染の原因となっています。
ウーロン茶加工に関しては、AQは両方の熱源で処理中に増加しましたが、2つの熱源の違いは有意でした。結果はまた、熱源としての石炭がAQレベルの上昇に大きな役割を果たし、固定はPFSに基づいてウーロン茶処理のAQ汚染を増加させる主なステップと見なされたことを示唆しました。天然ガス電気ハイブリッドを熱源として使用したウーロン茶加工中、AQレベルの傾向は0.005 mg/kg未満で停滞していました。これは、電気と天然ガスなどのクリーンエネルギーが加工からAQ汚染物質を生成するリスクを減らすことができることを示唆しています。
サンプリングテストに関して、結果は、石炭を電気ではなく熱源として使用すると、AQ汚染の状況が悪化したことを示しました。ただし、茶加工中に電気が最もきれいな熱源であることは明らかでしたが、熱源として電気を使用して茶製品にAQ汚染物質がまだありました。この状況は、以前に公開された研究とわずかに類似しているように見えますが、2つのアルケンとヒドロキノンおよびベンゾキノンの反応が潜在的な化学経路として示唆された[23]、この理由は今後の研究で調査されます。
結論
この作業では、GC-MS/MS分析方法の改善に基づいた比較実験によって、緑とウーロン茶のAQ汚染の可能な発生源が確認されました。私たちの調査結果は、高レベルのAQの主な汚染物質源が燃焼によって引き起こされる煙であり、加工段階に影響を与えただけでなく、ワークショップ環境にも影響を与えたことを直接支持しました。 AQのレベルの変化が目立たないローリング段階や枯れた段階とは異なり、固定などの石炭とfireの直接関与のある段階は、これらの段階での茶と煙の間の接触量によりAQ汚染が増加する主なプロセスです。したがって、天然ガスや電気などのきれいな燃料が、茶加工の熱源として推奨されました。さらに、実験結果は、燃焼によって生成される煙が存在しない場合、茶加工中にAQをトレースすることに寄与する他の要因がまだあることを示しましたが、将来の研究でさらに調査する必要があるワークショップでは、少量のAQも観察されました。
材料と方法
試薬、化学物質、材料
Anthraquinone Standard(99.0%)は、Ehrenstorfer GmbH Company博士(ドイツ、Augsburg)から購入しました。 D8-Anthraquinone内部標準(98.6%)は、C/D/N同位体(カナダ、ケベック)から購入しました。無水硫酸ナトリウム(Na2SO4)および硫酸マグネシウム(MGSO4)(上海、中国)。 Florisilは、Wenzhou Organic Chemical Company(Wenzhou、China)から供給されました。 Mircro-Glass Fiber Paper(90 mm)は、Ahlstrom-MunksjöCompany(フィンランドのヘルシンキ)から購入しました。
サンプル準備
緑茶のサンプルは、固定、転がり、最初の乾燥、再乾燥(囲まれた機器を使用)で処理され、ウーロン茶サンプルは枯れ、緑(揺れ葉が交互に繰り返され、固定、詰め込まれた転がり、乾燥で処理されました。徹底的な混合後、各ステップからのサンプルを100gで3回収集しました。すべてのサンプルは、さらなる分析のために-20°Cで保存されました。
空気サンプルは、中容量サンプラー(PTS-100、中国、青島青島電子機器会社)[27]を使用して、ガラス繊維紙(90 mm)で収集し、100 L/minで4時間走りました。
強化サンプルは、0.005 mg/kg、0.010 mg/kg、0.020 mg/kg、新鮮なティーシュート、0.005 mg/kg、0.020 mg/kg、ドライティーで0.050 mg/kg、0.012 mg/kg(0.5 µg/mg)、0.036/kg/k(1.5 µg/kg/k(0.012 mg/kg)で、0.020 mg/kg、0.050 mg/kg)で強化されたサンプルをスパイクしました。エアスマープル)、それぞれガラスろ紙用の0.072 mg/kg(エアサンプルの場合は3.0 µg/m3)。徹底的に揺れた後、すべてのサンプルを12時間放置し、その後抽出とクリーンアップステップを続けました。
水分含有量は、各ステップを混合した後、20 gのサンプルを摂取し、105°Cで1時間加熱し、重量を測定して3回繰り返し、平均値を摂取して加熱する前に重量で割ったことで得られました。
サンプルの抽出とクリーンアップ
TEAサンプル:TEAサンプルからのAQの抽出と精製は、Wang et al。の公開された方法に基づいて行われました。いくつかの適応がある[21]。簡単に言えば、1.5 gの茶サンプルを最初に30μLD8-AQ(2 mg/kg)と混合し、30分間放置し、その後1.5 mL脱イオン水とよく混合し、30分間放置しました。 N-ヘキサン中の15 mL 20%アセトンを茶サンプルに添加し、15分間超音波処理しました。次に、サンプルを1.0 g MGSO4で30秒間ボルテックスし、11,000 rpmで5分間遠心分離しました。 100 mlの梨型のフラスコに移動した後、10 mLの上部有機相を蒸発させて、37°Cで真空下でほぼ乾燥しました。 N-ヘキサン中の5 mL 2.5%アセトンは、浄化のために梨型のフラスコの抽出物を再分解しました。ガラスカラム(10 cm×0.8 cm)は、2 cm Na2SO4の2層の間のガラスウールと2Gフロリジルの上部から2Gフロリジルの上部から構成されていました。次に、N-ヘキサン中の5 mLの2.5%アセトンがカラムを事前に粉砕しました。再溶解溶液をロードした後、AQをN-ヘキサン中の5 mL、10 mL、10 mLの2.5%アセトンで3回溶出しました。結合された溶出物を梨型のフラスコに移し、37°Cで真空下でほぼ乾燥して蒸発させました。次に、乾燥残留物をヘキサン中の1 mLの2.5%アセトンで再構成し、その後0.22 µmの細孔サイズフィルターを介してろ過しました。次に、再構成された溶液を1:1の体積比でアセトニトリルと混合しました。揺れのステップに続いて、サブネイタントはGC-MS/MS分析に使用されました。
空気サンプル:18μlのD8-AQ(2 mg/kg)を滴下した繊維紙の半分を、N-ヘキサン中の15 mLの20%アセトンに浸し、15分間超音波処理しました。有機相を11,000 rpmで5分間遠心分離することにより分離し、上層全体を梨型のフラスコで除去しました。すべての有機相は、37°Cで真空下でほぼ乾燥して蒸発しました。ヘキサン中の5 mLの2.5%アセトンは、茶サンプルと同じ方法で精製のために抽出物を再溶解しました。
GC-MS/MS分析
Varian 300タンデム質量検出器(Varian、Walnut Creek、CA、USA)を備えたVarian 450ガスクロマトグラフを使用して、MS Workstationバージョン6.9.3ソフトウェアでAQ分析を実行しました。バリアン因子4キャピラリーカラムVF-5ms(30 m×0.25 mm×0.25μm)をクロマトグラフィー分離に使用しました。キャリアガスであるヘリウム(> 99.999%)は、アルゴンの衝突ガス(> 99.999%)で1.0 ml/minの一定流量に設定されました。オーブンの温度は80°Cから始まり、1分間保持されました。 15°C/minで240°Cに増加し、20°C/minで260°Cに達し、5分間保持しました。イオン源の温度は210°Cで、トランスファーライン温度は280°Cでした。注入量は1.0μLでした。 MRM条件を表3に示します。
Agilent 7000Dトリプル四重極質量分析計(Agilent、Stevens Creek、CA、USA)を装備したAgilent 8890ガスクロマトグラフを使用して、Masshunterバージョン10.1ソフトウェアで精製効果を分析しました。 Agilent J&W HP-5MS GCカラム(30 m×0.25 mm×0.25μm)をクロマトグラフィー分離に使用しました。キャリアガスであるヘリウム(> 99.999%)は、窒素の衝突ガス(> 99.999%)で2.25 mL/minの一定流量に設定されました。 EIイオン源の温度は、トランスファーライン温度と同じ280°Cで調整されました。オーブンの温度は80°Cから始まり、5分間保持されました。 15°C/minから240°Cまで上げてから、25°C/minで280°Cに達し、5分間維持しました。 MRM条件を表3に示します。
統計分析
新鮮な葉のAQ含有量は、処理中にAQレベルを比較および分析するために、水分含有量で除算することにより、乾物含有量に修正されました。
TEAサンプルのAQの変更は、Microsoft ExcelソフトウェアおよびIBM SPSS統計20で評価されました。
処理係数を使用して、茶加工中のAQの変化を説明しました。 PF = RL/RF。ここで、RFは処理ステップの前のAQレベルであり、RLは処理ステップ後のAQレベルです。 PFは、特定の処理ステップ中のAQ残差の減少(PF <1)または増加(PF> 1)を示します。
私は、次のように、マトリックスと溶媒中のキャリブレーションの勾配の比率に基づいて、分析機器に応答した減少(ME <1)または増加(ME> 1)を示しています。
me =(slopematrix/slopesolvent -1)×100%
Slopematrixがマトリックスに合わせた溶媒のキャリブレーション曲線の勾配である場合、Slopesolventは溶媒のキャリブレーション曲線の傾きです。
謝辞
この作業は、Z江省の科学技術主要プロジェクト(2015C12001)および中国国立科学財団(42007354)によってサポートされていました。
利益相反
著者は、利益相反がないと宣言しています。
権利と許可
著作権:©2022著者による。専用ライセンシーマキシマムアカデミックプレス、ジョージア州フェイエットビル。この記事は、Creative Commons Attribution License(CC by 4.0)の下で配布されるオープンアクセスの記事で、https://creativecommons.org/licenses/by/4.0/にアクセスしてください。
参照
[1] ITC。 2021年。統計の年次速報2021。https://inttea.com/publication/
[2] Hicks A. 2001。世界の茶生産とアジアの経済状況の産業への影響のレビュー。 Au Journal of Technology 5
Google Scholar
[3]魚類T、川中H、熊野Y、ヤグチY、トモムラM、他2014年。低温貯蔵プロセスを伴う緑茶における臭気剤化合物とその生化学形成の特性評価。 Food Chemistry 148:388-95 doi:10.1016/j.foodchem.2013.10.069
CrossRef Google Scholar
[4] Chen Z、Ruan J、Cai D、Zhang L.2007。TEA生態系とその制御における三桁汚染チェーン。 Scientia Agricula sinica 40:948-58
Google Scholar
[5] He H、Shi L、Yang G、You M、Vasseur L. 2020。茶プランテーションにおける土壌重金属および農薬残留物の生態学的リスク評価。農業10:47 doi:10.3390/Agriculture10020047
CrossRef Google Scholar
[6] Jin C、He Y、Zhang K、Zhou G、Shi J、他2005年。茶葉の鉛汚染とそれに影響する非エダフィ因子。 Chemosphere 61:726-32 doi:10.1016/j.chemosphere.2005.03.053
CrossRef Google Scholar
[7] Owuor Po、Obaga So、OthienoCo。1990。紅茶の化学組成に対する高度の影響。 Journal of the Science of Food and Agriculture 50:9-17 doi:10.1002/jsfa.2740500103
CrossRef Google Scholar
[8]ガルシア・ロンドニョ・VA、レイノソ・M、レスニク・S・2014年。食品添加物と汚染物質:パートB 7:247-53 DOI:10.1080/19393210.2014.919963
CrossRef Google Scholar
[9]石崎A、西野K、漢字N、ナリマツS、カタオカH. 2010年。2010年。 Journal of Chromatography A 1217:5555-63 doi:10.1016/j.chroma.2010.06.068
CrossRef Google Scholar
[10] Phan Thi La、Ngoc NT、Quynh NT、Thanh NV、Kim TTなど2020年。ベトナムの乾燥茶葉と茶注入における多環芳香族炭化水素(PAH):汚染レベルと食事リスク評価。環境地球化学と健康42:2853-63 doi:10.1007/s10653-020-00524-3
CrossRef Google Scholar
[11] Zelinkova Z、Wenzl T. 2015。食品中の16のEPA PAHの発生 - レビュー。多環芳香族化合物35:248-84 doi:10.1080/10406638.2014.918550
CrossRef Google Scholar
[12] Omodara NB、Olabemiwo om、Adedosu Ta。 2019年。fireと炭のスモークストックと猫の魚で形成されたPAHの比較。 American Journal of Food Science and Technology 7:86-93 doi:10.12691/ajfst-7-3-3
CrossRef Google Scholar
[13] Zou Ly、Zhang W、Atkiston S. 2003。オーストラリアのさまざまなfire種の燃焼からの多環芳香族炭化水素排出の特性評価。環境汚染124:283-89 doi:10.1016/s0269-7491(02)00460-8
CrossRef Google Scholar
[14] Charles GD、Bartels MJ、Zacharewski TR、Gollapudi BB、Frashour NLなど2000年。エストロゲン受容体-αレポーター遺伝子アッセイにおけるベンゾ[a]ピレンとそのヒドロキシル化代謝産物の活性。毒性科学55:320-26 doi:10.1093/toxsci/55.2.320
CrossRef Google Scholar
[15] Han Y、Chen Y、Ahmad S、Feng Y、Zhang F、他2018年。石炭燃焼からのPMおよび化学組成の高およびサイズ分解測定:EC形成プロセスへの影響。環境科学技術52:6676-85 doi:10.1021/acs.est.7b05786
CrossRef Google Scholar
[16] Khiadani(Hajian)M、Amin MM、Beik FM、Ebrahimi A、Farhadkhani M、et al。 2013年。イランでより多く使用されている8つのブランドの紅茶における多環芳香族炭化水素濃度の決定。 International Journal of Environmental Health Engineering 2:40 doi:10.4103/2277-9183.122427
CrossRef Google Scholar
[17]フィッツパトリックEM、ロスAB、ベイツJ、アンドリュースG、ジョーンズJM、他2007年。松の木材の燃焼からの酸素化種の放出と、すす形成との関係。プロセスの安全性と環境保護85:430-40 DOI:10.1205/PSEP07020
CrossRef Google Scholar
[18] Shen G、Tao S、Wang W、Yang Y、Ding J、et al。 2011年。屋内固形燃料燃焼からの酸素化多環式芳香族炭化水素の放出。環境科学技術45:3459-65 doi:10.1021/es104364t
CrossRef Google Scholar
[19]国際癌研究機関(IARC)、世界保健機関。 2014年。ディーゼルとガソリンエンジンの排気といくつかのニトロアレン。人間に対する発がん性リスクの評価に関する癌研究に関する国際研究機関。報告。 105:9
[20] de OliveiraGalvãoMF、De Oliveira Alves N、Ferreira PA、Caumo S、De Castro Vasconcellos P、et al。 2018年。ブラジルのアマゾン地域のバイオマス燃焼粒子:ニトロと酸素-PAHの変異原性効果と健康リスクの評価。環境汚染233:960-70 doi:10.1016/j.envpol.2017.09.068
CrossRef Google Scholar
[21] Wang X、Zhou L、Luo F、Zhang X、Sun Hなど2018。9,10-Anthraquinone茶プランテーションでの堆積物は、茶中の汚染の理由の1つかもしれません。食品化学244:254-59 doi:10.1016/j.foodchem.2017.09.123
CrossRef Google Scholar
[22] Anggraini T、Neswati、Nanda RF、Syukri D. 2020。インドネシアの黒茶処理中の9,10-アントラキノン汚染の同定。 Food Chemistry 327:127092 doi:10.1016/j.foodchem.2020.127092
CrossRef Google Scholar
[23] Zamora R、Hidalgo FJ。 2021年。カルボニルヒドロキノン/ベンゾキノン反応によるナフソキノンとアントラキノンの形成:茶中の9,10-アントラキノンの起源の潜在的な経路。 Food Chemistry 354:129530 doi:10.1016/j.foodchem.2021.129530
CrossRef Google Scholar
[24] Yang M、Luo F、Zhang X、Wang X、Sun Hなど2022年。茶植物におけるアントラセンの取り込み、転座、および代謝。総環境の科学821:152905 doi:10.1016/j.scitotenv.2021.152905
CrossRef Google Scholar
[25] Zastrow L、Schwind KH、SchwägeleF、Speer K.2019。Anthraquinone(atq)およびPolycycycic芳香族炭化水素(PAH)の内容に対する喫煙とバーベキューの影響。 Journal of Agricultural and Food Chemistry 67:13998-4004 doi:10.1021/acs.jafc.9b03316
CrossRef Google Scholar
[26] Fouillaud M、Caro Y、Venkatachalam M、Grondin I、DufosséL。2018。Anthraquinones。食品中のフェノール化合物:特性評価と分析、eds。 Leo Ml.vol。 9。ボカラトン:CRCプレス。 pp。130-70https://hal.univ-reunion.fr/hal-01657104
[27]Piñeiro-Iglesias M、López-Mahı́aP、Muniategui-Lorenzo S、Prada-Rodrı́guezD、Querol X、et al。 2003年。大気の粒子状物質のサンプルにおけるPAHと金属の同時決定のための新しい方法。大気環境37:4171-75 doi:10.1016/s1352-2310(03)00523-5
CrossRef Google Scholar
この記事について
この記事を引用してください
Yu J、Zhou L、Wang X、Yang M、Sun Hなど2022。9,10-Antraquinone汚染は、熱源として石炭を使用した茶処理における汚染。飲料工場研究2:8 doi:10.48130/bpr-2022-0008
投稿時間:5月9日 - 2022年