Abstrait
La 9,10-anthraquinone (AQ) est un contaminant présentant un risque cancérigène potentiel et présent dans le thé dans le monde entier. La limite maximale de résidus (LMR) d'AQ dans le thé fixée par l'Union européenne (UE) est de 0,02 mg/kg. Les sources possibles d'AQ dans le traitement du thé et les principales étapes de son apparition ont été étudiées sur la base d'une méthode analytique d'AQ modifiée et d'une analyse par chromatographie en phase gazeuse et spectrométrie de masse en tandem (GC-MS/MS). Par rapport à l'électricité comme source de chaleur dans la transformation du thé vert, l'AQ a augmenté de 4,3 à 23,9 fois dans la transformation du thé avec le charbon comme source de chaleur, dépassant largement 0,02 mg/kg, tandis que le niveau d'AQ dans l'environnement a triplé. La même tendance a été observée dans la transformation du thé oolong sous la chaleur du charbon. Les étapes de contact direct entre les feuilles de thé et les fumées, telles que la fixation et le séchage, sont considérées comme les principales étapes de la production d'AQ dans la transformation du thé. Les niveaux d'AQ ont augmenté avec l'augmentation du temps de contact, ce qui suggère que des niveaux élevés de polluant AQ dans le thé pourraient provenir des fumées provoquées par le charbon et la combustion. Quarante échantillons provenant de différents ateliers utilisant de l'électricité ou du charbon comme sources de chaleur ont été analysés, allant de 50,0 % à 85,0 % et de 5,0 % à 35,0 % pour la détection et le dépassement des taux d'AQ. De plus, la teneur maximale en AQ de 0,064 mg/kg a été observée dans le produit à base de thé avec du charbon comme source de chaleur, ce qui indique que les niveaux élevés de contamination par l'AQ dans les produits à base de thé sont probablement dus au charbon.
Mots clés : 9,10-Anthraquinone, Transformation du thé, Charbon, Source de contamination
INTRODUCTION
Le thé fabriqué à partir de feuilles de l'arbuste à feuilles persistantes Camellia sinensis (L.) O. Kuntze est l'une des boissons les plus populaires au monde en raison de son goût rafraîchissant et de ses bienfaits pour la santé. En 2020, la production mondiale de thé a augmenté pour atteindre 5 972 millions de tonnes, soit un doublement au cours des 20 dernières années[1]. Selon différentes méthodes de transformation, il existe six principaux types de thé, dont le thé vert, le thé noir, le thé noir, le thé oolong, le thé blanc et le thé jaune[2,3]. Pour garantir la qualité et la sécurité des produits, il est très important de surveiller les niveaux de polluants et d’en définir l’origine.
L'identification des sources de contaminants, tels que les résidus de pesticides, les métaux lourds et d'autres polluants tels que les hydrocarbures aromatiques polycycliques (HAP), constitue la première étape du contrôle de la pollution. La pulvérisation directe de produits chimiques synthétiques dans les plantations de thé, ainsi que la dérive de l'air provoquée par les opérations à proximité des plantations de thé, sont la principale source de résidus de pesticides dans le thé[4]. Les métaux lourds peuvent s’accumuler dans le thé et entraîner une toxicité, principalement due au sol, aux engrais et à l’atmosphère[5−7]. Quant aux autres pollutions apparaissant de manière inattendue dans le thé, elles étaient assez difficiles à identifier en raison des procédures complexes de la chaîne de production du thé, notamment la plantation, la transformation, le conditionnement, le stockage et le transport. Les HAP présents dans le thé provenaient du dépôt des gaz d'échappement des véhicules et de la combustion des combustibles utilisés lors du traitement des feuilles de thé, comme le bois de chauffage et le charbon[8−10].
Lors de la combustion du charbon et du bois de chauffage, des polluants tels que des oxydes de carbone se forment[11]. En conséquence, il est possible que des résidus de ces polluants mentionnés ci-dessus se retrouvent dans les produits transformés, tels que les céréales, le bouillon fumé et le poisson-chat, à haute température, ce qui constitue une menace pour la santé humaine[12,13]. Les HAP provoqués par la combustion proviennent de la volatilisation des HAP contenus dans les carburants eux-mêmes, de la décomposition à haute température des composés aromatiques et de la réaction composée entre radicaux libres[14]. La température, la durée et la teneur en oxygène de la combustion sont des facteurs importants qui affectent la conversion des HAP. Avec l'augmentation de la température, la teneur en HAP a d'abord augmenté puis diminué, et la valeur maximale s'est produite à 800 °C ; La teneur en HAP a fortement diminué pour suivre l'augmentation du temps de combustion lorsqu'elle était inférieure à une limite appelée « temps limite ». Avec l'augmentation de la teneur en oxygène dans l'air de combustion, les émissions de HAP ont diminué de manière significative, mais une oxydation incomplète produirait des OPAH et d'autres dérivés.[15 −17].
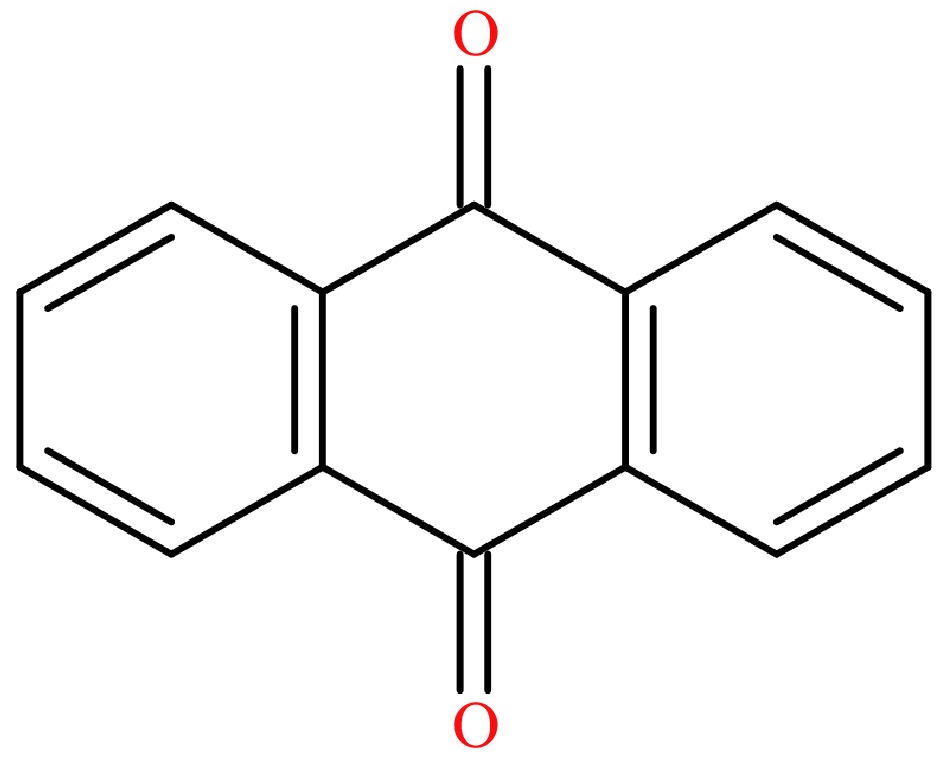
La 9,10-anthraquinone (AQ, CAS : 84-65-1, Fig. 1), un dérivé oxygéné des HAP[18], se compose de trois cycles condensés. Il a été répertorié comme cancérogène possible (groupe 2B) par le Centre international de recherche sur le cancer en 2014[19]. L'AQ peut empoisonner le complexe de clivage de la topoisomérase II et inhiber l'hydrolyse de l'adénosine triphosphate (ATP) par l'ADN topoisomérase II, provoquant des cassures double brin de l'ADN, ce qui signifie qu'une exposition à long terme dans un environnement contenant de l'AQ et un contact direct avec un niveau élevé d'AQ peut entraîner des dommages à l’ADN, des mutations et augmenter le risque de cancer[20]. En raison des effets négatifs sur la santé humaine, la limite maximale de résidus (LMR) AQ de 0,02 mg/kg a été fixée dans le thé par l'Union européenne. Selon nos études précédentes, les dépôts d'AQ ont été suggérés comme étant la principale source lors de la plantation de thé[21]. En outre, sur la base des conséquences expérimentales sur la transformation du thé vert et noir indonésien, il est évident que le niveau d'AQ a changé de manière significative et la fumée provenant des équipements de transformation a été suggérée comme l'une des principales raisons[22]. Cependant, l’origine précise de l’AQ dans la transformation du thé est restée insaisissable, bien que certaines hypothèses sur la voie chimique de l’AQ aient été suggérées[23,24], indiquant qu’il est extrêmement important de déterminer les facteurs cruciaux affectant le niveau d’AQ dans la transformation du thé.
Figure 1. La formule chimique de l'AQ.
Compte tenu des recherches sur la formation d'AQ lors de la combustion du charbon et de la menace potentielle des combustibles dans le traitement du thé, une expérience comparative a été menée pour expliquer l'effet du traitement des sources de chaleur sur l'AQ dans le thé et l'air, une analyse quantitative sur les changements de la teneur en AQ à différentes étapes de traitement, ce qui est utile pour confirmer l'origine précise, le modèle d'occurrence et le degré de pollution par l'AQ dans le traitement du thé.
RÉSULTATS
Validation de la méthode
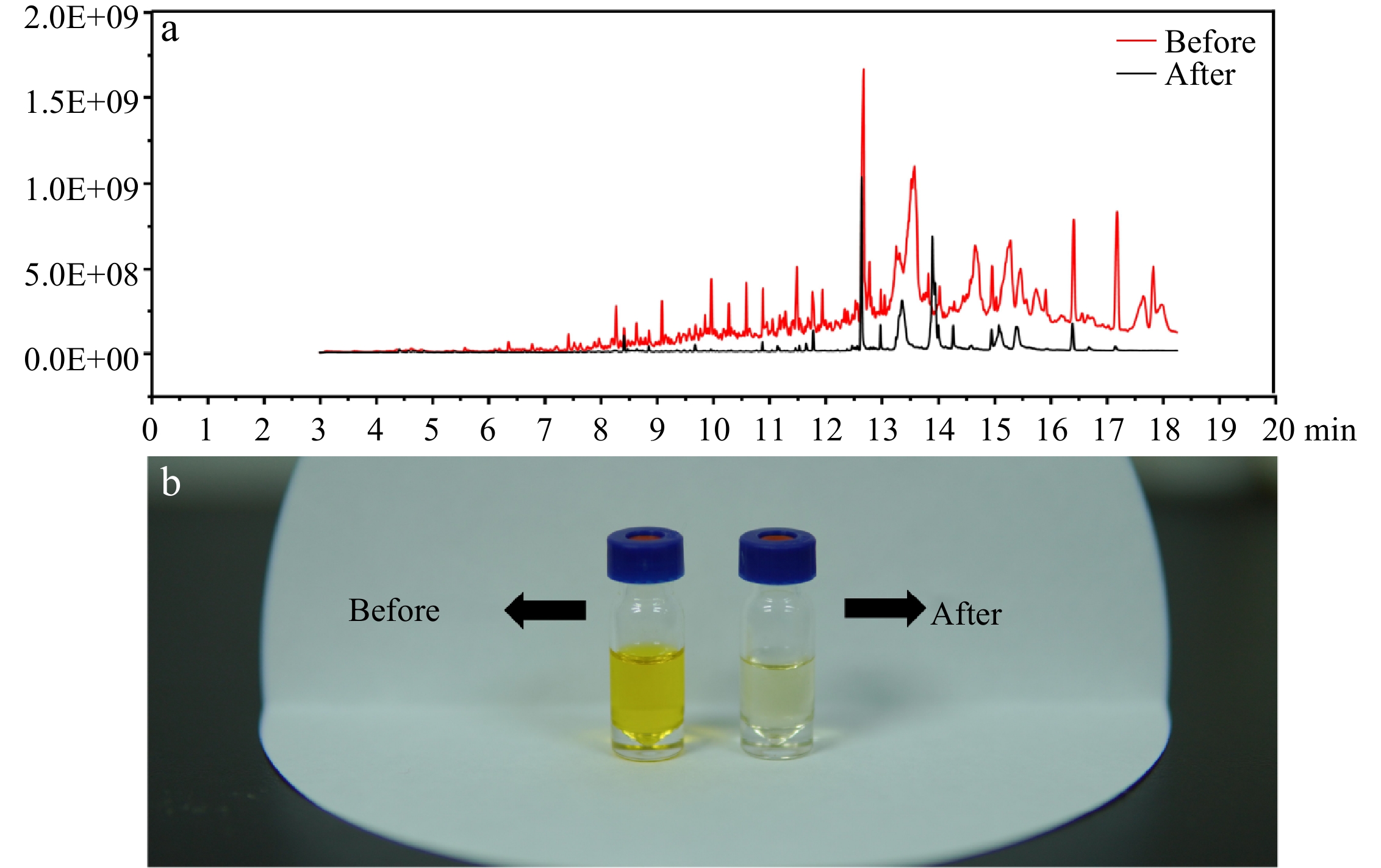
Par rapport à notre étude précédente [21], une procédure d’extraction liquide-liquide a été combinée avant injection en GC-MS/MS afin d’améliorer la sensibilité et de maintenir les relevés instrumentaux. Sur la figure 2b, la méthode améliorée a montré une amélioration significative de la purification de l'échantillon, le solvant étant devenu de couleur plus claire. Sur la figure 2a, un spectre de balayage complet (50 à 350 m/z) montre qu'après purification, la ligne de base du spectre MS est évidemment réduite et moins il y a de pics chromatographiques disponibles, ce qui indique qu'un grand nombre de composés interférents ont été éliminés après l'élimination. extraction liquide-liquide.
Figure 2. (a) Spectre d'analyse complet de l'échantillon avant et après la purification. (b) L'effet purifiant de la méthode améliorée.
La validation de la méthode, y compris la linéarité, la récupération, la limite de quantification (LOQ) et l'effet de matrice (ME), est présentée dans le tableau 1. Il est satisfaisant d'obtenir la linéarité avec le coefficient de détermination (r2) supérieur à 0,998, qui variait de 0,005 à 0,2 mg/kg dans la matrice de thé et le solvant acétonitrile, et dans l'échantillon d'air avec une plage de 0,5 à 8 μg/m3.
La récupération de l'AQ a été évaluée à trois concentrations enrichies entre les concentrations mesurées et réelles dans le thé sec (0,005, 0,02, 0,05 mg/kg), les pousses de thé fraîches (0,005, 0,01, 0,02 mg/kg) et l'échantillon d'air (0,5, 1,5, 3 µg/m3). La récupération de l'AQ dans le thé variait de 77,78 % à 113,02 % dans le thé sec et de 96,52 % à 125,69 % dans les pousses de thé, avec un % RSD inférieur à 15 %. La récupération de l'AQ dans les échantillons d'air variait entre 78,47 % et 117,06 %, avec un pourcentage de RSD inférieur à 20 %. La concentration la plus faible a été identifiée comme LOQ, soit 0,005 mg/kg, 0,005 mg/kg et 0,5 μg/m³ dans les pousses de thé, le thé sec et les échantillons d'air, respectivement. Comme indiqué dans le tableau 1, la matrice de thé sec et de pousses de thé a légèrement augmenté la réponse AQ, conduisant à une EM de 109,0 % et 110,9 %. Quant à la matrice d'échantillons d'air, l'EM était de 196,1 %.
Les niveaux d'AQ pendant le traitement du thé vert
Dans le but de découvrir les effets de différentes sources de chaleur sur le thé et l'environnement de transformation, un lot de feuilles fraîches a été divisé en deux groupes spécifiques et traité séparément dans deux ateliers de transformation de la même entreprise. Un groupe était approvisionné en électricité et l'autre en charbon.
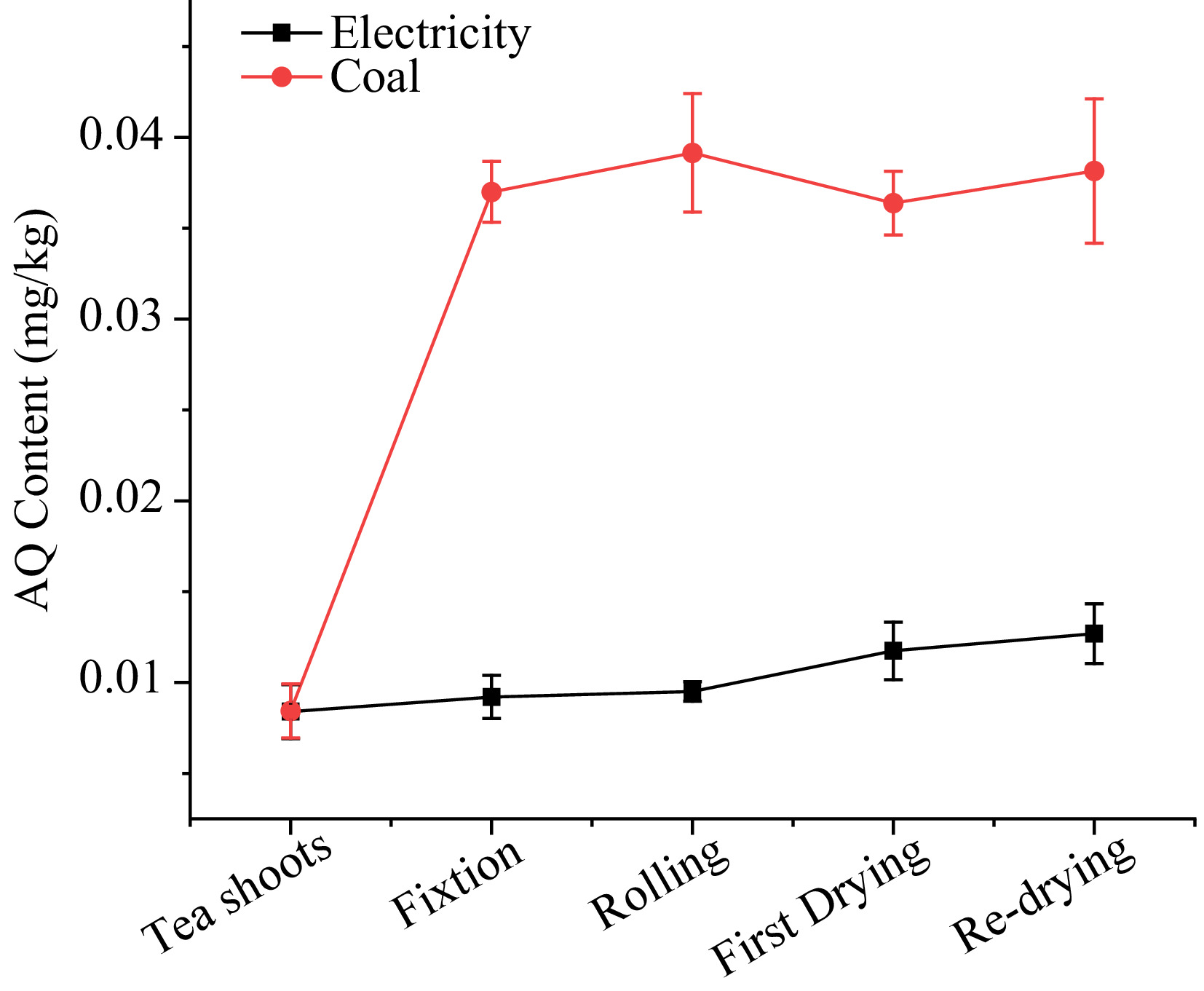
Comme le montre la figure 3, le niveau d'AQ avec l'électricité comme source de chaleur variait de 0,008 à 0,013 mg/kg. Au cours du processus de fixation, le dessèchement des feuilles de thé provoqué par le traitement dans un pot à haute température a entraîné une augmentation de 9,5 % de l'AQ. Ensuite, le niveau d’AQ est resté pendant le processus de laminage malgré la perte de jus, ce qui suggère que les processus physiques pourraient ne pas affecter le niveau d’AQ lors du traitement du thé. Après les premières étapes de séchage, le niveau d'AQ a légèrement augmenté de 0,010 à 0,012 mg/kg, puis a continué à augmenter jusqu'à 0,013 mg/kg jusqu'à la fin du nouveau séchage. Les PF, qui montraient de manière significative la variation à chaque étape, étaient respectivement de 1,10, 1,03, 1,24 et 1,08 pour la fixation, le laminage, le premier séchage et le re-séchage. Les résultats des PF suggèrent que le traitement sous énergie électrique avait un léger effet sur les niveaux d'AQ dans le thé.
Figure 3. Le niveau d'AQ lors du traitement du thé vert avec de l'électricité et du charbon comme sources de chaleur.
Dans le cas du charbon comme source de chaleur, la teneur en AQ a fortement augmenté au cours du traitement du thé, passant de 0,008 à 0,038 mg/kg. L'AQ de 338,9 % a augmenté lors de la procédure de fixation, atteignant 0,037 mg/kg, ce qui dépassait de loin la LMR de 0,02 mg/kg fixée par l'Union européenne. Pendant la phase de roulage, le niveau d'AQ a encore augmenté de 5,8 % malgré l'éloignement de la machine de fixation. Lors du premier séchage et du re-séchage, la teneur en AQ a peu augmenté ou a légèrement diminué. Les PF utilisant le charbon comme source de chaleur lors de la fixation, du premier séchage par laminage et du re-séchage étaient respectivement de 4,39, 1,05, 0,93 et 1,05.
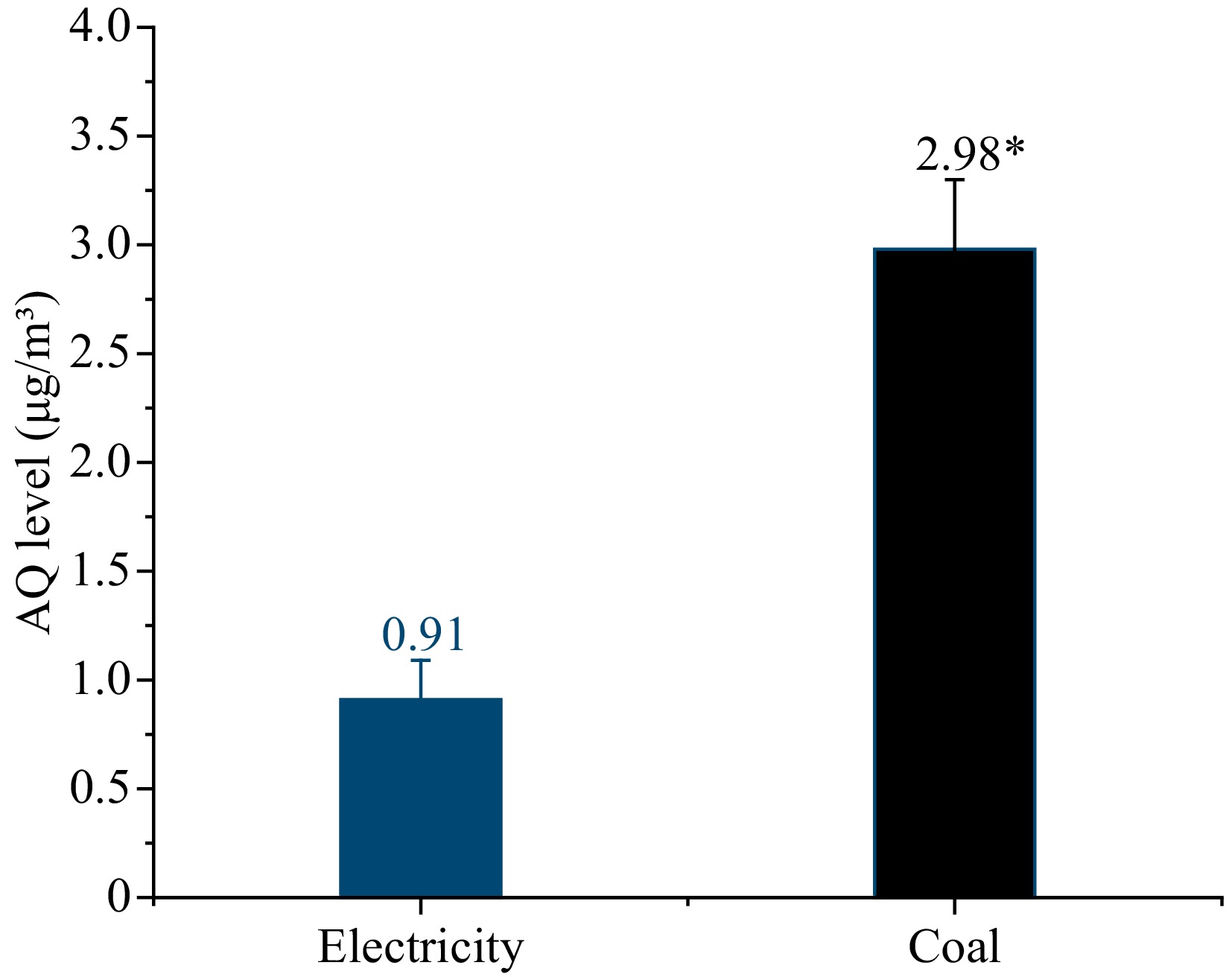
Pour déterminer davantage la relation entre la combustion du charbon et la pollution par l'AQ, les particules en suspension (PM) dans l'air des ateliers sous les deux sources de chaleur ont été collectées pour évaluation de l'air, comme le montre la figure 4. Le niveau d'AQ des PM avec le charbon comme la source de chaleur était de 2,98 μg/m3, ce qui était plus de trois fois supérieur à celui de l'électricité de 0,91 μg/m3.
Figure 4. Les niveaux d'AQ dans l'environnement avec l'électricité et le charbon comme source de chaleur. * Indique des différences significatives dans les niveaux d'AQ dans les échantillons (p < 0,05).
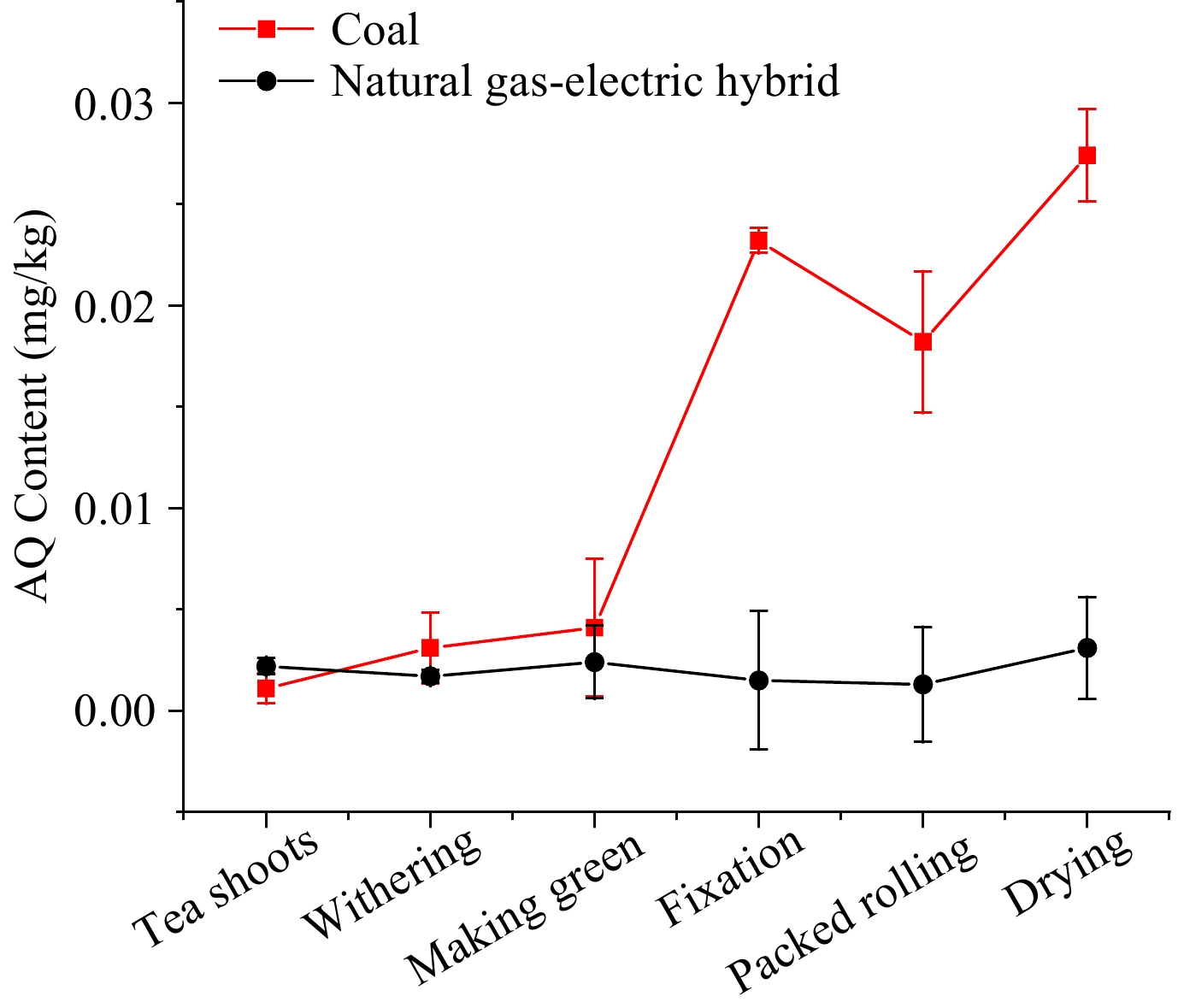
Les niveaux d'AQ lors de la transformation du thé oolong Le thé oolong, principalement produit au Fujian et à Taiwan, est une sorte de thé partiellement fermenté. Pour déterminer plus en détail les principales étapes de l'augmentation du niveau d'AQ et les effets des différents combustibles, le même lot de feuilles fraîches a été transformé en thé oolong avec du charbon et un hybride gaz naturel-électricité comme sources de chaleur, simultanément. Les niveaux d'AQ dans le traitement du thé oolong utilisant différentes sources de chaleur sont présentés dans la figure 5. Pour le traitement du thé oolong avec un hybride gaz naturel-électricité, la tendance du niveau d'AQ stagnait en dessous de 0,005 mg/kg, ce qui était similaire à celui du thé vert. avec l'électricité.
Figure 5. Niveau d'AQ lors du traitement du thé oolong avec un mélange gaz naturel-électricité et du charbon comme source de chaleur.
Avec le charbon comme source de chaleur, les niveaux d'AQ dans les deux premières étapes, flétrissement et verdissement, étaient essentiellement les mêmes qu'avec un mélange gaz naturel-électricité. Cependant, les procédures ultérieures jusqu'à la fixation ont montré que l'écart s'est élargi progressivement, auquel cas le niveau d'AQ est passé de 0,004 à 0,023 mg/kg. Le niveau lors de l'étape de laminage emballé a diminué à 0,018 mg/kg, ce qui peut être dû à la perte de jus de thé emportant certains des contaminants AQ. Après l'étape de laminage, la concentration dans l'étape de séchage a augmenté jusqu'à 0,027 mg/kg. Pour le flétrissement, la mise au vert, la fixation, le laminage emballé et le séchage, les PF étaient respectivement de 2,81, 1,32, 5,66, 0,78 et 1,50.
L'apparition de l'AQ dans les produits à base de thé avec différentes sources de chaleur
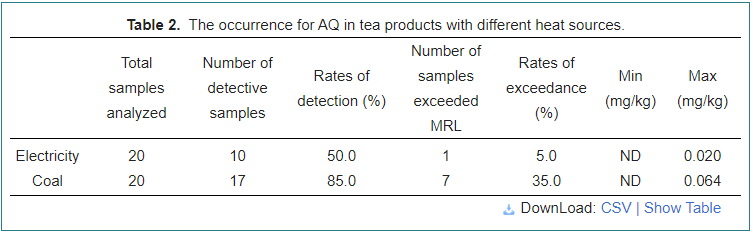
Pour déterminer les effets sur la teneur en AQ du thé avec différentes sources de chaleur, 40 échantillons de thé provenant d'ateliers de thé utilisant l'électricité ou le charbon comme source de chaleur ont été analysés, comme le montre le tableau 2. Par rapport à l'utilisation de l'électricité comme source de chaleur, le charbon avait le plus taux de détection (85,0 %) avec un niveau AQ maximum de 0,064 mg/kg, indiquant qu'il était facile de provoquer un contaminant AQ par les fumées produites par la combustion du charbon, et un taux de 35,0 % a été observé dans des échantillons de charbon. De manière plus frappante, l'électricité présentait les taux de détection et de dépassement les plus bas, respectivement de 56,4 % et 7,7 %, avec une teneur maximale de 0,020 mg/kg.
DISCUSSION
Sur la base des PF lors du traitement avec les deux types de sources de chaleur, il était clair que la fixation était l'étape principale qui conduisait à l'augmentation des niveaux d'AQ dans la production de thé avec du charbon et que le traitement sous énergie électrique avait un léger effet sur la teneur en AQ. dans le thé. Au cours du traitement du thé vert, la combustion du charbon a produit beaucoup de fumées lors du processus de fixation par rapport au processus de chauffage électrique, ce qui indique que les fumées étaient peut-être la principale source de polluants AQ provenant du contact instantané avec les pousses de thé lors du traitement du thé, similaire au processus d'exposition dans les échantillons de barbecue fumé[25]. La légère augmentation de la teneur en AQ au cours de l'étape de laminage suggère que les fumées provoquées par la combustion du charbon affectent non seulement le niveau d'AQ pendant l'étape de fixation, mais également dans l'environnement de traitement en raison des dépôts atmosphériques. Des charbons ont également été utilisés comme source de chaleur lors du premier séchage et du re-séchage, mais au cours de ces deux étapes, la teneur en AQ a légèrement augmenté ou diminué légèrement. Cela peut s'expliquer par le fait que le séchoir à vent chaud fermé gardait le thé à l'écart des fumées provoquées par la combustion du charbon[26]. Afin de déterminer la source du polluant, les niveaux d'AQ dans l'atmosphère ont été analysés, entraînant un écart important entre les deux ateliers. La principale raison en est que le charbon utilisé dans les étapes de fixation, de premier séchage et de re-séchage générerait de l'AQ lors d'une combustion incomplète. Ces AQ étaient ensuite adsorbées dans les petites particules de solides après la combustion du charbon et dispersées dans l'air, élevant les niveaux de pollution par l'AQ dans l'environnement de l'atelier[15]. Au fil du temps, en raison de la grande surface spécifique et de la capacité d’adsorption du thé, ces particules se sont ensuite déposées à la surface des feuilles de thé, entraînant une augmentation de la QA dans la production. Par conséquent, on pensait que la combustion du charbon était la principale voie menant à une contamination excessive par l’AQ lors de la transformation du thé, les fumées étant la source de pollution.
En ce qui concerne le traitement du thé oolong, l'AQ a augmenté lors du traitement avec les deux sources de chaleur, mais la différence entre les deux sources de chaleur était significative. Les résultats suggèrent également que le charbon en tant que source de chaleur joue un rôle majeur dans l'augmentation du niveau d'AQ, et que la fixation est considérée comme l'étape principale de l'augmentation de la contamination par l'AQ dans le traitement du thé oolong basé sur les PF. Au cours du traitement du thé oolong avec un hybride gaz naturel-électricité comme source de chaleur, la tendance du niveau d'AQ stagnait en dessous de 0,005 mg/kg, ce qui était similaire à celui du thé vert avec de l'électricité, ce qui suggère que l'énergie propre, comme l'électricité et l'énergie naturelle. gazeux, peut diminuer le risque de production de contaminants AQ lors du traitement.
Quant aux tests d'échantillonnage, les résultats ont montré que la situation de contamination par l'AQ était pire lors de l'utilisation du charbon comme source de chaleur plutôt que de l'électricité, ce qui pourrait être dû aux fumées de combustion du charbon entrant en contact avec les feuilles de thé et persistant sur le lieu de travail. Cependant, même s'il était évident que l'électricité était la source de chaleur la plus propre pendant le traitement du thé, il y avait encore des contaminants AQ dans les produits à base de thé utilisant l'électricité comme source de chaleur. La situation semble légèrement similaire aux travaux publiés précédemment dans lesquels la réaction des 2-alcènes avec les hydroquinones et les benzoquinones a été suggérée comme voie chimique potentielle[23], les raisons de cette situation seront étudiées dans des recherches futures.
CONCLUSIONS
Dans ce travail, les sources possibles de pollution AQ dans le thé vert et le thé oolong ont été confirmées par des expériences comparatives basées sur des méthodes analytiques GC-MS/MS améliorées. Nos résultats confirment directement que la principale source de polluants à l'origine de niveaux élevés d'AQ était les fumées provoquées par la combustion, qui affectaient non seulement les étapes de traitement, mais également l'environnement des ateliers. Contrairement aux étapes de roulage et de flétrissement, où les changements du niveau d'AQ étaient discrets, les étapes impliquant directement le charbon et le bois de chauffage, comme la fixation, sont le principal processus dans lequel la contamination par l'AQ a augmenté en raison de la quantité de contact entre le thé. et des fumées pendant ces étapes. Par conséquent, des combustibles propres tels que le gaz naturel et l’électricité ont été recommandés comme source de chaleur dans le traitement du thé. De plus, les résultats expérimentaux ont également montré qu'en l'absence de fumées générées par la combustion, d'autres facteurs contribuaient encore à la trace d'AQ pendant le traitement du thé, tandis que de petites quantités d'AQ ont également été observées dans l'atelier avec des carburants propres, qui devraient être étudiés plus en détail. dans les recherches futures.
MATÉRIELS ET MÉTHODES
Réactifs, produits chimiques et matériaux
L'étalon d'anthraquinone (99,0 %) a été acheté auprès de la société Dr. Ehrenstorfer GmbH (Augsbourg, Allemagne). L'étalon interne D8-Anthraquinone (98,6 %) a été acheté auprès de C/D/N Isotopes (Québec, Canada). Sulfate de sodium anhydre (Na2SO4) et sulfate de magnésium (MgSO4) (Shanghai, Chine). Florisil a été fourni par Wenzhou Organic Chemical Company (Wenzhou, Chine). Le papier micro-fibre de verre (90 mm) a été acheté auprès de la société Ahlstrom-munksjö (Helsinki, Finlande).
Préparation des échantillons
Les échantillons de thé vert ont été traités par fixation, laminage, premier séchage et re-séchage (à l'aide d'un équipement fermé), tandis que les échantillons de thé oolong ont été traités par flétrissement, rendu vert (basculement et feuilles fraîches debout en alternance), fixation, roulage emballé et séchage. Des échantillons de chaque étape ont été collectés trois fois à raison de 100 g après un mélange minutieux. Tous les échantillons ont été conservés à -20 ° C pour une analyse plus approfondie.
Des échantillons d'air ont été collectés sur du papier en fibre de verre (90 mm) à l'aide d'échantillonneurs de volume moyen (PTS-100, Qingdao Laoshan Electronic Instrument Company, Qingdao, Chine) [27], fonctionnant à 100 L/min pendant 4 h.
Les échantillons enrichis ont été enrichis avec de l'AQ à 0,005 mg/kg, 0,010 mg/kg, 0,020 mg/kg pour les pousses de thé fraîches, à 0,005 mg/kg, 0,020 mg/kg, 0,050 mg/kg pour le thé sec et à 0,012 mg/kg. (0,5 µg/m3 pour échantillon d'air), 0,036 mg/kg (1,5 µg/m3 pour l'échantillon d'air), 0,072 mg/kg (3,0 µg/m3 pour l'échantillon d'air) pour le papier filtre en verre, respectivement. Après avoir soigneusement agité, tous les échantillons ont été laissés pendant 12 h, suivis d'étapes d'extraction et de nettoyage.
La teneur en humidité a été obtenue en prélevant 20 g de l'échantillon après avoir mélangé chaque étape, en chauffant à 105 ° C pendant 1 h, puis en pesant et en répétant trois fois et en prenant la valeur moyenne et en la divisant par le poids avant le chauffage.
Extraction et nettoyage des échantillons
Échantillon de thé : L'extraction et la purification de l'AQ à partir d'échantillons de thé ont été réalisées sur la base de la méthode publiée par Wang et al. avec plusieurs adaptations[21]. En bref, 1,5 g d'échantillons de thé ont d'abord été mélangés avec 30 μL de D8-AQ (2 mg/kg) et laissés au repos pendant 30 min, puis bien mélangés avec 1,5 ml d'eau déminéralisée et laissés au repos pendant 30 min. 15 ml d'acétone à 20 % dans du n-hexane ont été ajoutés aux échantillons de thé et soniqués pendant 15 min. Ensuite, les échantillons ont été vortexés avec 1,0 g de MgSO4 pendant 30 s et centrifugés pendant 5 min à 11 000 tr/min. Après avoir été transférés dans des flacons en forme de poire de 100 ml, 10 ml de la phase organique supérieure ont été évaporés presque à sec sous vide à 37 °C. 5 ml d'acétone à 2,5 % dans du n-hexane ont dissous l'extrait dans des flacons en forme de poire pour purification. La colonne de verre (10 cm × 0,8 cm) était constituée de bas en haut de laine de verre et de 2 g de florisil, placé entre deux couches de 2 cm de Na2SO4. Ensuite, 5 ml d'acétone à 2,5 % dans du n-hexane ont prélavé la colonne. Après avoir chargé la solution redissoute, l'AQ a été éluée trois fois avec 5 ml, 10 ml, 10 ml d'acétone à 2,5 % dans du n-hexane. Les éluats combinés ont été transférés dans des flacons en forme de poire et évaporés presque à sec sous vide à 37 °C. Le résidu séché a ensuite été reconstitué avec 1 ml d'acétone à 2,5 % dans de l'hexane, suivi d'une filtration à travers un filtre de taille de pores de 0,22 µm. Ensuite, la solution reconstituée a été mélangée avec de l'acétonitrile dans un rapport volumique de 1:1. Après l’étape d’agitation, le sous-nageant a été utilisé pour l’analyse GC-MS/MS.
Échantillon d'air : La moitié du papier fibreux, égoutté avec 18 μL de d8-AQ (2 mg/kg), a été immergé dans 15 mL d'acétone à 20 % dans du n-hexane, puis soniqué pendant 15 min. La phase organique a été séparée par centrifugation à 11 000 tr/min pendant 5 min et la totalité de la couche supérieure a été éliminée dans un flacon en forme de poire. Toutes les phases organiques ont été évaporées presque à sec sous vide à 37 °C. 5 mL d'acétone à 2,5 % dans l'hexane ont redissous les extraits pour purification de la même manière que dans les échantillons de thé.
Analyse GC-MS/MS
Le chromatographe en phase gazeuse Varian 450 équipé du détecteur de masse tandem Varian 300 (Varian, Walnut Creek, Californie, États-Unis) a été utilisé pour effectuer l'analyse AQ avec le logiciel MS WorkStation version 6.9.3. La colonne capillaire Varian Factor Four VF-5ms (30 m × 0,25 mm × 0,25 µm) a été utilisée pour la séparation chromatographique. Le gaz vecteur, l'hélium (> 99,999 %), a été réglé à un débit constant de 1,0 ml/min avec du gaz de collision d'argon (> 99,999 %). La température du four a démarré à 80 °C et s'est maintenue pendant 1 min ; augmenté à 15 °C/min jusqu'à 240 °C, puis atteint 260 °C à 20 °C/min et maintenu pendant 5 min. La température de la source d'ions était de 210 °C, ainsi que la température de la ligne de transfert de 280 °C. Le volume d'injection était de 1,0 µL. Les conditions MRM sont présentées dans le tableau 3.
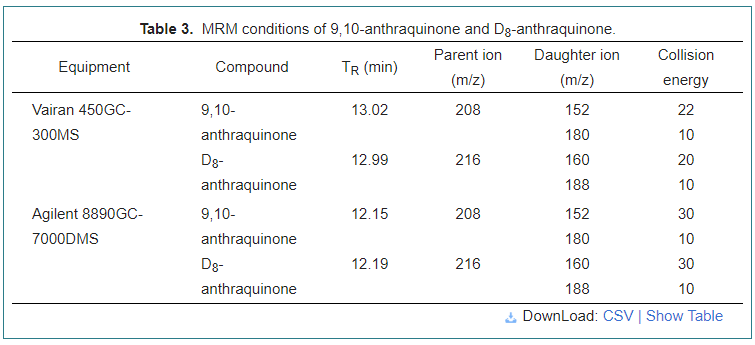
Le chromatographe en phase gazeuse Agilent 8890 équipé du spectromètre de masse triple quadripôle Agilent 7000D (Agilent, Stevens Creek, Californie, États-Unis) a été utilisé pour analyser l'effet de purification avec le logiciel MassHunter version 10.1. La colonne GC Agilent J&W HP-5 ms (30 m × 0,25 mm × 0,25 μm) a été utilisée pour la séparation chromatographique. Le gaz vecteur, l'hélium (> 99,999 %), a été réglé à un débit constant de 2,25 ml/min avec un gaz de collision constitué d'azote (> 99,999 %). La température de la source d'ions EI a été ajustée à 280 ° C, identique à la température de la ligne de transfert. La température du four a commencé à 80 °C et a été maintenue pendant 5 minutes ; augmenté de 15 °C/min jusqu'à 240 °C, puis atteint 280 °C à 25 °C/min et maintenu pendant 5 min. Les conditions MRM sont présentées dans le tableau 3.
Analyse statistique
La teneur en AQ des feuilles fraîches a été corrigée par rapport à la teneur en matière sèche en divisant par la teneur en humidité afin de comparer et d'analyser les niveaux d'AQ pendant le traitement.
Les changements d'AQ dans les échantillons de thé ont été évalués avec le logiciel Microsoft Excel et IBM SPSS Statistics 20.
Le facteur de transformation a été utilisé pour décrire les changements de l'AQ pendant le traitement du thé. PF = Rl/Rf, où Rf est le niveau AQ avant l'étape de traitement et Rl est le niveau AQ après l'étape de traitement. PF indique une diminution (PF < 1) ou une augmentation (PF > 1) de l'AQ résiduelle au cours d'une étape de traitement spécifique.
ME indique une diminution (ME < 1) ou une augmentation (ME > 1) en réponse aux instruments analytiques, qui est basée sur le rapport des pentes d'étalonnage dans la matrice et le solvant comme suit :
ME = (matrice de pente/solvant de pente − 1) × 100 %
Où pentematrix est la pente de la courbe d'étalonnage dans le solvant adapté à la matrice, pentesolvant est la pente de la courbe d'étalonnage dans le solvant.
REMERCIEMENTS
Ce travail a été soutenu par le projet majeur de science et technologie dans la province du Zhejiang (2015C12001) et par la Fondation nationale des sciences de Chine (42007354).
Conflit d'intérêt
Les auteurs déclarent qu'ils n'ont aucun conflit d'intérêts.
Droits et autorisations
Copyright : © 2022 par le(s) auteur(s). Titulaire exclusif de la licence Maximum Academic Press, Fayetteville, GA. Cet article est un article en libre accès distribué sous licence Creative Commons Attribution (CC BY 4.0), visitez https://creativecommons.org/licenses/by/4.0/.
RÉFÉRENCES
[1] CTI. 2021. Bulletin annuel de statistiques 2021. https://inttea.com/publication/
[2] Hicks A. 2001. Examen de la production mondiale de thé et de l'impact sur l'industrie de la situation économique asiatique. Journal de technologie de l'UA 5
Google Scholar
[3] Katsuno T, Kasuga H, Kusano Y, Yaguchi Y, Tomomura M et al. 2014. Caractérisation des composés odorants et de leur formation biochimique dans le thé vert avec un procédé de stockage à basse température. Chimie alimentaire 148 : 388−95 doi : 10.1016/j.foodchem.2013.10.069
CrossRef Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Chaîne de pollution tridimensionnelle dans l'écosystème du thé et son contrôle. Scientia Agricultura Sinica 40 : 948−58
Google Scholar
[5] He H, Shi L, Yang G, You M, Vasseur L. 2020. Évaluation des risques écologiques liés aux métaux lourds du sol et aux résidus de pesticides dans les plantations de thé. Agriculture 10:47 doi: 10.3390/agriculture10020047
CrossRef Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J et al. 2005. Contamination au plomb dans les feuilles de thé et facteurs non édaphiques qui l'affectent. Chemosphère 61 : 726−32 est ce que je : 10.1016/j.chemosphere.2005.03.053
CrossRef Google Scholar
[7] Owuor PO, Obaga SO, Othieno CO. 1990. Les effets de l'altitude sur la composition chimique du thé noir. Journal de la science de l'alimentation et de l'agriculture 50:9−17 doi : 10.1002/jsfa.2740500103
CrossRef Google Scholar
[8] Garcia Londoño VA, Reynoso M, Resnik S. 2014. Hydrocarbures aromatiques polycycliques (HAP) dans le yerba mate (Ilex paraguariensis) du marché argentin. Additifs alimentaires et contaminants : Partie B 7:247−53 doi : 10.1080/19393210.2014.919963
CrossRef Google Scholar
[9] Ishizaki A, Saito K, Hanioka N, Narimatsu S, Kataoka H. 2010. Détermination des hydrocarbures aromatiques polycycliques dans des échantillons alimentaires par microextraction automatisée en phase solide en tube couplée à une détection par chromatographie liquide-fluorescence haute performance . Journal of Chromatography A 1217 : 5555−63 est ce que je : 10.1016/j.chroma.2010.06.068
CrossRef Google Scholar
[10] Phan Thi LA, Ngoc NT, Quynh NT, Thanh NV, Kim TT et al. 2020. Hydrocarbures aromatiques polycycliques (HAP) dans les feuilles de thé sèches et les infusions de thé au Vietnam : niveaux de contamination et évaluation des risques alimentaires. Géochimie environnementale et santé 42 :2853−63 doi : 10.1007/s10653-020-00524-3
CrossRef Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. La présence de 16 HAP EPA dans les aliments – Une revue. Composés aromatiques polycycliques 35:248−84 doi : 10.1080/10406638.2014.918550
CrossRef Google Scholar
[12] Omodara NB, Olabemiwo OM, Adedosu TA. 2019. Comparaison des HAP formés dans le bouillon fumé au bois de chauffage et au charbon de bois et dans le poisson-chat. Journal américain des sciences et technologies alimentaires 7 : 86−93 doi : 10.12691/ajfst-7-3-3
CrossRef Google Scholar
[13] Zou LY, Zhang W, Atkiston S. 2003. Caractérisation des émissions d'hydrocarbures aromatiques polycycliques provenant de la combustion de différentes espèces de bois de chauffage en Australie. Pollution de l'environnement 124 : 283−89 doi : 10.1016/S0269-7491(02)00460-8
CrossRef Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL et al. 2000. Activité du benzo [a] pyrène et de ses métabolites hydroxylés dans un test du gène rapporteur du récepteur des œstrogènes-α. Sciences toxicologiques 55:320−26 doi : 10.1093/toxsci/55.2.320
CrossRef Google Scholar
[15] Han Y, Chen Y, Ahmad S, Feng Y, Zhang F et al. 2018. Mesures à haute résolution temporelle et granulométrique des particules et de la composition chimique provenant de la combustion du charbon : implications pour le processus de formation de CE. Sciences et technologies de l'environnement 52 : 6676−85 doi : 10.1021/acs.est.7b05786
CrossRef Google Scholar
[16] Khiadani (Hajian) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M et al. 2013. Détermination de la concentration en hydrocarbures aromatiques polycycliques dans huit marques de thé noir les plus utilisées en Iran. Journal international d'ingénierie de la santé environnementale 2:40 doi: 10.4103/2277-9183.122427
CrossRef Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J, Andrews G, Jones JM et al. 2007. Émission d'espèces oxygénées provenant de la combustion du bois de pin et sa relation avec la formation de suie. Sécurité des processus et protection de l'environnement 85:430−40 doi : 10.1205/psep07020
CrossRef Google Scholar
[18] Shen G, Tao S, Wang W, Yang Y, Ding J et al. 2011. Émissions d'hydrocarbures aromatiques polycycliques oxygénés provenant de la combustion intérieure de combustibles solides. Sciences et technologies de l'environnement 45 : 3459−65 doi : 10.1021/es104364t
CrossRef Google Scholar
[19] Centre international de recherche sur le cancer (CIRC), Organisation mondiale de la santé. 2014. Echappements de moteurs diesel et essence et quelques nitroarènes. Centre international de recherche sur le cancer, Monographies sur l'évaluation des risques cancérogènes pour l'homme. Rapport. 105:9
[20] de Oliveira Galvão MF, de Oliveira Alves N, Ferreira PA, Caumo S, de Castro Vasconcellos P, et al. 2018. Particules brûlant la biomasse dans la région amazonienne brésilienne : effets mutagènes des nitro et oxy-HAP et évaluation des risques pour la santé. Pollution de l'environnement 233 : 960−70 doi : 10.1016/j.envpol.2017.09.068
CrossRef Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H et al. 2018. Le dépôt de 9,10-anthraquinone dans les plantations de thé pourrait être l'une des raisons de la contamination du thé. Chimie alimentaire 244 : 254−59 doi : 10.1016/j.foodchem.2017.09.123
CrossRef Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Identification de la contamination par la 9,10-anthraquinone lors de la transformation du thé noir et vert en Indonésie. Chimie alimentaire 327:127092 doi: 10.1016/j.foodchem.2020.127092
CrossRef Google Scholar
[23] Zamora R, Hidalgo FJ. 2021. Formation de naphtoquinones et d'anthraquinones par des réactions carbonyl-hydroquinone/benzoquinone : une voie potentielle pour l'origine de la 9,10-anthraquinone dans le thé. Chimie alimentaire 354:129530 doi: 10.1016/j.foodchem.2021.129530
CrossRef Google Scholar
[24] Yang M, Luo F, Zhang X, Wang X, Sun H et al. 2022. Absorption, translocation et métabolisme de l'anthracène dans les plants de thé. Science de l'environnement total 821:152905 doi : 10.1016/j.scitotenv.2021.152905
CrossRef Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019. Influence du fumage et du barbecue sur la teneur en anthraquinone (ATQ) et en hydrocarbures aromatiques polycycliques (HAP) dans les saucisses de type Frankfurter. Journal de chimie agricole et alimentaire 67 : 13998−4004 doi : 10.1021/acs.jafc.9b03316
CrossRef Google Scholar
[26] Fouillaud M, Caro Y, Venkatachalam M, Grondin I, Dufossé L. 2018. Anthraquinones. Dans Composés phénoliques dans les aliments : caractérisation et analyse, éd. Léon ML.Vol. 9. Boca Raton : Presse CRC. pp. 130−70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muniategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, et al. 2003. Une nouvelle méthode pour la détermination simultanée des HAP et des métaux dans des échantillons de particules atmosphériques. Environnement atmosphérique 37 : 4171−75 doi : 10.1016/S1352-2310(03)00523-5
CrossRef Google Scholar
À propos de cet article
Citer cet article
Yu J, Zhou L, Wang X, Yang M, Sun H et al. 2022. Contamination par la 9,10-anthraquinone dans le traitement du thé utilisant le charbon comme source de chaleur. Recherche sur les usines de boissons 2 : 8 est ce que je : 10.48130/BPR-2022-0008
Heure de publication : 09 mai 2022