Abstracto
9,10-ansquinona (AQ) es un contaminante con un riesgo cancerígeno potencial y ocurre en el té de todo el mundo. El límite de residuos máximos (MRL) de AQ en el té establecido por la Unión Europea (UE) es de 0.02 mg/kg. Las posibles fuentes de AQ en el procesamiento del té y las principales etapas de su ocurrencia se investigaron en función de un método analítico AQ modificado y el análisis de espectrometría de masas en tándem de cromatografía de gases (GC-MS/MS). En comparación con la electricidad como fuente de calor en el procesamiento del té verde, AQ aumentó de 4.3 a 23.9 veces en el procesamiento del té con carbón como fuente de calor, superior a 0.02 mg/kg, mientras que el nivel de AQ en el entorno se triplicó. Se observó la misma tendencia en el procesamiento de té de Oolong bajo calor de carbón. Los pasos con contacto directo entre las hojas y los humos de té, como la fijación y el secado, se consideran los principales pasos de producción de AQ en el procesamiento del té. Los niveles de AQ aumentaron con el creciente tiempo de contacto, lo que sugiere que los altos niveles de contaminantes AQ en el té pueden derivarse de los humos causados por el carbón y la combustión. Se analizaron cuatro muestras de diferentes talleres con electricidad o carbón como fuentes de calor, variadas de 50.0% -85.0% y 5.0% −35.0% para la detección y excede las tasas de AQ. Además, se observó el contenido máximo de AQ de 0.064 mg/kg en el producto de té con carbón como fuente de calor, lo que indica que los altos niveles de contaminación AQ en los productos de té probablemente serán aportados por el carbón.
Palabras clave: 9,10-antraquinona, procesamiento del té, carbón, fuente de contaminación
INTRODUCCIÓN
El té fabricado con las hojas del arbusto Evergreen Camellia sinensis (L.) O. Kuntze, es una de las bebidas más populares a nivel mundial debido a su refrescante sabor y beneficios para la salud. En 2020 en todo el mundo, la producción de té había aumentado a 5,972 millones de toneladas métricas, lo que se duplicó en los últimos 20 años [1]. Basado en diferentes formas de procesamiento, hay seis tipos principales de té, que incluyen té verde, té negro, té oscuro, té oolong, té blanco y té amarillo [2,3]. Para garantizar la calidad y seguridad de los productos, es muy importante monitorear los niveles de contaminantes y definir el origen.
Identificar las fuentes de contaminantes, como los residuos de pesticidas, metales pesados y otros contaminantes, como los hidrocarburos aromáticos policíclicos (HAP), es el paso principal para controlar la contaminación. La pulverización directa de productos químicos sintéticos en plantaciones de té, así como la deriva de aire causada por operaciones cerca de los jardines de té, son la principal fuente de residuos de pesticidas en el té [4]. Los metales pesados pueden acumularse en el té y conducir a la toxicidad, que se derivan principalmente del suelo, el fertilizante y la atmósfera [5-7]. En cuanto a otra contaminación que apareció inesperadamente en el té, fue bastante difícil de identificar debido a los complejos procedimientos de la cadena de té de producción, incluida la plantación, el procesamiento, el paquete, el almacenamiento y el transporte. Los HAP en el té provienen de la deposición de los escapes del vehículo y la combustión de los combustibles utilizados durante el procesamiento de hojas de té, como la leña y el carbón [8-10].
Durante la combustión de carbón y leña, se forman contaminantes como los óxidos de carbono [11]. Como resultado, es susceptible de residuos de estos contaminantes mencionados anteriormente en los productos procesados, como el grano, el stock ahumado y el pescado de gato, a alta temperatura, lo que representa una amenaza para la salud humana [12,13]. Los HAP causados por la combustión se derivan de la volatilización de los HAP contenidos en los combustibles, la descomposición de alta temperatura de los compuestos aromáticos y la reacción compuesta entre los radicales libres [14]. La temperatura de combustión, el tiempo y el contenido de oxígeno son factores importantes que afectan la conversión de HAP. Con el aumento de la temperatura, el contenido de HAP primero aumentó y luego disminuyó, y el valor máximo ocurrió a 800 ° C; El contenido de HAP disminuyó bruscamente para rastrear con el aumento del tiempo de combustión cuando estaba por debajo de un límite llamado 'tiempo límite', con el aumento del contenido de oxígeno en el aire de combustión, las emisiones de HAP se redujeron significativamente, pero la oxidación incompleta produciría opá y otros derivados [15-17].
9,10-antraquinona (AQ, CAS: 84-65-1, Fig. 1), un derivado de HAP que contiene oxígeno [18], consta de tres ciclos condensados. Fue listado como un posible carcinógeno (Grupo 2B) por la Agencia Internacional de Investigación sobre Cáncer en 2014 [19]. AQ puede envenenar al complejo de escisión de topoisomerasa II e inhibir la hidrólisis del trifosfato de adenosina (ATP) por la topoisomerasa II de ADN, lo que provoca las roturas de doble cadena de ADN, lo que significa que la exposición a largo plazo bajo el entorno que contiene AQ y el contacto directo con el nivel alto de AQ puede conducir al daño del ADN, la mutación y aumentar el riesgo de cáncer [20]. Como efectos negativos en la salud humana, la Unión Europea estableció el límite de residuos máximos de AQ (MRL) de 0.02 mg/kg en el té. Según nuestros estudios anteriores, los depósitos de AQ se sugirieron como la fuente principal durante la plantación de té [21]. Además, según las consecuencias experimentales en el procesamiento de té verde y negro indonesio, es obvio que el nivel de AQ cambió significativamente y el humo del equipo de procesamiento se sugirió como una de las principales razones [22]. Sin embargo, el origen preciso de AQ en el procesamiento del té seguía siendo difícil, aunque se sugirieron algunas hipótesis de la vía química AQ [23,24], lo que indica que es extremadamente importante determinar los factores cruciales que afectan el nivel de AQ en el procesamiento del té.
Figura 1. La fórmula química de Aq.
Dada la investigación sobre la formación de AQ durante la combustión de carbón y la amenaza potencial de los combustibles en el procesamiento del té, se realizó un experimento comparativo para explicar el efecto del procesamiento de fuentes de calor en AQ en el té y el aire, análisis cuantitativo sobre los cambios del contenido de AQ en diferentes pasos de procesamiento, lo que es útil para confirmar el origen preciso, el patrón de ocurrencia y el grado de contaminación de AQ en el procesamiento del té.
RESULTADOS
Validación de métodos
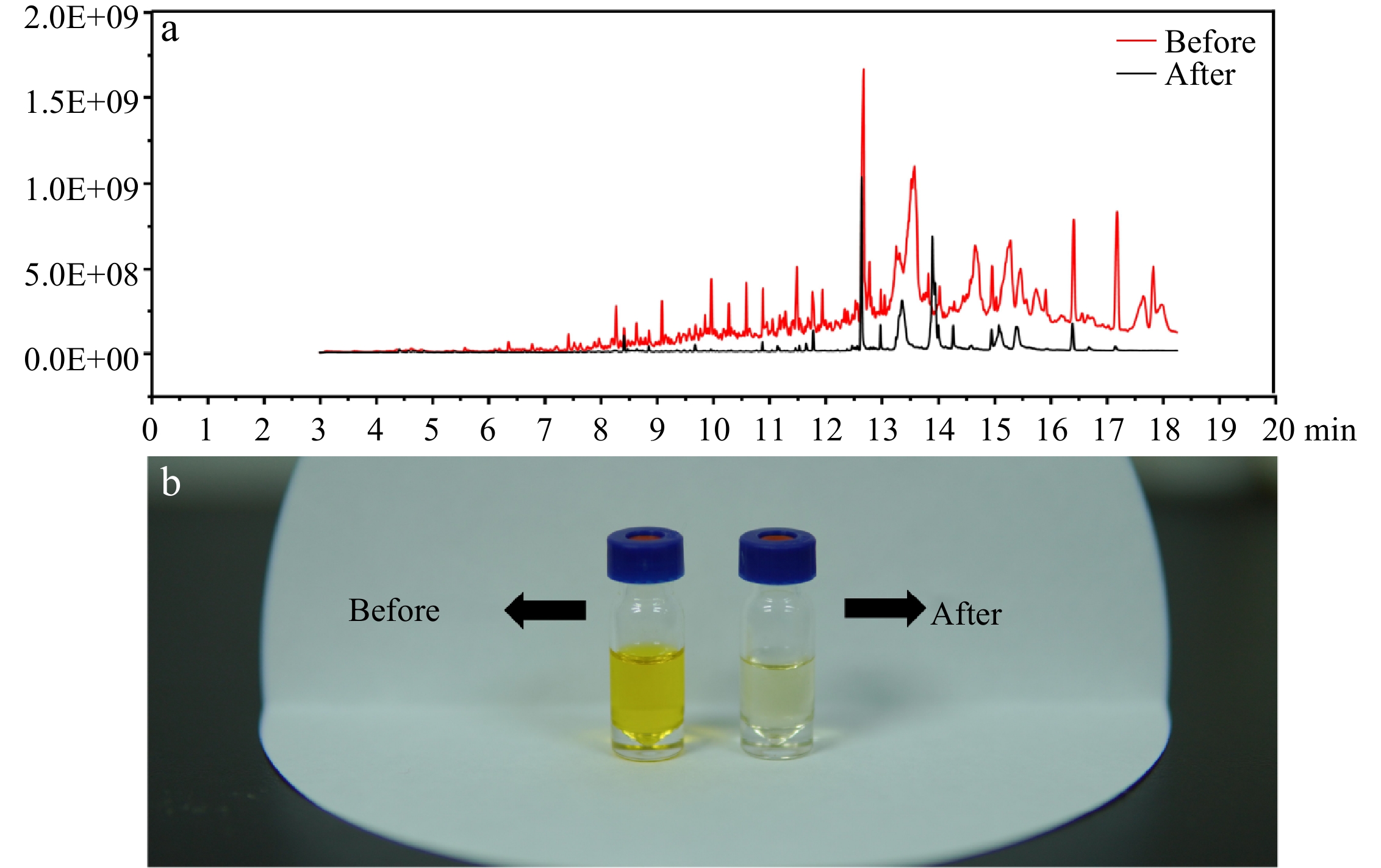
En comparación con nuestro estudio anterior [21], se combinó un procedimiento de extracción líquido-líquido antes de la inyección a GC-MS/MS para mejorar la sensibilidad y mantener declaraciones instrumentales. En la Fig. 2B, el método mejorado mostró una mejora significativa en la purificación de la muestra, el solvente se volvió más claro en color. En la Fig. 2A, un espectro de escaneo completo (50-350 m/z) ilustró que después de la purificación, la línea base del espectro de MS se redujo obviamente y los menos picos cromatográficos estaban disponibles, lo que indica que se eliminaron una gran cantidad de compuestos interferentes después de la extracción líquido líquido.
Figura 2. (A) Espectro de escaneo completo de la muestra antes y después de la purificación. (b) El efecto de purificación del método mejorado.
La validación del método, incluida la linealidad, la recuperación, el límite de cuantificación (LOQ) y el efecto matricial (ME), se muestran en la Tabla 1. Es satisfactorio obtener la linealidad con el coeficiente de determinación (R2) superior a 0.998, que varió de 0.005 a 0.2 mg/kg en la matriz de té y solvente de acetonitril, y en la muestra de aire de 0.5 a 8.
La recuperación de AQ se evaluó a tres concentraciones en pico entre las concentraciones medidas y reales en el té seco (0.005, 0.02, 0.05 mg/kg), brotes de té fresco (0.005, 0.01, 0.02 mg/kg) y muestra de aire (0.5, 1.5, 3 μg/m3). La recuperación de AQ en el té varió de 77.78% a 113.02% en té seco y de 96.52% a 125.69% en brotes de té, con RSD% inferior al 15%. La recuperación de AQ en muestras de aire varió de 78.47% a 117.06% con RSD% inferior al 20%. La concentración de pico más baja se identificó como LOQ, que fueron 0.005 mg/kg, 0.005 mg/kg y 0.5 μg/m³ en brotes de té, muestras de té y aire seco, respectivamente. Como se enumera en la Tabla 1, la matriz del té seco y los brotes de té aumentó ligeramente la respuesta AQ, lo que llevó al ME de 109.0% y 110.9%. En cuanto a la matriz de las muestras de aire, el ME fue del 196.1%.
Los niveles de AQ durante el procesamiento del té verde
Con el objetivo de descubrir los efectos de las diferentes fuentes de calor en el té y el entorno de procesamiento, un lote de hojas frescas se dividió en dos grupos específicos y se procesó por separado en dos talleres de procesamiento en la misma empresa. Un grupo fue suministrado con electricidad y el otro con carbón.
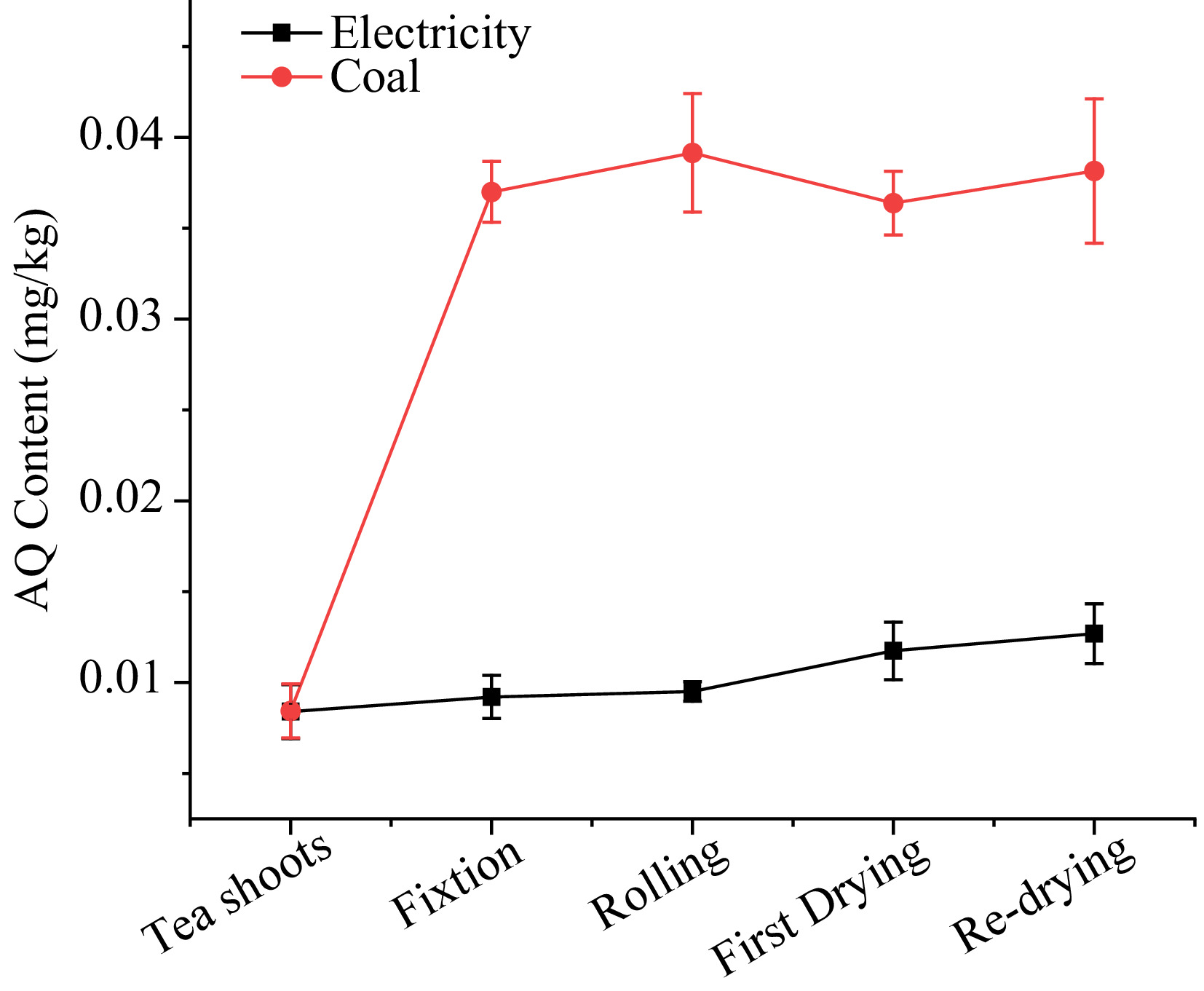
Como se muestra en la Fig. 3, el nivel de AQ con electricidad a medida que la fuente de calor varió de 0.008 a 0.013 mg/kg. Durante el proceso de fijación, el pergamino de las hojas de té causadas por el procesamiento en una olla con alta temperatura resultó en un aumento del 9.5% en AQ. Luego, el nivel de AQ permaneció durante el proceso de laminación a pesar de la pérdida de jugo, lo que sugiere que los procesos físicos pueden no afectar el nivel de AQ en el procesamiento del té. Después de los primeros pasos de secado, el nivel de AQ aumentó ligeramente de 0.010 a 0.012 mg/kg, luego continuó aumentando a 0.013 mg/kg hasta el final de la redacción. Los PFS, que mostraron significativamente la variación en cada paso, fueron 1.10, 1.03, 1.24, 1.08 en fijación, rodamiento, primer secado y secado, respectivamente. Los resultados de PFS sugirieron que el procesamiento bajo energía eléctrica tuvo un ligero efecto en los niveles de AQ en el té.
Figura 3. El nivel AQ durante el procesamiento del té verde con electricidad y carbón como fuentes de calor.
En el caso del carbón como fuente de calor, el contenido de AQ aumentó bruscamente durante el procesamiento del té, aumentando de 0.008 a 0.038 mg/kg. El 338.9% AQ se incrementaron en el procedimiento de fijación, alcanzando 0.037 mg/kg, que excedió con creces el MRL de 0.02 mg/kg establecido por la Unión Europea. Durante la etapa de rodadura, el nivel de AQ aún aumentó en un 5,8% a pesar de estar lejos de la máquina de fijación. En el primer secado y el rehichamiento, el contenido de AQ aumentó poco o disminuyó ligeramente. El PFS que usa carbón como fuente de calor en la fijación, rodar primero secado y secado fue de 4.39, 1.05, 0.93 y 1.05, respectivamente.
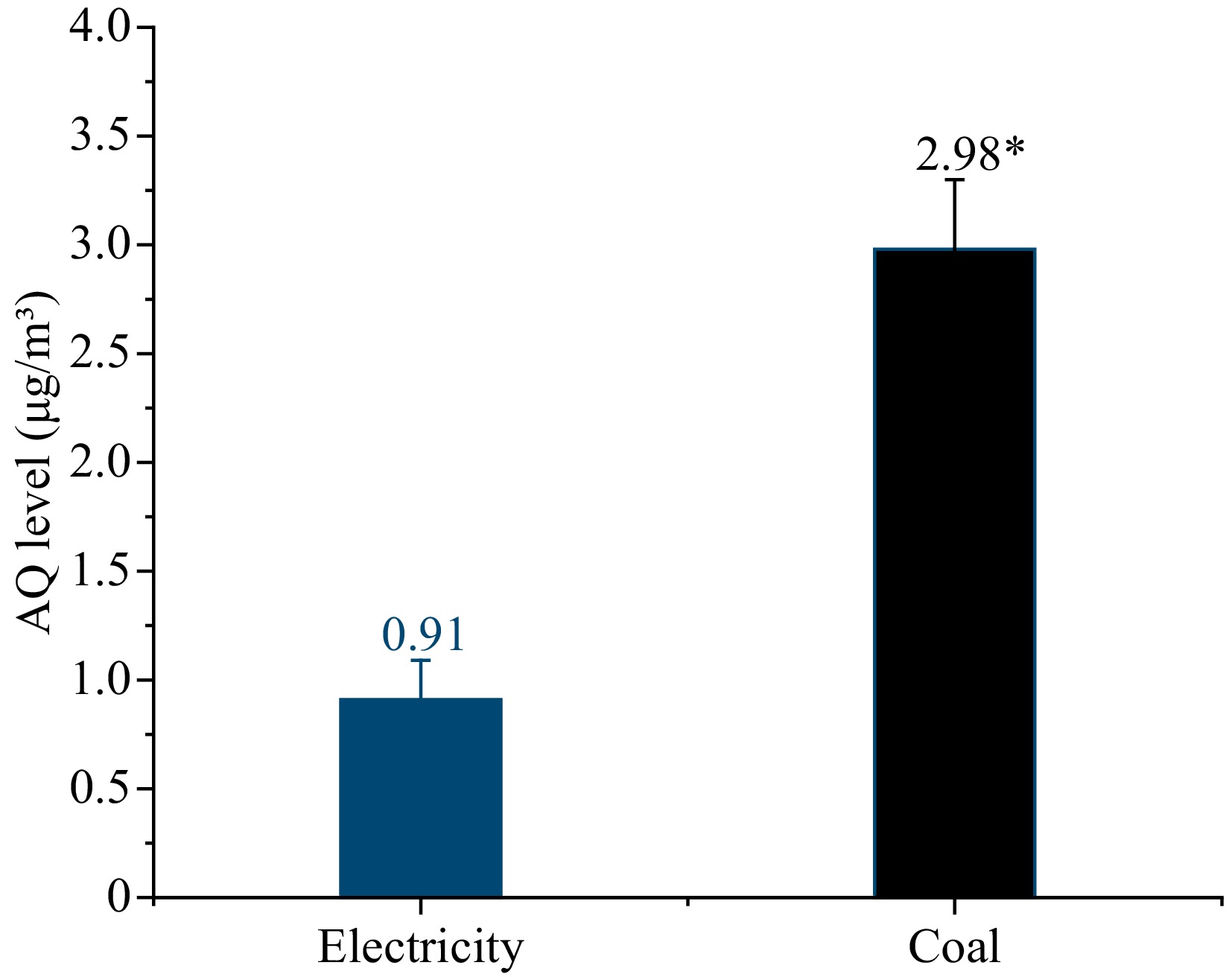
Para determinar aún más la relación entre la combustión de carbón y la contaminación AQ, los asuntos de partículas suspendidas (PM) en el aire en los talleres bajo ambas fuentes de calor se recolectaron para la evaluación del aire, como se muestra en la figura 4. El nivel AQ de PMS con carbón como fuente de calor fue de 2.98 μg/m3, que fue más de tres veces más alto que el electricidad 0.91 μg/M3.
Figura 4. Los niveles de AQ en el medio ambiente con electricidad y carbón como fuente de calor. * Indica diferencias significativas en los niveles de AQ en las muestras (p <0.05).
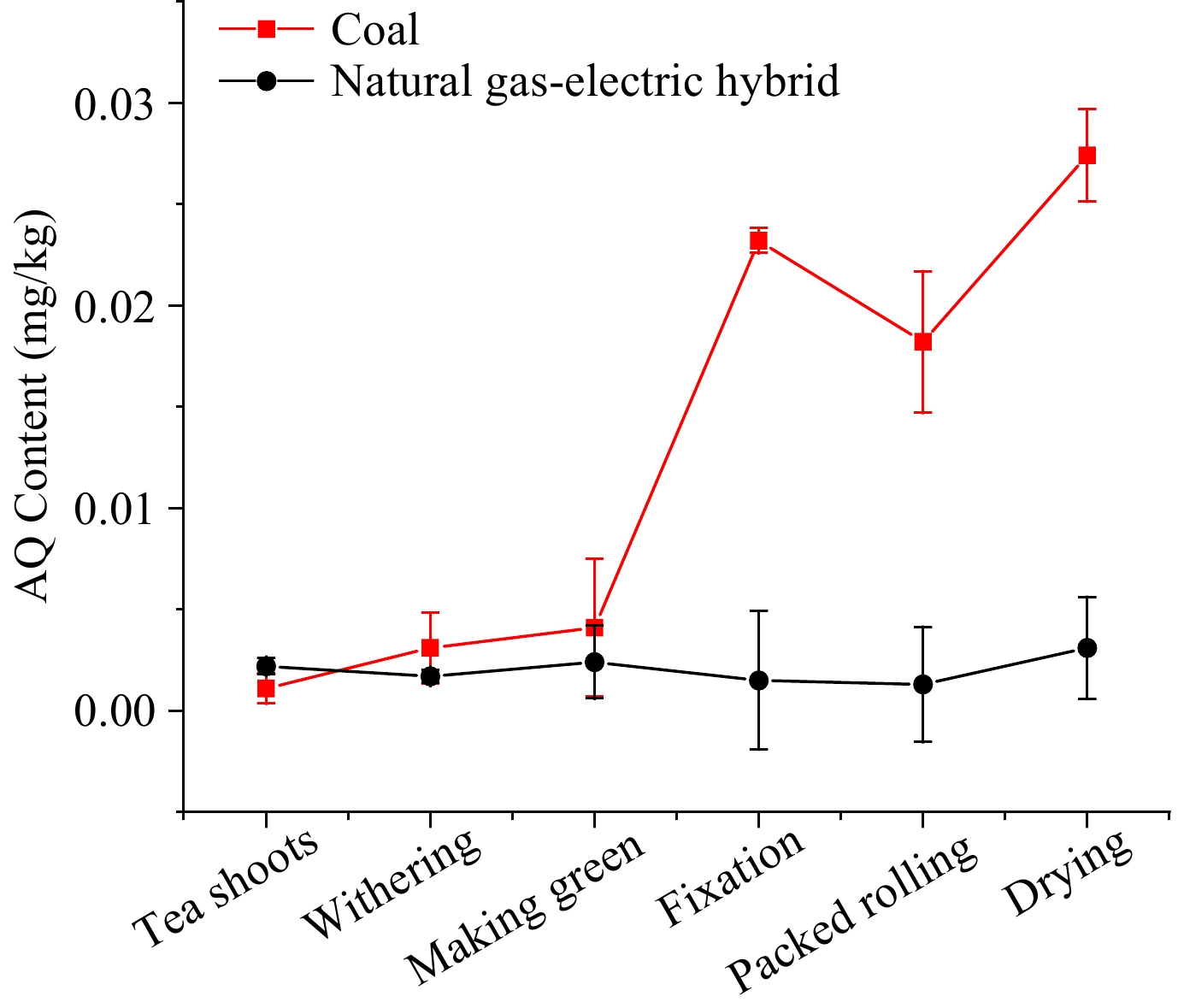
Los niveles de AQ durante el procesamiento de té Oolong Oolong Tea, producidos principalmente en Fujian y Taiwán, es una especie de té parcialmente fermentado. Para determinar aún más los pasos principales de aumentar el nivel de AQ y los efectos de diferentes combustibles, el mismo lote de hojas frescas se convirtió en té oolong con carbón e híbrido de gas natural-eléctrico como fuentes de calor, simultáneamente. Los niveles de AQ en el procesamiento de té de Oolong utilizando diferentes fuentes de calor se muestran en la figura 5. Para el procesamiento de té de Oolong con híbrido de gas natural-eléctrico, la tendencia del nivel de AQ se estancó por debajo de 0.005 mg/kg, que era similar a la de la electricidad.
Figura 5. El nivel de AQ durante el procesamiento de té Oolong con mezcla de gas natural y carbón como fuente de calor.
Con el carbón como fuente de calor, los niveles de AQ en los dos primeros pasos, marchitando y haciendo verde, fueron esencialmente los mismos que con la mezcla de gas natural eléctrico. Sin embargo, los procedimientos posteriores hasta que la fijación mostró la brecha se amplió gradualmente, momento en el cual el nivel de AQ aumentó de 0.004 a 0.023 mg/kg. El nivel en el paso de rodadura empaquetado disminuyó a 0.018 mg/kg, lo que puede deberse a la pérdida de jugo de té que lleva algunos de los contaminantes AQ. Después de la etapa de rodadura, el nivel en la etapa de secado aumentó a 0.027 mg/kg. Al marchitar, hacer verde, fijar, rodar y secar, el PFS fue 2.81, 1.32, 5.66, 0.78 y 1.50, respectivamente.
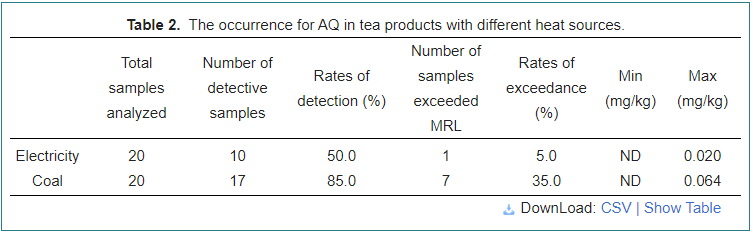
La aparición de AQ en productos de té con diferentes fuentes de calor.
To determine the effects on AQ content of tea with different heat sources, 40 tea samples from the tea workshops using electricity or coal as heat sources were analyzed, as shown in Table 2. Compared with using electricity as a heat source, coal had the most detective rates (85.0%) with the maximum AQ level of 0.064 mg/kg, indicating that it was easy to cause AQ contaminant by fumes produced by coal combustion, and a rate of Se observó 35.0% en muestras de carbón. Lo más notable, la electricidad tenía las tasas de detective y excedancia más bajas de 56.4% y 7.7% respectivamente, con un contenido máximo de 0.020 mg/kg.
DISCUSIÓN
Basado en el PFS durante el procesamiento con los dos tipos de fuentes de calor, estaba claro que la fijación fue el principal paso que condujo al aumento de los niveles de AQ en la producción de té con carbón y el procesamiento bajo energía eléctrica tuvo un ligero efecto en el contenido de AQ en el té. Durante el procesamiento del té verde, la combustión de carbón produjo muchos humos en el proceso de fijación en comparación con el proceso de calefacción eléctrica, lo que indica que tal vez los humos fueron la principal fuente de contaminantes AQ del contacto con brotes de té instantáneamente en el procesamiento del té, similar al proceso de exposición en las muestras de barbacoa ahumada [25]. El ligeramente aumento en el contenido de AQ durante la etapa de rodamiento sugirió que los humos causados por la combustión de carbón no solo afectaron el nivel de AQ durante el paso de fijación, sino también en el entorno de procesamiento debido a la deposición atmosférica. También se usaron los carbones como fuente de calor en el primer secado y volver a secar, pero en estos dos pasos el contenido de AQ aumentó ligeramente o disminuyó ligeramente. Esto puede explicarse por el hecho de que la secadora de viento caliente cerrada mantuvo el té alejado de los humos causados por la combustión de carbón [26]. Para determinar la fuente de contaminantes, se analizaron los niveles de AQ en la atmósfera, lo que resultó en una brecha significativa entre los dos talleres. La razón principal de esto es que el carbón utilizado en las etapas de fijación, primer secado y secado generaría AQ durante la combustión incompleta. Estos AQ se adsorbieron en las pequeñas partículas de sólidos después de la combustión de carbón y se dispersaron en el aire, elevando los niveles de contaminación AQ en el entorno del taller [15]. Con el tiempo, debido a la gran superficie específica y la capacidad de adsorción del té, estas partículas se asentaron en la superficie de las hojas de té, lo que resulta en el aumento de AQ en la producción. Por lo tanto, se pensó que la combustión de carbón era la ruta principal que conduce a una contaminación excesiva de AQ en el procesamiento del té, siendo los humos la fuente de contaminación.
En cuanto al procesamiento de té de Oolong, AQ se incrementó en procesamiento con ambas fuentes de calor, pero la diferencia entre las dos fuentes de calor fue significativa. Los resultados también sugirieron que el carbón como fuente de calor jugó un papel importante en el aumento del nivel de AQ, y la fijación se consideró como el paso principal para aumentar la contaminación de AQ en el procesamiento de té de Oolong en función del PFS. Durante el procesamiento del té Oolong con híbrido de gas natural como la fuente de calor, la tendencia del nivel de AQ se estancó por debajo de 0.005 mg/kg, que era similar a la del té verde con electricidad, lo que sugiere que la energía limpia, como la electricidad y el gas natural, puede disminuir el riesgo de producir contaminantes AQ del procesamiento.
En cuanto a las pruebas de muestreo, los resultados mostraron que la situación de la contaminante de AQ era peor cuando se usaba el carbón como fuente de calor en lugar de electricidad, lo que podría deberse a los humos de la combustión de carbón que entraba en contacto con las hojas de té y se quedaba alrededor del lugar de trabajo. Sin embargo, aunque era obvio que la electricidad era la fuente de calor más limpia durante el procesamiento del té, todavía había un contaminante AQ en los productos de té utilizando electricidad como fuente de calor. La situación parece ligeramente similar al trabajo publicado previamente en el que la reacción de 2 alquenales con hidroquinonas y benzoquinonas se sugirió como una vía química potencial [23], se investigarán las razones en futuras investigaciones.
Conclusiones
En este trabajo, las posibles fuentes de contaminación AQ en el té verde y oolong se confirmaron mediante experimentos comparativos basados en métodos analíticos GC-MS/MS mejorados. Nuestros hallazgos respaldaron directamente que la principal fuente de contaminantes de altos niveles de AQ fue causada por la combustión, que no solo afectó las etapas de procesamiento sino que también afectó los entornos de talleres. A diferencia de las etapas rodantes y marchitas, donde los cambios en el nivel de AQ fueron discretos, las etapas con participación directa del carbón y la leña, como la fijación, son el proceso principal en el que la contaminación de AQ aumentó debido a la cantidad de contacto entre el té y los humos durante estas etapas. Por lo tanto, se recomendaron combustibles limpios como el gas natural y la electricidad como fuente de calor en el procesamiento del té. Además, los resultados experimentales también mostraron que en ausencia de humos generados por la combustión, todavía había otros factores que contribuyeron a trazar AQ durante el procesamiento del té, mientras que también se observaron pequeñas cantidades de AQ en el taller con combustibles limpios, que deberían investigarse más a fondo en futuras investigaciones.
MATERIALES Y MÉTODOS
Reactivos, productos químicos y materiales
El estándar de antraquinona (99.0%) se adquirió al Dr. Ehrenstorfer GmbH Company (Augsburg, Alemania). El estándar interno D8-Anthraquinona (98.6%) se adquirió de isótopos C/D/N (Quebec, Canadá). Sulfato de sodio anhidro (NA2SO4) y sulfato de magnesio (MGSO4) (Shanghai, China). Florisil fue suministrado por Wenzhou Organic Chemical Company (Wenzhou, China). El papel de fibra Mircro-Glass (90 mm) se adquirió en la compañía Ahlstrom-Munksjö (Helsinki, Finlandia).
Preparación de muestra
Las muestras de té verde se procesaron con fijación, rodamiento, primer secado y secado (usando equipos cerrados), mientras que las muestras de té de Oolong se procesaron con marchito, haciendo verde (balanceo y de pie fresco alternativamente), fijación, rodamiento empacado y secado. Las muestras de cada paso se recogieron tres veces a 100 g después de una mezcla exhaustiva. Todas las muestras se almacenaron a -20 ° C para un análisis posterior.
Las muestras de aire se recogieron mediante papel de fibra de vidrio (90 mm) utilizando muestreadores de volumen medio (PTS-100, Qingdao Laoshan Electronic Instrument Company, Qingdao, China) [27], funcionando a 100 l/min durante 4 h.
Las muestras fortificadas se aumentaron con AQ a 0.005 mg/kg, 0.010 mg/kg, 0.020 mg/kg para brotes de té fresco, a 0.005 mg/kg, 0.020 mg/kg, 0.050 mg/kg para té seco y a 0.012 mg/kg (0.5 µg/m3 para muestra de aire), 0.036 mg/kg/kg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg/mg SMAPLE DE AIRE), 0.072 mg/kg (3.0 µg/m3 para la muestra de aire) para papel de filtro de vidrio, respectivamente. Después de temblar completamente, todas las muestras se dejaron durante 12 h, seguidas de extracción y pasos de limpieza.
El contenido de humedad se obtuvo tomando 20 g de la muestra después de mezclar cada paso, calentando a 105 ° C durante 1 h, luego pesando y repitiendo tres veces y tomando el valor promedio y dividiéndolo por el peso antes del calentamiento.
Extracción de muestra y limpieza
Muestra de té: la extracción y purificación de AQ de muestras de té se realizó en base al método publicado de Wang et al. con varias adaptaciones [21]. Brevemente, 1,5 g de muestras de té se mezclaron primero con 30 μl de D8-AQ (2 mg/kg) y se fueron para resistir durante 30 minutos, luego bien mezclados con 1,5 ml de agua desionizada y se fue para soportar durante 30 minutos. Se añadieron 15 ml al 20% de acetona en n-hexano a las muestras de té y se sonicó durante 15 minutos. Luego, las muestras se vórtice con 1,0 g de mgSO4 durante 30 s, y se centrifugaron durante 5 minutos, a 11,000 rpm. Después de moverse a matraces en forma de pera de 100 ml, se evaporaron 10 ml de la fase orgánica superior a casi la sequedad al vacío a 37 ° C. 5 ml al 2.5% de acetona en n-hexano redislvió el extracto en matraces en forma de pera para la purificación. La columna de vidrio (10 cm × 0.8 cm) consistía desde la parte inferior a la parte superior de la lana de vidrio y el florisil 2G, que estaba entre dos capas de 2 cm Na2SO4. Luego, 5 ml de acetona al 2.5% en n-hexano previertaron la columna. Después de cargar la solución redisoleada, AQ se eluyó tres veces con 5 ml, 10 ml, 10 ml de acetona al 2.5% en N-hexano. Los eluados combinados se transfirieron a matraces en forma de pera y se evaporaron a casi sequedad al vacío a 37 ° C. Luego, el residuo seco se reconstituyó con 1 ml de acetona al 2.5% en hexano seguido de filtración a través de un filtro de tamaño de poro de 0.22 µm. Luego, la solución reconstituida se mezcló con acetonitrilo a una relación de volumen de 1: 1. Después del paso de agitación, el subnatante se usó para el análisis GC-MS/MS.
Muestra de aire: la mitad del papel de fibra, goteado con 18 μl D8-AQ (2 mg/kg), se sumergió en 15 ml de acetona al 20% en N-hexano, luego sonicó durante 15 minutos. La fase orgánica se separó por centrifugación a 11,000 rpm durante 5 minutos y toda la capa superior se eliminó en un matraz en forma de pera. Todas las fases orgánicas se evaporaron a casi sequedad al vacío a 37 ° C. 5 ml de acetona al 2.5% en hexano redisló los extractos para la purificación de la misma manera que en las muestras de té.
Análisis GC-MS/MS
Se utilizó el cromatógrafo de gas Varian 450 equipado con el detector de masa en tándem Varian 300 (Varian, Walnut Creek, CA, EE. UU.) Para realizar un análisis AQ con el software MS Workstation versión 6.9.3. Se usó VF-5MS de la columna Capilar Varian Factor cuatro (30 m × 0.25 mm × 0.25 μm) para la separación cromatográfica. El gas portador, helio (> 99.999%), se estableció a un caudal constante de 1.0 ml/min con gas de colisión de argón (> 99.999%). La temperatura del horno comenzó desde 80 ° C y se mantuvo durante 1 min; aumentó a 15 ° C/min a 240 ° C, luego alcanzó 260 ° C a 20 ° C/min y se mantuvo durante 5 minutos. La temperatura de la fuente de iones fue de 210 ° C, así como la temperatura de la línea de transferencia de 280 ° C. El volumen de inyección fue de 1.0 μl. Las condiciones MRM se muestran en la Tabla 3.
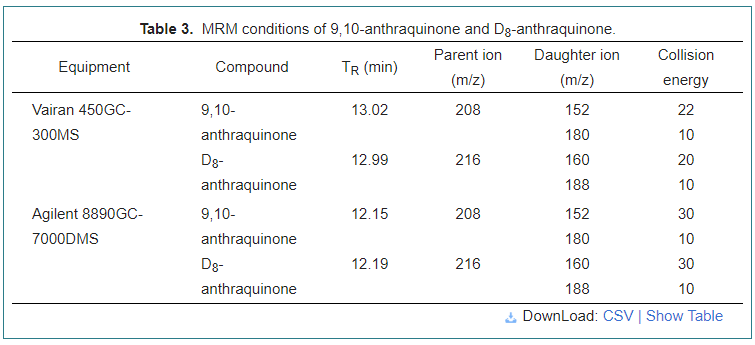
El cromatógrafo de gases Agilent 8890 equipado con el espectrómetro de masas triple cuadrupolo Agilent 7000D (Agilent, Stevens Creek, CA, EE. UU.) Se utilizó para analizar el efecto de purificación con el software Masshunter versión 10.1. La columna GC HP-5MS Agilent J&W (30 m × 0.25 mm × 0.25 μm) se usó para la separación cromatográfica. El gas portador, el helio (> 99.999%), se estableció a una velocidad de flujo constante de 2.25 ml/min con gas de colisión de nitrógeno (> 99.999%). La temperatura de la fuente de iones Ei se ajustó a 280 ° C, lo mismo que la temperatura de la línea de transferencia. La temperatura del horno comenzó desde 80 ° C y se mantuvo durante 5 minutos; elevado por 15 ° C/min a 240 ° C, luego alcanzó 280 ° C a 25 ° C/min y se mantuvo durante 5 min. Las condiciones MRM se muestran en la Tabla 3.
Análisis estadístico
El contenido de AQ en hojas frescas se corrigió al contenido de materia seca dividiendo por contenido de humedad para comparar y analizar los niveles de AQ durante el procesamiento.
Los cambios de AQ en muestras de té se evaluaron con el software Microsoft Excel e IBM SPSS Statistics 20.
El factor de procesamiento se utilizó para describir los cambios en AQ durante el procesamiento del té. PF = RL/RF, donde RF es el nivel AQ antes del paso de procesamiento y RL es el nivel AQ después del paso de procesamiento. PF indica una disminución (PF <1) o un aumento (PF> 1) en residual AQ durante un paso de procesamiento específico.
Me indica una disminución (me <1) o un aumento (me> 1) en respuesta a los instrumentos analíticos, que se basa en la relación de pendientes de calibración en la matriz y el solvente de la siguiente manera:
Me = (slopematrix/slopesolvent - 1) × 100%
Donde Slopematrix es la pendiente de la curva de calibración en el disolvente de matriz, la pendiente es la pendiente de la curva de calibración en el disolvente.
EXPRESIONES DE GRATITUD
Este trabajo fue apoyado por el proyecto importante de ciencia y tecnología en la provincia de Zhejiang (2015C12001) y la Fundación Nacional de Ciencias de China (42007354).
Incompatibilidad
Los autores declaran que no tienen conflicto de intereses.
Derechos y permisos
Copyright: © 2022 por el autor (s). Licenciatario exclusivo Maximum Academic Press, Fayetteville, GA. Este artículo es un artículo de acceso abierto distribuido bajo la licencia de atribución de Creative Commons (CC por 4.0), visite https://createivecommons.org/licenses/by/4.0/.
Referencias
[1] ITC. 2021. Boletín anual de estadísticas 2021. Https://inttea.com/publication/
[2] Hicks A. 2001. Revisión de la producción mundial del té y el impacto en la industria de la situación económica asiática. Au Journal of Technology 5
Google Scholar
[3] Katsuno T, Kasuga H, Kusano Y, Yaguchi Y, Tomomura M, et al. 2014. Caracterización de los compuestos odorantes y su formación bioquímica en el té verde con un proceso de almacenamiento de baja temperatura. Food Chemistry 148: 388−95 doi: 10.1016/j.foodchem.2013.10.069
CrossRef Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Cadena de contaminación de tridimios en el ecosistema del té y su control. Scientia Agricultura Sinica 40: 948-58
Google Scholar
[5] He H, Shi L, Yang G, You M, Vasseur L. 2020. Evaluación de riesgos ecológicos de metales pesados del suelo y residuos de pesticidas en plantaciones de té. Agricultura 10:47 doi: 10.3390/agricultura10020047
CrossRef Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J, et al. 2005. Contaminación de plomo en las hojas de té y factores no edfrados que lo afectan. Chemosphere 61: 726−32 doi: 10.1016/j.chemosphere.2005.03.053
CrossRef Google Scholar
[7] Owuor PO, Obaga SO, Othieno co. 1990. Los efectos de la altitud en la composición química del té negro. Journal of the Science of Food and Agriculture 50: 9-17 doi: 10.1002/jsfa.2740500103
CrossRef Google Scholar
[8] García Londoño VA, Reynoso M, Resnik S. 2014. Hidrocarburos aromáticos policíclicos (HAP) en Yerba Mate (Ilex paraguariensis) del mercado argentino. Aditivos y contaminantes alimentarios: Parte B 7: 247−53 doi: 10.1080/19393210.2014.919963
CrossRef Google Scholar
[9] Ishizaki A, Saito K, Hanioka N, Narimatsu S, Kataoka H. 2010. Determinación de hidrocarburos aromáticos policíclicos en muestras de alimentos por microextracción de fase sólida en línea automatizada acoplada con detección de cromatografía líquida de alto rendimiento-fluorescencia. Journal of Chromatography A 1217: 5555−63 doi: 10.1016/j.chroma.2010.06.068
CrossRef Google Scholar
[10] Phan Thi la, Ngoc NT, Quynh NT, Thanh NV, Kim TT, et al. 2020. Hidrocarburos aromáticos policíclicos (HAP) en hojas de té seco e infusiones de té en Vietnam: niveles de contaminación y evaluación de riesgos dietéticos. Geoquímica y salud ambiental 42: 2853−63 doi: 10.1007/s10653-020-00524-3
CrossRef Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. La aparición de 16 HAP de la EPA en alimentos - una revisión. Compuestos aromáticos policíclicos 35: 248−84 doi: 10.1080/10406638.2014.918550
CrossRef Google Scholar
[12] Omodara NB, Olabemiwo OM, Adedosu TA. 2019. Comparación de HAP formados en leña y carbón ahumado y pescado gato. American Journal of Food Science and Technology 7: 86-93 doi: 10.12691/ajfst-7-3-3
CrossRef Google Scholar
[13] Zou Ly, Zhang W, Atkiston S. 2003. La caracterización de las emisiones de hidrocarburos aromáticos policíclicos por la quema de diferentes especies de leña en Australia. Contaminación ambiental 124: 283-89 doi: 10.1016/s0269-7491 (02) 00460-8
CrossRef Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL, et al. 2000. Actividad del benzo [A] pireno y sus metabolitos hidroxilados en un ensayo de genes informadores de receptor de estrógeno-α. Ciencias toxicológicas 55: 320−26 doi: 10.1093/toxsci/55.2.320
CrossRef Google Scholar
[15] Han Y, Chen Y, Ahmad S, Feng Y, Zhang F, et al. 2018. Mediciones altas de tiempo y tamaño de la composición química de PM y la combustión de carbón: implicaciones para el proceso de formación de la CE. Environmental Science & Technology 52: 6676−85 doi: 10.1021/acs.est.7b05786
CrossRef Google Scholar
[16] Khiadani (Hajian) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M, et al. 2013. Determinación de la concentración de hidrocarburos aromáticos policíclicos en ocho marcas de té negro que se usan más en Irán. Revista Internacional de Ingeniería de Salud Ambiental 2:40 DOI: 10.4103/2277-9183.122427
CrossRef Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J, Andrews G, Jones JM, et al. 2007. Emisión de especies oxigenadas de la combustión de madera de pino y su relación con la formación de hollín. Proceso de seguridad y protección del medio ambiente 85: 430-40 doi: 10.1205/psep07020
CrossRef Google Scholar
[18] Shen G, Tao S, Wang W, Yang Y, Ding J, et al. 2011. Emisión de hidrocarburos aromáticos policíclicos oxigenados de la combustión de combustible sólido interior. Environmental Science & Technology 45: 3459−65 doi: 10.1021/es104364t
CrossRef Google Scholar
[19] Agencia Internacional de Investigación sobre Cáncer (IARC), Organización Mundial de la Salud. 2014. Ecranajes del motor diesel y de gasolina y algunos nitroarenos. Agencia Internacional de Investigación sobre Monografías de Cáncer sobre la evaluación de riesgos cancerígenos para los humanos. Informe. 105: 9
[20] De Oliveira Galvão MF, De Oliveira Alves N, Ferreira PA, Caumo S, de Castro Vasconcellos P, et al. 2018. Las partículas de quema de biomasa en la región amazónica brasileña: efectos mutagénicos de nitro y oxi-pahs y evaluación de riesgos para la salud. Contaminación ambiental 233: 960−70 doi: 10.1016/j.envpol.2017.09.068
CrossRef Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H, et al. 2018. El depósito de 9,10-ansquinona en la plantación de té podría ser una de las razones de la contaminación en el té. Food Chemistry 244: 254-59 doi: 10.1016/j.foodchem.2017.09.123
CrossRef Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Identificación de contaminación de 9,10-antraquinona durante el procesamiento de té negro y verde en Indonesia. Food Chemistry 327: 127092 doi: 10.1016/j.foodchem.2020.127092
CrossRef Google Scholar
[23] Zamora R, Hidalgo FJ. 2021. Formación de naftoquinonas y antraquinonas por reacciones de carbonil-hidroquinona/benzoquinona: una ruta potencial para el origen de 9,10-orthraquinona en el té. Food Chemistry 354: 129530 doi: 10.1016/j.foodchem.2021.129530
CrossRef Google Scholar
[24] Yang M, Luo F, Zhang X, Wang X, Sun H, et al. 2022. Absorción, translocación y metabolismo del antraceno en plantas de té. Ciencia del entorno total 821: 152905 doi: 10.1016/j.scitotenv.2021.152905
CrossRef Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019. Influencia del tabaquismo y la barbacoa en el contenido de la antraquinona (ATQ) e hidrocarburos aromáticos policíclicos (HAP) en las salas de tipo Frankfurter. Journal of Agricultural and Food Chemistry 67: 13998−4004 doi: 10.1021/acs.jafc.9b03316
CrossRef Google Scholar
[26] Fouillaud M, Caro Y, Venkatachalam M, Grondin I, Dufossé L. 2018. Antraquinones. En compuestos fenólicos en alimentos: caracterización y análisis, eds. Leo Ml.Vol. 9. Boca Raton: CRC Press. pp. 130-70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muniategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, et al. 2003. Un nuevo método para la determinación simultánea de HAP y metales en muestras de partículas atmosféricas. Ambiente atmosférico 37: 4171−75 doi: 10.1016/s1352-2310 (03) 00523-5
CrossRef Google Scholar
Sobre este artículo
Cita este artículo
Yu J, Zhou L, Wang X, Yang M, Sun H, et al. 2022. 9,10-Antraquinona en el procesamiento del té utilizando carbón como fuente de calor. Bebedge Plant Research 2: 8 doi: 10.48130/bpr-2022-0008
Tiempo de publicación: mayo-09-2022