Abstrakt
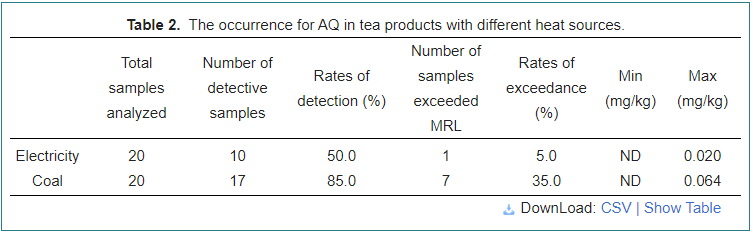
9,10-Anthraquinon (AQ) ist ein Verunreinigungsmittel mit einem potenziellen krebserzeugenden Risiko und tritt weltweit im Tee auf. Die maximale Rückstandsgrenze (MRL) von AQ im von der Europäischen Union (EU) festgelegten Tee beträgt 0,02 mg/kg. Die möglichen AQ-Quellen in der Teeverarbeitung und die Hauptstadien ihres Auftretens wurden auf der Grundlage einer modifizierten AQ-Analysemethode und einer Gaschromatographie-Tandem-Massenspektrometrie (GC-MS/MS) untersucht. Im Vergleich zu Elektrizität als Wärmequelle bei der Verarbeitung von grünem Tee stieg die AQ bei der Teeverarbeitung mit Kohle um das 4,3 bis 23,9 -fache als Wärmequelle von mehr als 0,02 mg/kg, während sich der AQ -Niveau in der Umwelt verdreifachte. Der gleiche Trend wurde bei der Oolong -Teeverarbeitung bei Kohlewärme beobachtet. Die Schritte mit direktem Kontakt zwischen Teeblättern und Dämpfen, wie Fixierung und Trocknen, gelten als Hauptschritte der AQ -Produktion in der Teeverarbeitung. Die AQ -Werte nahmen mit der steigenden Kontaktzeit zu, was darauf hindeutet, dass ein hohes Maß an AQ -Schadstoff im Tee aus den durch Kohle und Verbrennung verursachten Dämpfen abgeleitet werden kann. Viertes Proben aus verschiedenen Workshops mit Strom oder Kohle bei der Analyse von Wärmequellen lag im Bereich von 50,0% –85,0% und 5,0% –35,0% zur Nachweis und überschreiten die Raten von aq. Darüber hinaus wurde der maximale AQ -Gehalt von 0,064 mg/kg im Teeprodukt mit Kohle als Wärmequelle beobachtet, was darauf hinweist, dass die hohen AQ -Verunreinigungswerte in Teeprodukten wahrscheinlich durch Kohle beigetragen werden.
Schlüsselwörter: 9,10-Anthrachinon, Teeverarbeitung, Kohle, Kontaminationsquelle
EINFÜHRUNG
Tee, hergestellt aus Blättern der immergrünen Strauch Camellia sinensis (L.) O. Kuntze, ist aufgrund seines erfrischenden Geschmacks- und gesundheitlichen Vorteile eines der weltweit beliebtesten Getränke. Im Jahr 2020 war die Teeproduktion weltweit auf 5.972 Millionen Tonnen gestiegen, was sich in den letzten 20 Jahren verdoppelte [1]. Basierend auf verschiedenen Verarbeitungsmöglichkeiten gibt es sechs Haupttypen von Tee, einschließlich grünem Tee, schwarzem Tee, dunkler Tee, Oolong -Tee, weißem Tee und gelbem Tee [2,3]. Um die Qualität und Sicherheit von Produkten zu gewährleisten, ist es sehr wichtig, die Schadstoffe zu überwachen und den Ursprung zu definieren.
Die Identifizierung der Quellen von Kontaminanten wie Pestizidresten, Schwermetallen und anderen Schadstoffen wie polycyclischen aromatischen Kohlenwasserstoffen (PAK) ist der Hauptschritt zur Kontrolle der Verschmutzung. Direktes Sprühen von synthetischen Chemikalien in Teeplantagen sowie Luftdrift, die durch Operationen in der Nähe von Teegärten verursacht werden, sind die Hauptquelle für Pestizidreste in Tee [4]. Schwermetalle können sich im Tee ansammeln und zu Toxizität führen, die hauptsächlich aus Boden, Dünger und Atmosphäre stammen [5–7]. In Bezug auf andere Umweltverschmutzung, die unerwartet im Tee auftrat, war es aufgrund der komplexen Verfahren der Produktionskette, einschließlich Plantage, Verarbeitung, Verpackung, Lagerung, Lagerung und Transport, ziemlich schwierig zu identifizieren. Die PAK im Tee stammten aus der Ablagerung von Fahrzeugabgasen und der Verbrennung von Kraftstoffen während der Verarbeitung von Teeblättern wie Brennholz und Kohle [8–10].
Während der Kohle- und Brennholzverbrennung werden Schadstoffe wie Kohlenoxide gebildet [11]. Infolgedessen ist es anfällig für Rückstände dieser oben genannten Schadstoffe, die in den verarbeiteten Produkten wie Getreide, geräuchertem Bestand und Katzenfisch bei hoher Temperatur auftreten und eine Bedrohung für die menschliche Gesundheit darstellen [12,13]. Die durch die Verbrennung verursachten PAK sind aus der Verflüchtigung von PAK, die in den Brennstoffen selbst enthalten sind, der Hochtemperatur-Zersetzung von aromatischen Verbindungen und der Verbindungsreaktion zwischen freien Radikalen [14]. Verbrennungstemperatur, Zeit und Sauerstoffgehalt sind wichtige Faktoren, die die Umwandlung von PAK beeinflussen. Mit dem Temperaturanstieg nahm der PAK -Gehalt zuerst zu und nahm dann den Spitzenwert bei 800 ° C auf; Der PAK -Gehalt nahm stark ab, um mit zunehmender Verbrennungszeit zu verfolgen, als er unter einer Grenze, die als "Grenzzeit" bezeichnet wurde, mit dem Zunahme des Sauerstoffgehalts in der Verbrennungsluft, die PAK -Emissionen signifikant verringert, aber eine unvollständige Oxidation würde Opahs und andere Derivate produzieren [15-17].
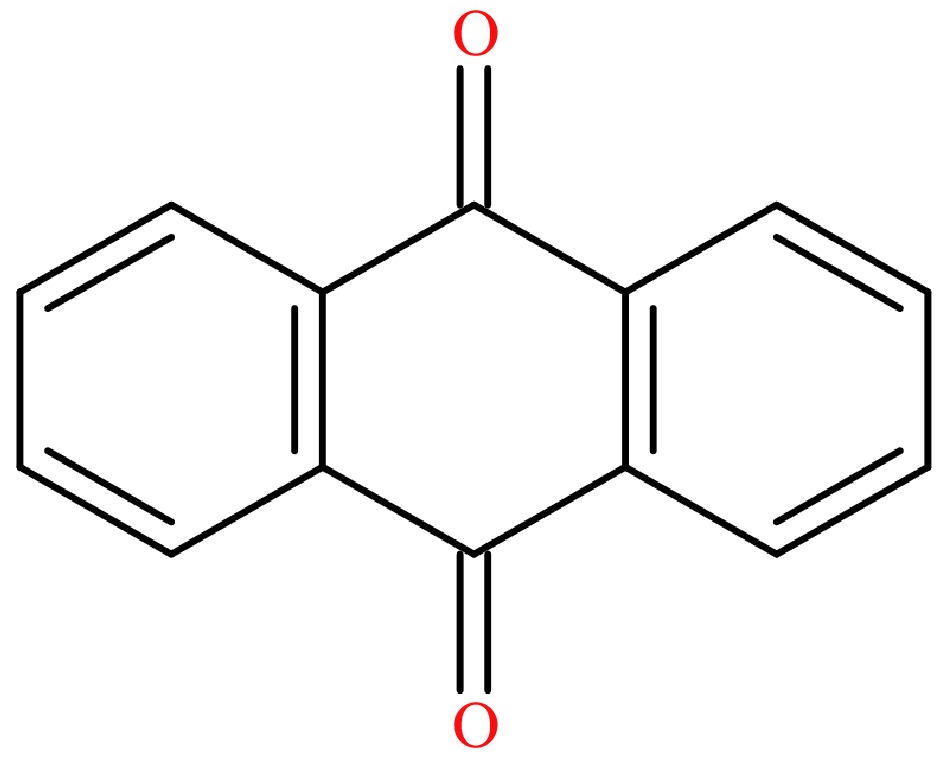
9,10-Anthraquinon (aq, CAS: 84-65-1, Abb. 1), ein sauerstoffhaltiges Derivat von PAK [18], besteht aus drei kondensierten Zyklen. Es wurde 2014 von der Internationalen Agentur für Krebsforschung als möglicher Karzinogen (Gruppe 2B) aufgeführt [19]. AQ kann auf Topoisomerase-II-Spaltkomplex vergiften und die Hydrolyse von Adenosintriphosphat (ATP) durch DNA-Topoisomerase II hemmen, wodurch DNA-Doppelstrangbrüche verursacht werden, was bedeutet, dass die Langzeitbelastung unter AQ-hängende Umgebung und direkter Kontakt mit hohem Niveau mit hohem Niveau zu DNA-Schäden führen und das Risiko von Krebs zu erhöhen. Als negative Auswirkungen auf die menschliche Gesundheit wurde die Europäische Union in Tee in Tee eingestellt. Nach unseren früheren Studien wurden die Ablagerungen von AQ als Hauptquelle während der Teeplantage vorgeschlagen [21]. Basierend auf den experimentellen Folgen bei der Verarbeitung von indonesischen grünen und schwarzen Tee ist es offensichtlich, dass sich der AQ -Spiegel erheblich verändert hat und der Rauch aus der Verarbeitungsausrüstung als einer der Hauptgründe vorgeschlagen wurde [22]. Der genaue Ursprung von AQ in der Teeverarbeitung blieb jedoch schwer fassbar, obwohl einige Hypothesen des AQ -chemischen Signalwegs vorgeschlagen wurden [23, 24], was darauf hinweist, dass es äußerst wichtig ist, die entscheidenden Faktoren zu bestimmen, die den AQ -Spiegel bei der Teeverarbeitung beeinflussen.
Abbildung 1. Die chemische Formel von aq.
Angesichts der Untersuchung der Bildung von AQ während der Kohleverbrennung und der potenziellen Bedrohung durch Kraftstoffe in der Teeverarbeitung wurde ein vergleichendes Experiment durchgeführt, um die Auswirkung der Verarbeitung von Wärmequellen auf AQ in Tee und Luft zu erklären, quantitative Analysen zu den Änderungen des AQ -Gehalts bei verschiedenen Verarbeitungsschritten, was hilfreich ist, um die genaue Herkunft, das Vorkommensmuster und den Grad der AQ -Verarbeitung der AQ -Verarbeitung zu bestätigen.
Ergebnisse
Methodenvalidierung
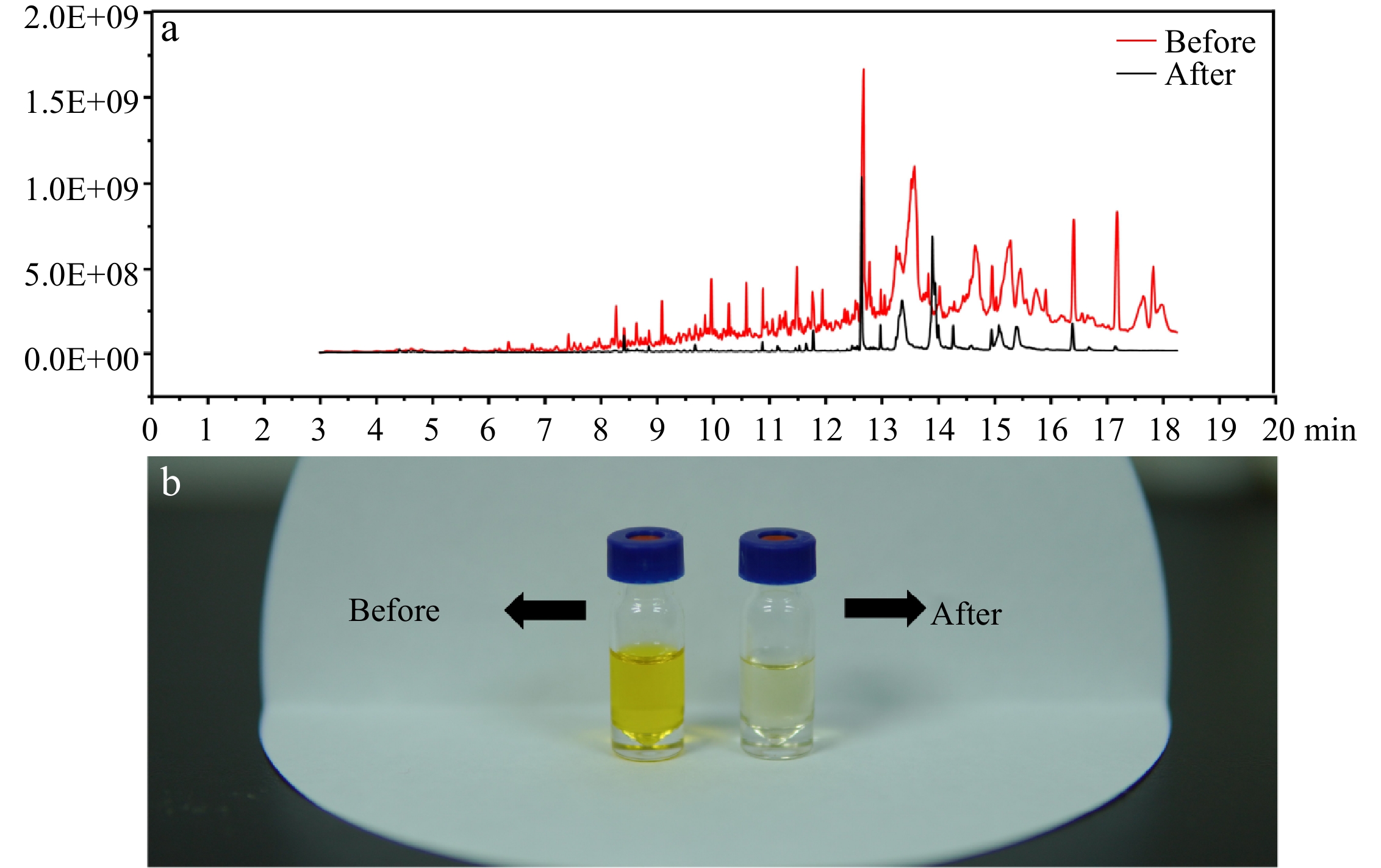
Im Vergleich zu unserer vorherigen Studie [21] wurde vor der Injektion in GC-MS/MS ein Verfahren zur Extraktion von Flüssigkeitsflüssigkeiten kombiniert, um die Empfindlichkeit zu verbessern und instrumentelle Aussagen aufrechtzuerhalten. In Fig. 2B zeigte das verbesserte Verfahren eine signifikante Verbesserung der Reinigung der Probe, das Lösungsmittel wurde leichter. In Fig. 2A zeigte ein vollständiges Scan-Spektrum (50–350 m/z), dass nach der Reinigung die Basislinie des MS-Spektrums offensichtlich reduziert und die weniger chromatographischen Peaks verfügbar waren, was darauf hinweist, dass eine große Anzahl von Interferenzverbindungen nach der Extraktion von Flüssigkeitsflüssigkeiten entfernt wurde.
Abbildung 2. (a) Volles Scan -Spektrum der Probe vor und nach der Reinigung. (b) Der Reinigungseffekt der verbesserten Methode.
Methodenvalidierung, einschließlich Linearität, Wiederherstellung, Quantifizierungsgrenze (LOQ) und Matrixeffekt (ME), sind in Tabelle 1 gezeigt. Es ist zufriedenstellend, die Linearität mit dem Bestimmungskoeffizienten (R2) höher als 0,998 zu erhalten, die zwischen 0,005 und 0,2 mg/kg in der Tea -Matrix und Acetonitrile -Solvents und Acetonitrile -Solvents und Acetonitrilen -Solvents und Acetonitril -Solvents lagen.
Die Wiederherstellung von AQ wurde bei drei Stachelkonzentrationen zwischen gemessenen und tatsächlichen Konzentrationen im trockenen Tee (0,005, 0,02, 0,05 mg/kg), frischen Teeaufnahmen (0,005, 0,01, 0,02 mg/kg) und Luftprobe (0,5, 1,5, 3 μg/m3) bewertet. Die Wiederherstellung von AQ im Tee lag zwischen 77,78% und 113,02% im trockenen Tee und von 96,52% bis 125,69% bei Teebrühnen, wobei RSD% weniger als 15% war. Die Wiederherstellung von AQ in Luftproben lag zwischen 78,47% und 117,06% mit RSD% unter 20%. Die niedrigste Spiked -Konzentration wurde als LOQ identifiziert, die 0,005 mg/kg, 0,005 mg/kg und 0,5 μg/m³ in Teeaufnahmen, trockenen Tee und Luftproben betrug. Wie in Tabelle 1 aufgeführt, erhöhte die Matrix aus trockenem Tee und Tee die AQ -Reaktion leicht, was zu ME von 109,0% und 110,9% führte. Was die Matrix der Luftproben betrifft, betrug das ME 196,1%.
Die Ebenen von AQ während der Verarbeitung von grüner Tee
Mit dem Ziel, die Auswirkungen verschiedener Wärmequellen auf die Tee- und Verarbeitungsumgebung herauszufinden, wurde eine Menge frischer Blätter in zwei spezifische Gruppen unterteilt und in zwei Verarbeitungsworkshops im selben Unternehmen getrennt verarbeitet. Eine Gruppe wurde mit Strom und der anderen mit Kohle versorgt.
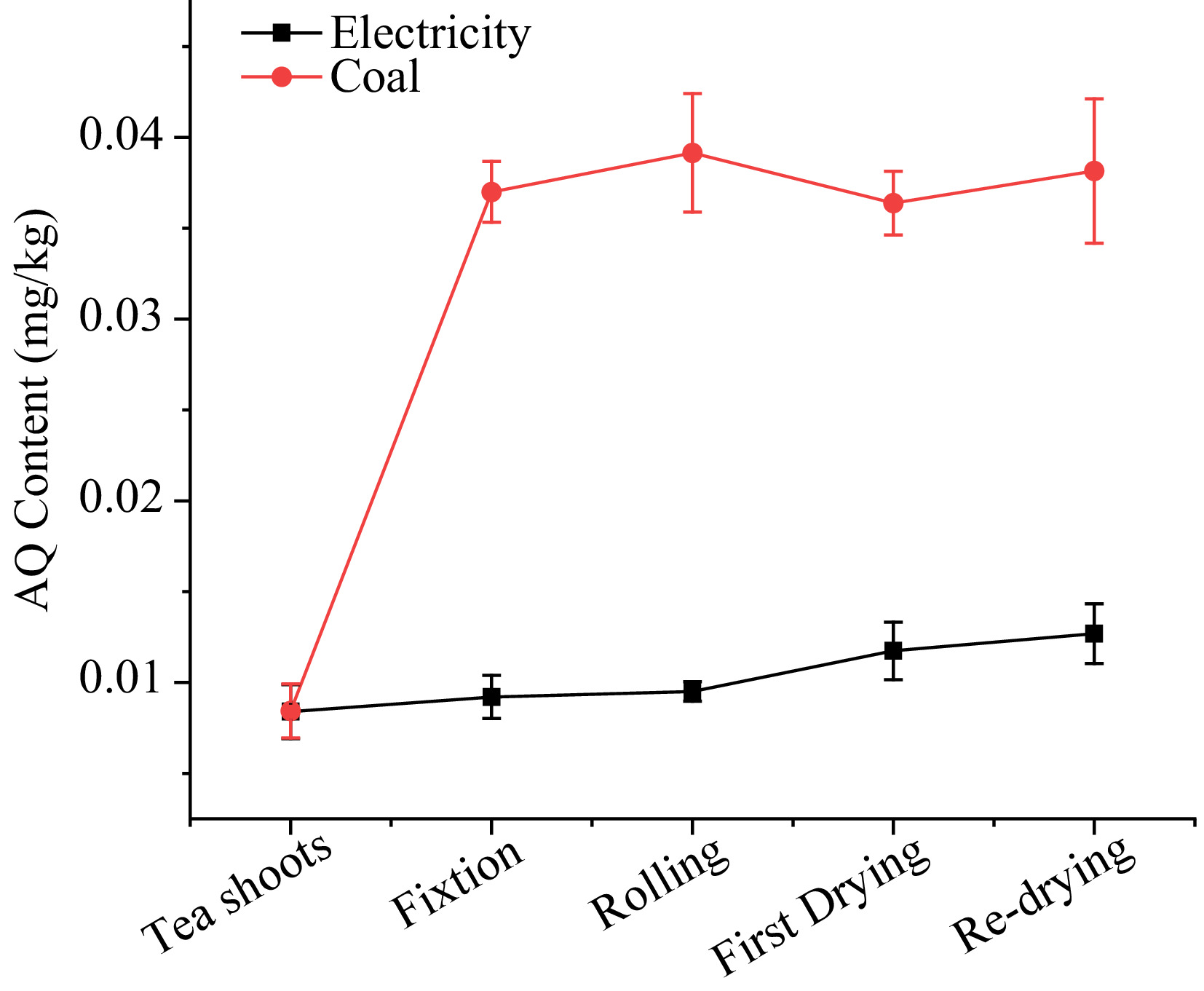
Wie in Fig. 3 gezeigt, lag der AQ -Wert mit Elektrizität als Wärmequelle zwischen 0,008 und 0,013 mg/kg. Während des Fixierungsprozesses führte das Pergament von Teeblättern, die durch die Verarbeitung in einem Topf mit hoher Temperatur verursacht wurden, zu einem Anstieg des AQ um 9,5%. Anschließend blieb der AQ -Niveau trotz des Saftverlusts während des Rolling -Prozesses, was darauf hindeutet, dass physikalische Prozesse möglicherweise den Niveau der AQ bei der Teeverarbeitung nicht beeinflussen. Nach den ersten Trocknungsschritten stieg der AQ-Spiegel leicht von 0,010 auf 0,012 mg/kg und stieg dann bis zum Ende der Wiederfahrt weiter auf 0,013 mg/kg an. PFS, die die Variation in jedem Schritt signifikant zeigten, betrugen 1,10, 1,03, 1,24, 1,08 in Fixierung, Rollen, zuerst Trocknen bzw. Wiedertrocknungen. Die Ergebnisse von PFS deuten darauf hin, dass die Verarbeitung unter elektrischer Energie einen leichten Einfluss auf die AQ -Niveaus im Tee hatte.
Abbildung 3. Der AQ -Wert während der Verarbeitung von grünem Tee mit Strom und Kohle als Wärmequellen.
Bei Kohle als Wärmequelle nahm der AQ -Gehalt während der Teeverarbeitung stark zu und stieg von 0,008 auf 0,038 mg/kg. 338,9% AQ waren im Fixierungsverfahren erhöht und erreichten 0,037 mg/kg, was die von der Europäischen Union festgelegte MRL von 0,02 mg/kg weit überstieg. Während der Rollstufe stieg der Niveau des AQ immer noch um 5,8%, obwohl es weit vom Fixierungsgerät entfernt war. Beim ersten Trocknen und Neutrocknen nahm der AQ-Gehalt wenig zu oder nahm geringfügig ab. Die PFS, die Kohle als Wärmequelle in der Fixierung, zum Ersttrocknen und der Wiederentrocknung verwendete, betrug 4,39, 1,05, 0,93 bzw. 1,05.
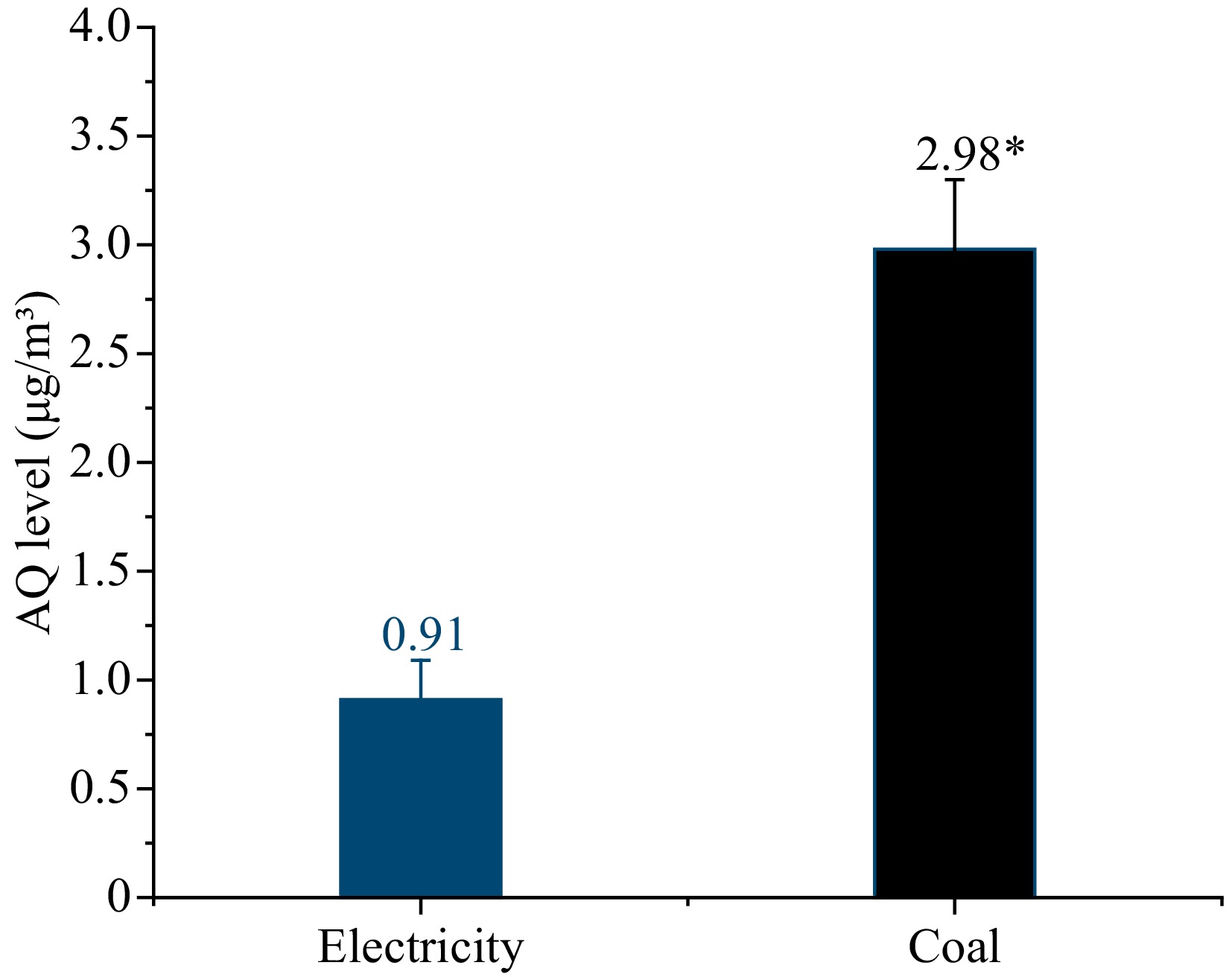
Um die Beziehung zwischen der Kohleverbrennung und der AQ -Verschmutzung weiter zu bestimmen, wurden die suspendierten Partikel (PMS) in den Workshops unter beiden Wärmequellen zur Luftbewertung gesammelt, wie in Abb. 4 gezeigt. Der AQ -Spiegel von PMS mit Kohlequelle betrug 2,98 μg/m3, was über dreimal höher als bei Elektrizität 0,91 μg/m3.
Abbildung 4. Die AQ -Werte in der Umgebung mit Strom und Kohle als Wärmequelle. * Zeigt signifikante Unterschiede in den AQ -Spiegeln in den Proben an (p <0,05).
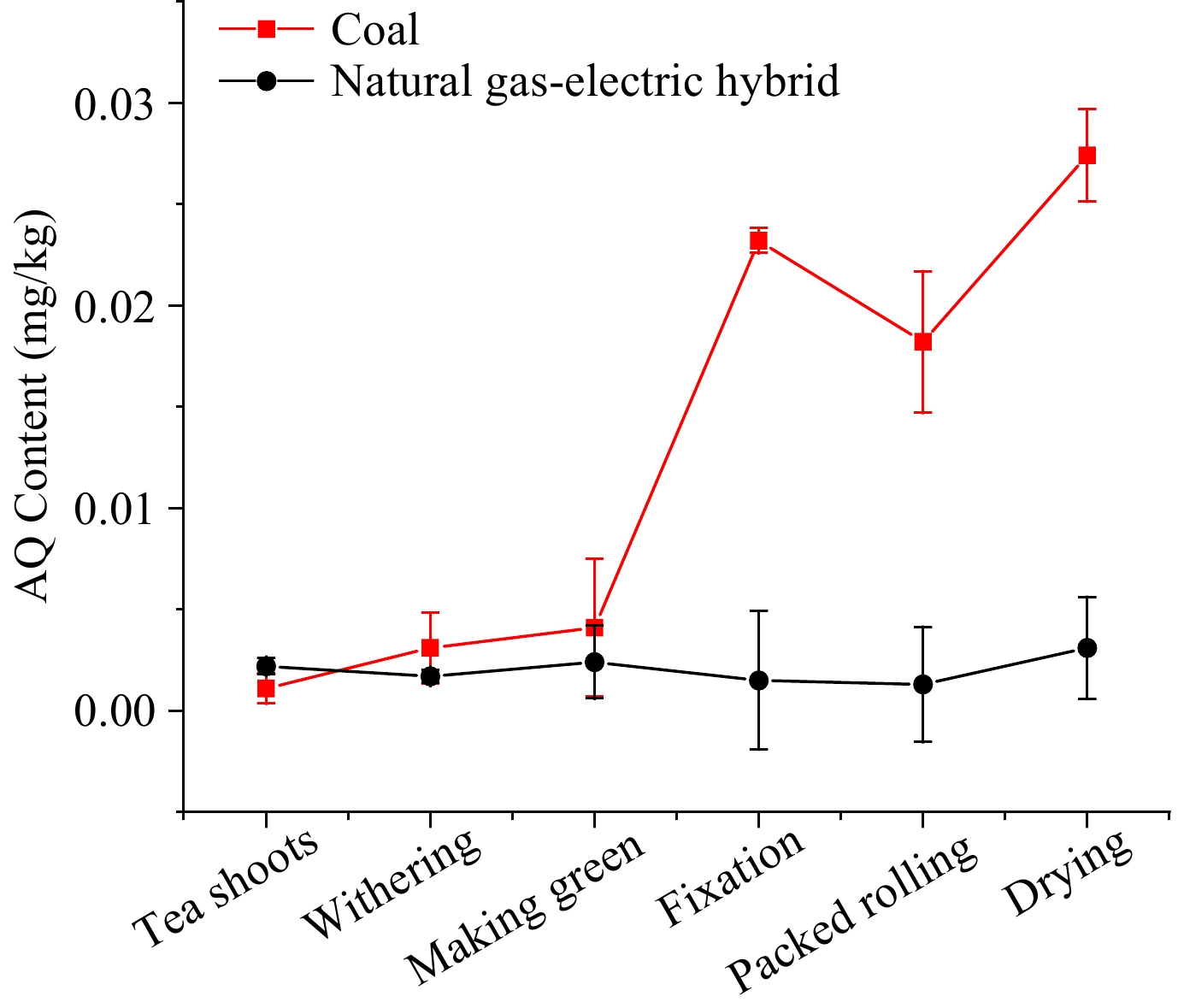
Die Niveaus von AQ während der Oolong -Tee -Verarbeitung von Oolong -Tee, die hauptsächlich in Fujian und Taiwan hergestellt werden, ist eine Art teilweise fermentierter Tee. Um die Hauptschritte des zunehmenden AQ-Spiegels und die Auswirkungen verschiedener Brennstoffe weiter zu bestimmen, wurde gleichzeitig die gleiche Menge frischer Blätter in Oolong-Tee mit Kohle- und Erdgaselektrik-Hybrid wie Wärmequellen verarbeitet. Die AQ-Werte in der Oolong-Teeverarbeitung unter Verwendung verschiedener Wärmequellen sind in Abb. 5 dargestellt. Für die Oolong-Teeverarbeitung mit Erdgaselektrik-Hybrid stagnierte der Trend des AQ-Spiegels unter 0,005 mg/kg, was dem in grünem Tee mit Elektrizität ähnlich war.
Abbildung 5. Der AQ-Spiegel während der Oolong-Teeverarbeitung mit Erdgaselektrikmischung und Kohle als Wärmequelle.
Mit Kohle als Wärmequelle waren die AQ-Werte in den ersten beiden Schritten, die verdorrend und grün machen, im Wesentlichen die gleichen wie bei Erdgaselektrikmischungen. Die nachfolgenden Verfahren bis zur Fixierung zeigten jedoch, dass sich die Lücke allmählich weit verbreiterte. Zu diesem Zeitpunkt stieg der AQ -Wert von 0,004 auf 0,023 mg/kg. Der Niveau im gepackten Rollschritt nahm auf 0,018 mg/kg ab, was auf den Verlust von Teesaft zurückzuführen sein kann, der einige von AQ -Schadstoffen abnimmt. Nach der Rollstufe stieg der Niveau in der Trocknungsstufe auf 0,027 mg/kg. Beim Verdampfen, Grünen, Fixierung, gepacktes Rollen und Trocknen betrugen die PFS 2,81, 1,32, 5,66, 0,78 bzw. 1,50.
Das Auftreten von AQ in Teeprodukten mit unterschiedlichen Wärmequellen
Um die Auswirkungen auf den AQ -Gehalt von Tee mit unterschiedlichen Wärmequellen zu bestimmen, wurden 40 Teeproben aus den Tee -Workshops unter Verwendung von Elektrizität oder Kohle als Wärmequellen analysiert, wie in Tabelle 2 gezeigt. Im Vergleich zur Verwendung von Elektrizität als Wärmequelle wiesen Kohle die meisten Detektivraten (85,0%) mit dem maximalen AQ -Wert von 0,064 mg. Die Rate von 35,0% wurde in Kohleproben beobachtet. Am auffälligsten war, dass Strom die niedrigsten Detektiv- und Excedance -Raten von 56,4% bzw. 7,7% mit dem maximalen Gehalt von 0,020 mg/kg hatte.
DISKUSSION
Basierend auf den PFs während der Verarbeitung mit den beiden Arten von Wärmequellen war klar, dass die Fixierung der Hauptschritt war, der zu einer Erhöhung der AQ -Werte in der Teeproduktion mit Kohle und Verarbeitung unter elektrischer Energie führte, hatte einen leichten Einfluss auf den Gehalt an aq in Tee. Während der Verarbeitung von grünem Tee erzeugte die Kohleverbrennung im Vergleich zum elektrischen Heizungsprozess eine Menge Dämpfe im Fixierungsprozess, was darauf hinweist, dass möglicherweise Dämpfe die Hauptquelle für AQ -Schadstoffe aus Kontakt mit Teeaufnahmen in der Teeverarbeitung waren, ähnlich dem Expositionsprozess in den geräucherten Grillproben [25]. Die geringfügige Zunahme des AQ -Gehalts während der Rollstufe deutete darauf hin, dass die durch Kohleverbrennung verursachten Dämpfe nicht nur den AQ -Niveau während des Fixierungsschritts, sondern auch in der Verarbeitungsumgebung aufgrund der atmosphärischen Ablagerung beeinflussten. Kohlen wurden auch als Wärmequelle beim ersten Trocknen und Neutrocknen verwendet, aber in diesen beiden Schritten nahm der AQ-Gehalt leicht zu oder nahm leicht ab. Dies kann durch die Tatsache erklärt werden, dass der geschlossene Heiß-Wind-Trockner Tee von Dämpfen fernhielt, die durch Kohleverbrennung verursacht wurden [26]. Um die Schadstoffquelle zu bestimmen, wurden die AQ -Werte in der Atmosphäre analysiert, was zu einer signifikanten Lücke zwischen den beiden Workshops führte. Der Hauptgrund dafür ist, dass die in der Fixierung verwendete Kohle, das erste Trocknungs- und WiederverdrY-Stadien während einer unvollständigen Verbrennung AQ erzeugen würde. Diese AQ wurden dann nach Kohleverbrennung in den kleinen Partikeln von Feststoffe adsorbiert und in der Luft verteilt, wodurch die AQ -Verschmutzung in der Workshop -Umgebung erhöht wurde [15]. Im Laufe der Zeit setzten sich diese Partikel aufgrund der großen spezifischen Oberfläche und der Adsorptionskapazität von Tee auf der Oberfläche der Teeblätter ab, was zu einer Zunahme der AQ in der Produktion führte. Daher wurde angenommen, dass Kohleverbrennung die Hauptroute ist, die zu einer übermäßigen AQ -Kontamination bei der Teeverarbeitung führte, wobei die Dämpfe die Quelle der Verschmutzung sind.
Bei der Oolong -Teeverarbeitung wurde AQ mit beiden Wärmequellen verarbeitet, aber der Unterschied zwischen den beiden Wärmequellen war signifikant. Die Ergebnisse deuten auch darauf hin, dass Kohle als Wärmequelle eine wichtige Rolle bei der Erhöhung des AQ -Niveaus spielte, und die Fixierung wurde als Hauptschritt zur Erhöhung der AQ -Kontamination bei der Oolong -Teeverarbeitung angesehen, die auf den PFs basiert. Während der Oolong-Teeverarbeitung mit Erdgaselektrik-Hybrid als Wärmequelle stagnierte der Trend des AQ-Spiegels unter 0,005 mg/kg, was dem bei grünem Tee mit Strom ähnlich war, was darauf hindeutet, dass saubere Energie wie Elektrizität und Erdgas das Risiko der Erzeugung von AQ-Kontaminanten durch die Verarbeitung verringern kann.
In Bezug auf Probenahmestests zeigten die Ergebnisse, dass die Situation der AQ -Verunreinigung schlechter war, wenn Kohle als Wärmequelle anstelle von Elektrizität verwendet wurde, was auf die Dämpfe aus der Verbrennung von Kohle zurückzuführen sein könnte, die mit Teeblättern in Kontakt kommen und am Arbeitsplatz annimmt. Obwohl es offensichtlich war, dass Elektrizität die sauberste Wärmequelle während der Teeverarbeitung war, gab es in Teeprodukten immer noch AQ -Verunreinigungen mit Elektrizität als Wärmequelle. Die Situation scheint den zuvor veröffentlichten Arbeiten leicht ähnlich zu sein, bei denen die Reaktion von 2-Alkenalen mit Hydroquinonen und Benzochinonen als potenzieller chemischer Weg vorgeschlagen wurde [23], Gründe dafür werden in zukünftigen Forschungen untersucht.
Schlussfolgerungen
In dieser Arbeit wurden die möglichen Quellen der AQ-Verschmutzung in Grün- und Oolong-Tee durch vergleichende Experimente bestätigt, die auf verbesserten GC-MS/MS-Analysemethoden basieren. Unsere Ergebnisse stützten direkt, dass die Hauptschadstoffquelle für hohe AQ -Werte durch Verbrennung verursacht wurde, was nicht nur die Verarbeitungsphasen, sondern auch die Workshop -Umgebungen beeinflusste. Anders als in den Roll- und Withing -Phasen, in denen die Änderungen des AQ -Niveaus unauffällig waren, sind die Stufen mit direkter Beteiligung von Kohle und Brennholz, wie z. B. Fixierung, der Hauptprozess, bei dem die AQ -Kontamination aufgrund der Kontaktmenge zwischen Tee und Dämpfen während dieser Phasen stieg. Daher wurden saubere Brennstoffe wie Erdgas und Strom als Wärmequelle bei der Verarbeitung von Tee empfohlen. Darüber hinaus zeigten die experimentellen Ergebnisse auch, dass in Abwesenheit von durch Verbrennung erzeugten Dämpfen noch andere Faktoren zur Verfolgung von AQ während der Teeverarbeitung beitrugen, während kleine Mengen an AQ auch im Workshop mit sauberen Brennstoffen beobachtet wurden, die in zukünftigen Forschungen weiter untersucht werden sollten.
MATERIALEN UND METHODEN
Reagenzien, Chemikalien und Materialien
Anthrachinone Standard (99,0%) wurde von der Dr. Ehrenstorfer GmbH Company (Augsburg, Deutschland) gekauft. Der interne Standard von D8-Anthraquinon (98,6%) wurde von C/D/N-Isotopen (Quebec, Kanada) gekauft. Wasserfreies Natriumsulfat (Na2SO4) und Magnesiumsulfat (MgSO4) (Shanghai, China). Florisil wurde von Wenzhou Organic Chemical Company (Wenzhou, China) geliefert. Mircro-Glass Fibre Paper (90 mm) wurde von Ahlstrom-Munksjö Company (Helsinki, Finnland) gekauft.
Probenvorbereitung
Die grün-Tee-Proben wurden mit Fixierung, Rollen, Ersttrocknen und Wiederverlangen (mit geschlossenen Geräten) verarbeitet, während die Oolong-Tee-Proben mit Verdosen, Grün (rocken und frischer Blätter abwechselnd), Fixierung, gepacktes Rollen und Trocknen verarbeitet wurden. Proben aus jedem Schritt wurden dreimal bei 100 g nach gründlichem Mischen gesammelt. Alle Proben wurden zur weiteren Analyse bei –20 ° C gelagert.
Luftproben wurden mit Glasfaserpapier (90 mm) unter Verwendung von Probensteinen mit mittlerem Volumen (PTS-100, Qingdao Laoshan Electronic Instrument Company, Qingdao, China) [27] bei 100 l/min für 4 Stunden gesammelt.
Die befestigten Proben wurden mit einem AQ bei 0,005 mg/kg, 0,010 mg/kg, 0,020 mg/kg für frische Teeaufnahmen, bei 0,005 mg/kg, 0,020 mg/kg, 0,050 mg/kg für trockene Tee und bei 0,012 mg/kg (0,5 µg/m3), 0,012 mg/kg (0,5 µg/m3), 0,036 mg/kg (0,5 µg/m3), versetzt. Luft Smaple), 0,072 mg/kg (3,0 µg/m3 für die Luftprobe) für Glasfilterpapier. Nach gründlichem Schütteln wurden alle Proben 12 Stunden lang gelassen, gefolgt von Extraktions- und Reinigungsschritten.
Der Feuchtigkeitsgehalt wurde erhalten, indem nach dem Mischen von 20 g der Probe nach jedem Schritt, Erhitzen bei 105 ° C für 1 h, gewogen und dreimal gewogen und wiederholt und den Durchschnittswert genommen und durch das Gewicht vor dem Erhitzen geteilt wurde.
Probenextraktion und Reinigung
Teeprobe: Die Extraktion und Reinigung von AQ aus Teeproben wurde basierend auf der veröffentlichten Methode von Wang et al. mit mehreren Anpassungen [21]. Kurz gesagt wurden 1,5 g Teeproben zuerst mit 30 & mgr; l D8-AQ (2 mg/kg) gemischt und 30 Minuten lang stehen, dann gut mit 1,5 ml entionisiertem Wasser gemischt und 30 Minuten lang gelassen. 15 ml 20% Aceton in N-Hexan wurde zu den Teeproben gegeben und 15 Minuten lang beschrieben. Dann wurden die Proben 30 s mit 1,0 g mgso4 verwirbelt und 5 Minuten lang bei 11.000 U / min zentrifugiert. Nachdem sie auf 100 ml birnenförmige Kolben bewegt worden waren, wurden 10 ml der oberen organischen Phase bei 37 ° C zu fast Trockenheit unter Vakuum eingedampft. 5 ml 2,5% Aceton in N-Hexan lösten den Extrakt zur Reinigung in birnenförmigen Flaschen um. Die Glassäule (10 cm × 0,8 cm) bestand von unten nach Oberseite der Glaswolle und 2 g Florisil, die zwischen zwei Schichten von 2 cm Na2SO4 lag. Dann verschob 5 ml 2,5% Aceton in N-Hexan die Säule. Nach dem Laden der aufgenommenen Lösung wurde AQ dreimal mit 5 ml, 10 ml, 10 ml 2,5% Aceton in N-Hexan eluiert. Die kombinierten Eluaten wurden in birnenförmige Flaschen übertragen und unter Vakuum bei 37 ° C zu fast Trockenheit verdampft. Der getrocknete Rückstand wurde dann mit 1 ml 2,5% Aceton in Hexan rekonstituiert, gefolgt von einer Filtration durch einen 0,22 uM Porengrößenfilter. Dann wurde die rekonstituierte Lösung mit Acetonitril bei einem Volumenverhältnis von 1: 1 gemischt. Nach dem Schüttelschritt wurde der Unternat für GC-MS/MS-Analyse verwendet.
Luftprobe: Die Hälfte des Faserpapiers, das mit 18 μl D8-AQ (2 mg/kg) tropft, wurde in 15 ml 20% Aceton in N-Hexan eingetaucht und dann 15 Minuten lang beschallt. Die organische Phase wurde durch 5-minütige Zentrifugation bei 11.000 U / min getrennt und die gesamte obere Schicht wurde in einem birnenförmigen Kolben entfernt. Alle organischen Phasen wurden unter Vakuum bei 37 ° C zu fast Trockenheit verdampft. 5 ml 2,5% Aceton in Hexan haben die Extrakte zur Reinigung auf die gleiche Weise wie in den Teeproben entleert.
GC-MS/MS-Analyse
Varian 450 Gaschromatograph mit Varian 300 Tandem -Massendetektor (Varian, Walnut Creek, CA, USA) wurde verwendet, um die AQ -Analyse mit MS Workstation Version 6.9.3 Software durchzuführen. Varianfaktor vier Kapillarsäulen-VF-5ms (30 m × 0,25 mm × 0,25 μm) wurden zur chromatographischen Trennung verwendet. Das Trägergas Helium (> 99,999%) wurde auf eine konstante Durchflussrate von 1,0 ml/min mit Kollisionsgas von Argon (> 99,999%) eingestellt. Die Ofentemperatur begann von 80 ° C und wurde 1 min gehalten; Erhöht bei 15 ° C/min bis 240 ° C, dann 260 ° C bei 20 ° C/min erreicht und 5 min gehalten. Die Temperatur der Ionenquelle betrug 210 ° C sowie die Übertragungsleitentemperatur von 280 ° C. Das Injektionsvolumen betrug 1,0 & mgr; l. Die MRM -Bedingungen sind in Tabelle 3 dargestellt.
Agilent 8890 Gaschromatograph mit Agilent 7000D Triple Quadrupol -Massenspektrometer (Agilent, Stevens Creek, CA, USA) wurde verwendet, um den Reinigungseffekt mit der Software Masshunter Version 10.1 zu analysieren. Die Agilent J & W HP-5MS-GC-Säule (30 m × 0,25 mm × 0,25 μm) wurde zur chromatographischen Trennung verwendet. Das Trägergas Helium (> 99,999%) wurde auf eine konstante Durchflussrate von 2,25 ml/min mit Kollisionsgas von Stickstoff (> 99,999%) eingestellt. Die Temperatur der EI -Ionenquelle wurde bei 280 ° C eingestellt, genau wie die Übertragungsleitentemperatur. Die Ofentemperatur begann von 80 ° C und wurde 5 Minuten lang gehalten. Angehoben von 15 ° C/min bis 240 ° C, dann 280 ° C bei 25 ° C/min erreicht und 5 min gehalten. Die MRM -Bedingungen sind in Tabelle 3 dargestellt.
Statistische Analyse
Der AQ -Gehalt in frischen Blättern wurde durch Dividierung durch Feuchtigkeitsgehalt auf Trockenmassengehalt korrigiert, um die AQ -Werte während der Verarbeitung zu vergleichen und zu analysieren.
Die Änderungen von AQ in Teeproben wurden mit Microsoft Excel -Software und IBM SPSS Statistics 20 bewertet.
Der Verarbeitungsfaktor wurde verwendet, um die Änderungen in der AQ während der Teeverarbeitung zu beschreiben. PF = RL/RF, wobei RF die AQ -Ebene vor dem Verarbeitungsschritt und RL ist und die AQ -Ebene nach dem Verarbeitungsschritt ist. PF zeigt eine Abnahme (PF <1) oder eine Erhöhung (PF> 1) in einem AQ -Rest während eines bestimmten Verarbeitungsschritts an.
ME zeigt eine Abnahme (ME <1) oder eine Erhöhung (ME> 1) als Reaktion auf die analytischen Instrumente an, die auf dem Verhältnis von Kalibrierungshängen in der Matrix und Lösungsmittel wie folgt basiert:
ME = (Slopematrix/Slopesolvent - 1) × 100%
Dabei ist Slopematrix die Neigung der Kalibrierungskurve in matrixanpassender Lösungsmittel, das Slopesolvent ist die Neigung der Kalibrierungskurve in Lösungsmittel.
Anerkennung
Diese Arbeit wurde durch das Hauptprojekt für Wissenschaft und Technologie in der Provinz Zhejiang (2015C12001) und der National Science Foundation of China (42007354) unterstützt.
Interessenkonflikt
Die Autoren erklären, dass sie keinen Interessenkonflikt haben.
Rechte und Berechtigungen
Copyright: © 2022 durch den Autor (en). Exklusiver Lizenznehmer Maximal Academic Press, Fayetteville, GA. Dieser Artikel ist ein Open -Access -Artikel, der unter Creative Commons Attribution License (CC von 4.0) verteilt ist, besuchen Sie https://creativecommons.org/licenses/by/4.0/.
Referenzen
[1] ITC. 2021. Jährliches Bulletin der Statistik 2021. Https://inttea.com/publication/
[2] Hicks A. 2001. Überprüfung der globalen Teeproduktion und die Auswirkungen auf die Industrie der asiatischen wirtschaftlichen Situation. Au Journal of Technology 5
Google Scholar
[3] Katsuno T., Kasuga H., Kusano Y., Yaguchi Y., Tomomura M., et al. 2014. Charakterisierung von Geruchsverbindungen und ihre biochemische Bildung in grünem Tee mit einem Speicherprozess mit niedriger Temperatur. Food Chemistry 148: 388–95 doi: 10.1016/j.foodchem.2013.10.069
Crossref Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Tri-DiMesion Pollution Chain im Tee-Ökosystem und seine Kontrolle. Scientia Agricultura Sinica 40: 948–58
Google Scholar
[5] Er H, Shi L, Yang G, You M, Vasseur L. 2020. Bewertung des Ökologischen Risikos von Bodenmetallen und Pestizidresten in Teeplantagen. Landwirtschaft 10:47 doi: 10.3390/Landwirtschaft10020047
Crossref Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J, et al. 2005. Bleikontamination in Teeblättern und nicht-edaphischen Faktoren, die sie beeinflussen. Chemosphäre 61: 726–32 doi: 10.1016/j.chemosphere.2005.03.053
Crossref Google Scholar
[7] Owuor PO, Obaga SO, Othieno CO. 1990. Die Auswirkungen der Höhe auf die chemische Zusammensetzung von schwarzem Tee. Journal of the Science of Food and Agriculture 50: 9–17 DOI: 10.1002/JSFA.2740500103
Crossref Google Scholar
[8] Garcia Londoño VA, Reynoso M., Resnik S. 2014. Polycyclische aromatische Kohlenwasserstoffe (PAK) in Yerba Mate (Ilex paraguariensis) vom argentinischen Markt. Lebensmittelzusatze & Kontaminanten: Teil B 7: 247–53 DOI: 10.1080/19393210.2014.919963
Crossref Google Scholar
[9] Ishizaki A, Saito K., Hanioka N., Narimatsu S., Kataoka H. 2010. Bestimmung von polycyclischen aromatischen Kohlenwasserstoffen in Lebensmittelproben durch automatisierte Online-In-Line-In-Tube-Festphasen-Mikroextraktionsdetektion, die mit Hochleistungsflüssigkeits-Flüssigchomatographie-Fluorescencencencence-Fluorescencence-Fluorescencencarbons gekoppelt sind. Journal of Chromatography A 1217: 5555–63 doi: 10.1016/j.chroma.2010.06.068
Crossref Google Scholar
[10] Phan Thi La, Ngoc NT, Quynh NT, Thanh NV, Kim TT, et al. 2020. Polycyclische aromatische Kohlenwasserstoffe (PAK) in trockenen Teeblättern und Tee -Infusionen in Vietnam: Kontaminationsniveau und Bewertung des Ernährungsrisikos. Umweltgeochemie und Gesundheit 42: 2853–63 DOI: 10.1007/S10653-020-00524-3
Crossref Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. Das Auftreten von 16 EPA -PAK -In -Foods - Eine Überprüfung. Polycyclische aromatische Verbindungen 35: 248–84 DOI: 10.1080/10406638.2014.918550
Crossref Google Scholar
[12] Omodara NB, Olabemiwo Om, Adedosu TA. 2019. Vergleich von PAK, die in Brennholz- und Holzkohle -Raucher- und Katzenfischen gebildet wurden. American Journal of Food Science and Technology 7: 86–93 DOI: 10.12691/AJFST-7-3-3
Crossref Google Scholar
[13] Zou Ly, Zhang W., Atkiston S. 2003. Die Charakterisierung polyzyklischer aromatischer Kohlenwasserstoffe aus dem Verbrennen verschiedener Brennholzarten in Australien. Umweltverschmutzung 124: 283–89 DOI: 10.1016/S0269-7491 (02) 00460-8
Crossref Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL, et al. 2000. Aktivität von Benzo [A] Pyren und seinen hydroxylierten Metaboliten in einem Östrogenrezeptor-α-Reporter-Gen-Assay. Toxikologische Wissenschaften 55: 320–26 doi: 10.1093/toxsci/55.2.320
Crossref Google Scholar
[15] Han Y, Chen Y, Ahmad S., Feng Y, Zhang F, et al. 2018. Hochzeit und größenaufgelöste Messungen der PM- und chemischen Zusammensetzung aus Kohleverbrennung: Implikationen für den EC-Bildungsprozess. Umweltwissenschaft und Technologie 52: 6676–85 DOI: 10.1021/ACS.EST.7B05786
Crossref Google Scholar
[16] Khiadani (Hajian) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M, et al. 2013. Bestimmung der polyzyklischen aromatischen Kohlenwasserstoffekonzentration in acht Marken mit schwarzem Tee, die im Iran mehr verwendet werden. Internationales Journal of Environmental Health Engineering 2:40 doi: 10.4103/2277-9183.122427
Crossref Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J., Andrews G., Jones JM, et al. 2007. Emission von sauerstoffhaltigen Spezies aus der Verbrennung von Kiefernholz und ihrer Beziehung zur Rußbildung. Prozesssicherheit und Umweltschutz 85: 430–40 doi: 10.1205/psep07020
Crossref Google Scholar
[18] Shen G., Tao S., Wang W., Yang Y., Ding J. et al. 2011. Emission von sauerstoffhaltigen polycyclischen aromatischen Kohlenwasserstoffen aus der massiven Brennstoffverbrennung in Innenräumen. Umweltwissenschaft und Technologie 45: 3459–65 DOI: 10.1021/ES104364t
Crossref Google Scholar
[19] Internationale Agentur für Krebsforschung (IARC), Weltgesundheitsorganisation. 2014. Diesel- und Benzinmotorabgas und einige Nitroarene. Internationale Agentur für Erforschung von Krebsmonographien zur Bewertung krebserzeugter Risiken für den Menschen. Bericht. 105: 9
[20] de Oliveira Galvão MF, De Oliveira Alves N., Ferreira PA, Caumo S., De Castro Vasconcellos P. et al. 2018. Biomasse-Verbrennungspartikel in der brasilianischen Amazonasregion: Mutagene Wirkungen von Nitro- und Oxy-PaHs und Bewertung von Gesundheitsrisiken. Umweltverschmutzung 233: 960–70 doi: 10.1016/j.envpol.2017.09.068
Crossref Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H, et al. 2018. 9,10-Anthroquinon-Ablagerung in Teeplantagen könnte einer der Gründe für die Kontamination im Tee sein. Food Chemistry 244: 254–59 doi: 10.1016/j.foodchem.2017.09.123
Crossref Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Identifizierung von 9,10-Anthroquinon-Kontamination während der Verarbeitung von Schwarz- und Grüntee in Indonesien. Lebensmittelchemie 327: 127092 DOI: 10.1016/j.foodchem.2020.127092
Crossref Google Scholar
[23] Zamora R, Hidalgo FJ. 2021. Bildung von Naphthochinonen und Anthrachinonen durch Carbonyl-Hydrochinon/Benzochinon-Reaktionen: Ein potenzieller Route für den Ursprung von 9,10-Anthroquinon im Tee. Food Chemistry 354: 129530 doi: 10.1016/j.foodchem.2021.129530
Crossref Google Scholar
[24] Yang M., Luo F., Zhang X., Wang X., Sun H. et al. 2022. Aufnahme, Translokation und Stoffwechsel von Anthracen in Teepflanzen. Wissenschaft des Gesamtumfelds 821: 152905 doi: 10.1016/j.scitotenv.2021.152905
Crossref Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019. Einfluss des Rauchens und Grillens auf den Inhalt von Anthraquinon (ATQ) und polycyclischer aromatischer Kohlenwasserstoffe (PAK) in Frankfurter-Wurst. Journal of Agricultural and Food Chemistry 67: 13998–4004 doi: 10.1021/acs.jafc.9b03316
Crossref Google Scholar
[26] Fouillaud M., Caro Y., Venkatachalam M., Grondin I., Dufossé L. 2018. Anthraquinones. In phenolischen Verbindungen in Lebensmittel: Charakterisierung und Analyse, Hrsg. Leo Ml.vol. 9. Boca Raton: CRC Press. S. 130–70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muniategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, et al. 2003. Eine neue Methode zur gleichzeitigen Bestimmung von PAK und Metallen in Proben von atmosphärischen Partikeln. Atmosphärische Umgebung 37: 4171–75 doi: 10.1016/s1352-2310 (03) 00523-5
Crossref Google Scholar
Über diesen Artikel
Zitieren Sie diesen Artikel
Yu J., Zhou L., Wang X., Yang M., Sun H. et al. 2022. 9,10-Anthroquinon-Kontamination in der Teeverarbeitung unter Verwendung von Kohle als Wärmequelle. Getränkepflanzenforschung 2: 8 DOI: 10.48130/BPR-2022-0008
Postzeit: Mai-09-2022